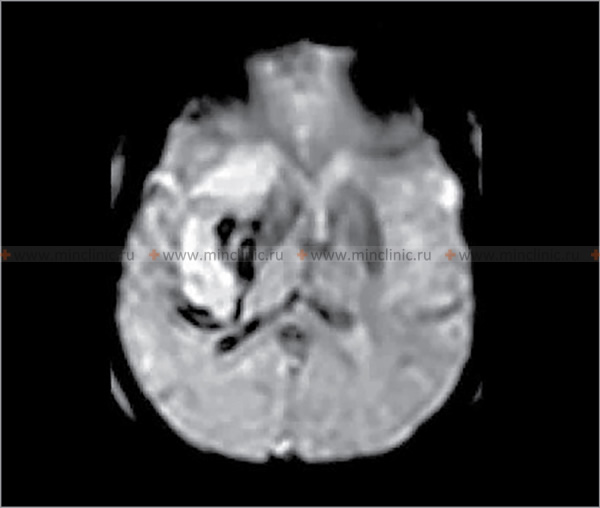
ცერებრული ემბოლია
ცერებრული ემბოლიის მიზეზები
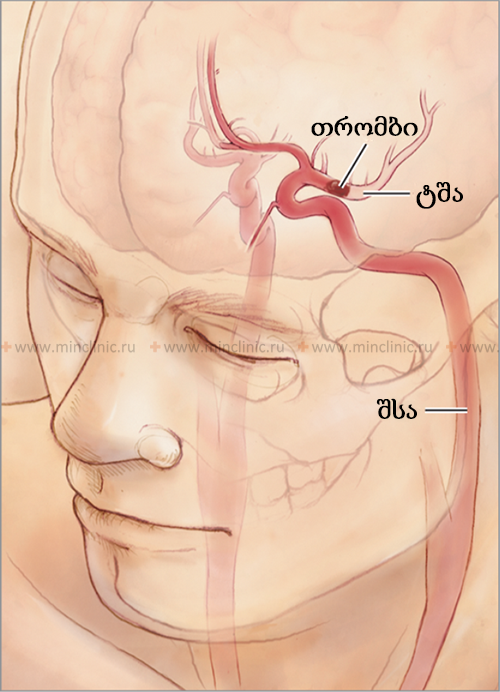
ცერებრული ემბოლია, ემბოლის (მოძრავი ნაწილაკის ან თრომბის) გაჭედვა თავის ტვინის არტერიაში, იშემიური ინსულტის წამყვანი მიზეზია [1, 2]. გული ამ ემბოლიების ყველაზე ხშირი წყაროა (კარდიოემბოლია) [1, 3]. არტერიო-არტერიული ემბოლია, სადაც ემბოლები წარმოიქმნება ათეროსკლეროზული ფოლაქებიდან (ხშირად ასოცირებულ თრომბთან ერთად) თავის ტვინის მკვებავ მსხვილ არტერიებში (როგორიცაა საძილე ან ვერტებრობაზილარული სისტემები), წარმოადგენს კიდევ ერთ მნიშვნელოვან, თუმცა შესაძლოა საერთო ჯამში ნაკლებად ხშირ, მიზეზს [1, 4]. სხვა პოტენციური მიზეზები, როგორიცაა ფილტვის ვენებში წარმოქმნილი თრომბოზი, ცხიმოვანი ემბოლია (ხშირად ლულოვანი ძვლების მოტეხილობის ან ორთოპედიული ოპერაციის შემდეგ), სიმსივნური ემბოლია (სიმსივნის ფრაგმენტების მოხვედრა სისხლის მიმოქცევაში), მარანტული ენდოკარდიტი (არაბაქტერიული ვეგეტაციები გულის სარქველებზე, ტიპურად ქრონიკულად დაავადებულ ან კიბოს მქონე პაციენტებში), პარადოქსული ემბოლია (ვენური კოლტების გადასვლა გულის მარჯვენა მხრიდან მარცხენაში ისეთი დეფექტის მეშვეობით, როგორიცაა ღია ოვალური ხვრელი) და გართულებები კისრის ან გულმკერდის ოპერაციის შემდეგ, შედარებით იშვიათად ითვლება [1, 2]. ფართო გამოკვლევების მიუხედავად, ემბოლიური ინსულტების მნიშვნელოვანი ნაწილი ვითარდება ემბოლიის მკაფიოდ იდენტიფიცირებადი წყაროს გარეშე; მათ კრიპტოგენურ ინსულტებს უწოდებენ [1, 5].
ცერებრული ემბოლიის ხშირი ეტიოლოგიები (მიზეზები) შეიძლება ფართოდ დავყოთ კატეგორიებად [1, 2, 3, 4]:
- კარდიოემბოლიური წყაროები (გულიდან წარმოშობილი ემბოლები):
- წინაგულთა ფიბრილაცია (AFib) და გულის სხვა არითმიები (ხშირად ასოცირებულია ისეთ ფონურ მდგომარეობებთან, როგორიცაა რევმატიული გულის დაავადება, ათეროსკლეროზი, ჰიპერტენზია ან გულის თანდაყოლილი მანკები). AFib არის ძირითადი მიზეზი.
- მიოკარდიუმის ინფარქტი, რომელიც იწვევს პარიეტალური თრომბის (გულის კედელზე მიმაგრებული კოლტის) ფორმირებას.
- მწვავე და ქვემწვავე ბაქტერიული ენდოკარდიტი (გულის სარქველების ინფექცია, რაც იწვევს სეპტიურ ემბოლიებს).
- გულის სარქვლოვანი დაავადება მნიშვნელოვანი არითმიების ან აშკარა პარიეტალური თრომბის გარეშეც (მაგ., მძიმე მიტრალური სტენოზი, მექანიკური პროთეზული სარქველები).
- გულის ქირურგიის გართულებები.
- გულის პროთეზული სარქველები (მექანიკურ სარქველებს აქვთ უფრო მაღალი თრომბოზული რისკი, ვიდრე ბიოპროთეზულ სარქველებს).
- არაბაქტერიული თრომბოზული ენდოკარდიტი (NBTE ან მარანტული ენდოკარდიტი - სტერილური ვეგეტაციები სარქველებზე, ხშირად ასოცირებული ავთვისებიან სიმსივნესთან ან ქრონიკულ ანთებასთან).
- პარადოქსული ემბოლია ინტრაკარდიული შუნტების მეშვეობით (როგორიცაა ღია ოვალური ხვრელი - PFO, ან წინაგულთაშუა ძგიდის დეფექტი - ASD), რაც საშუალებას აძლევს ვენურ კოლტებს მიაღწიოს არტერიულ სისხლის მიმოქცევას.
- ნაკლებად ხშირი გულისმიერი წყაროები, როგორიცაა წინაგულის მიქსომა (გულის სიმსივნე) ან კარდიომიოპათიები.
- არაკარდიოემბოლიური წყაროები:
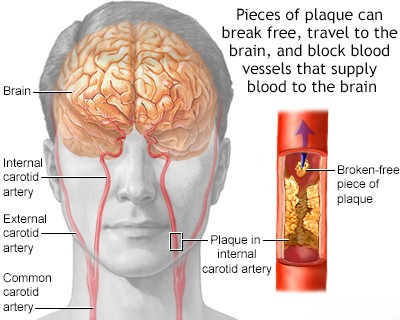
- აორტის (განსაკუთრებით აორტის რკალის) ან საძილე არტერიების ათეროსკლეროზი (რაც იწვევს პარიეტალური თრომბის ფორმირებას ან ათერომატოზული დეტრიტის გამოთავისუფლებას - ათეროემბოლიზმი). ამას ხშირად უწოდებენ არტერიო-არტერიულ ემბოლიას.
- მიუხედავად იმისა, რომ ნაკლებად ხშირია, როგორც *პირველადი* ემბოლიური წყარო, ცერებრული არტერიების (მაგ., ვერტებრალური, შუა ცერებრული) *in situ* თრომბოზი (კოლტის წარმოქმნა უშუალოდ შიგნით) შეიძლება მოხდეს, თუმცა ეს ტექნიკურად თრომბოზია და არა ემბოლია, სანამ ნაწილი არ მოწყდება.
- ფილტვის ვენის თრომბოზი (იშვიათი).
- ცხიმოვანი ემბოლიის სინდრომი (ჩვეულებრივ ტრავმის შემდეგ).
- სიმსივნური ემბოლია (ფრაგმენტები პირველადი ან მეტასტაზური სიმსივნეებიდან).
- ჰაეროვანი ემბოლია (მაგ., გარკვეული სამედიცინო პროცედურების, ყვინთვის ინციდენტების დროს).
- კისრისა და გულმკერდის ოპერაციების ან ტრავმის გართულებები, რომლებიც მოიცავს მაგისტრალურ სისხლძარღვებს.
- სეპტიური ემბოლები არაგულისმიერი ინფექციის წყაროებიდან (იშვიათი).
- კრიპტოგენური წყაროები (წყარო რჩება დაუდგენელი სტანდარტული გამოკვლევის შემდეგ) [5].
კრიპტოგენური ცერებრული ემბოლიები (ან კრიპტოგენური ინსულტები, ბევრი სავარაუდოდ ემბოლიური) წარმოადგენს მნიშვნელოვან სადიაგნოსტიკო გამოწვევას [5]. პაციენტებს შეიძლება ჰქონდეთ ფარული ჰიპერკოაგულაციური მდგომარეობები (პირობები, რომლებიც ზრდის თრომბის ფორმირების რისკს, მაგ., დაკავშირებული გარკვეულ მედიკამენტებთან, როგორიცაა ორალური კონტრაცეპტივები, ფონურ ქრონიკულ ანთებით დაავადებებთან, მემკვიდრეობით თრომბოფილიებთან ან მეტასტაზურ ავთვისებიან სიმსივნესთან), რაც წინასწარ განაწყობს მათ უეცარი ემბოლიური მოვლენებისკენ [1]. გარდა ამისა, გარდამავალი გულისმიერი მოვლენები, რომლებმაც შეიძლება წარმოშვას ემბოლები, როგორიცაა პაროქსიზმული წინაგულთა ფიბრილაციის ხანმოკლე ეპიზოდები ან სარქვლის გარდამავალი პათოლოგიები (როგორიცაა მიტრალური სტენოზის წკაპუნი, თუმცა თავად წკაპუნები არ არის ემბოლიური), შეიძლება გამოგვრჩეს რუტინული გამოკვლევის ან სტანდარტული ხანმოკლე გულის მონიტორინგის დროს [1, 5]. შედეგად, პაციენტების მნიშვნელოვანი რაოდენობა, განსაკუთრებით ახალგაზრდები (მაგ., 20-50 წლის ასაკში), განიცდის ემბოლიური ტიპის ინსულტებს საწყისი კვლევის შედეგად გამოვლენილი აშკარა მიზეზის გარეშე [1, 5].
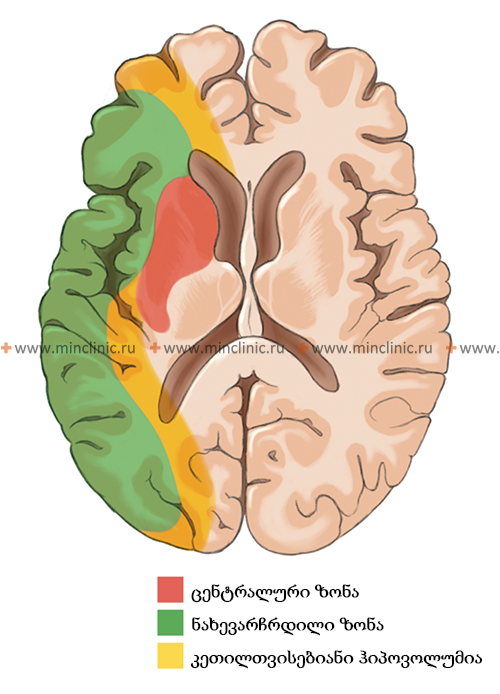
კლინიკური გამოსავალი დიდად არის დამოკიდებული თავად ემბოლზე და პაციენტის სისხლძარღვოვან ანატომიაზე [1]. ემბოლის ზომა, ლოკაცია და შემადგენლობა (მაგ., კოლტი, ცხიმი, სიმსივნე) განსაზღვრავს, რომელი ცერებრული არტერია დაიხშობა და, შესაბამისად, განვითარებული ცერებრული ინფარქტის (ინსულტის) მასშტაბსა და ლოკაციას [1, 2]. დიდი ემბოლები (მაგ., 2-3 მმ ან მეტი) უფრო მეტად ახშობენ დიდ სისხლძარღვებს, როგორიცაა ტვინის შუა არტერიის (MCA) ღერო, რაც პოტენციურად იწვევს ვრცელ ინფარქტს, რომელიც მოიცავს თავის ტვინის ქერქს, ქვემდებარე თეთრ ნივთიერებას და რუხი ნივთიერების ღრმა სტრუქტურებს (ბაზალური განგლიები, თალამუსი) [1, 2]. უფრო მცირე ემბოლები შეიძლება გადაადგილდეს უფრო შორს დისტალურად, დაახშოს MCA-ის ან ბაზილარული არტერიის მცირე პერფორანტული ტოტები, რაც ხშირად იწვევს უფრო მცირე, ღრმა ინფარქტებს, რომლებიც ცნობილია როგორც ლაკუნური ინფარქტები (თუმცა ლაკუნური ინსულტები უფრო კლასიკურად ასოცირდება მცირე სისხლძარღვთა დაავადებასთან/ლიპოჰიალინოზთან, ვიდრე ემბოლიასთან) [1, 6].
ემბოლები, განსაკუთრებით ისინი, რომლებიც შედგება თრომბოციტებისა და ფიბრინისგან (სისხლის კოლტები), ყოველთვის არ არიან სტატიკური. მათ შეუძლიათ გადაადგილდნენ უფრო შორს, სისხლის ნაკადის მიმართულებით, განიცადონ სპონტანური თრომბოლიზი (დაიშალონ ორგანიზმის საკუთარი კოლტის დამშლელი მექანიზმებით) ან დაიშალონ ფრაგმენტებად სისხლის მიმოქცევაში [1]. ამ დინამიურმა პროცესმა შეიძლება გამოიწვიოს მერყევი ნევროლოგიური სიმპტომები ან, ზოგიერთ იღბლიან შემთხვევაში, ადრეული რეპერფუზია და იშემიით გამოწვეული დეფიციტისგან სრული გამოჯანმრთელება [1]. ცერებრული ინფარქტის საბოლოო ლოკაცია და ზომა ასევე კრიტიკულად არის დამოკიდებული პაციენტის ინდივიდუალურ შესაძლებლობაზე კოლატერალური სისხლის ნაკადის მხრივ - დაუზიანებელი არტერიების უნარზე, მიაწოდონ სისხლი იშემიურ აუზს ალტერნატიული გზებით (როგორიცაა ვილიზის წრე ან ლეპტომენინგეალური ანასტომოზები)[1, 7].
მაგალითად, ადეკვატურმა კოლატერალურმა სისხლის ნაკადმა ვილიზის წრის გავლით ან ხერხემლის არტერიებიდან შეიძლება თავიდან აიცილოს ან მინიმუმამდე დაიყვანოს იშემია ან ინფარქტი მაშინაც კი, როდესაც ემბოლი ახშობს ისეთ მსხვილ პროქსიმალურ სისხლძარღვს, როგორიცაა შიდა საძილე არტერია, ტვინის წინა არტერიის A1 სეგმენტი ან პროქსიმალური ხერხემლის არტერია [7]. ანალოგიურად, ემბოლებმა, რომლებიც იჭედებიან კორტიკალურ ტოტებში ან თუნდაც ტვინის შუა არტერიის ღეროში, შეიძლება გამოიწვიოს შედარებით შეზღუდული კორტიკალური ან სუბკორტიკალური ინფარქტები, თუ არსებობს ძლიერი კოლატერალური ნაკადი ტვინის წინა ან უკანა არტერიების მიმდებარე აუზებიდან ტვინის ზედაპირზე არსებული ლეპტომენინგეალური კავშირების მეშვეობით [7]. კოლატერალური მიწოდების ეს პრინციპები ასევე ძალზე აქტუალურია უკანა ცირკულაციის ემბოლიის შედეგების განსაზღვრაში, რაც გავლენას ახდენს ტვინის ღეროსა და ნათხემზე [1, 7].
როდესაც ემბოლები ახშობენ სისხლძარღვებს, შემდგომმა რეპერფუზიამ (სისხლის ნაკადის აღდგენამ, სპონტანურად ან მკურნალობის გზით) დაზიანებულ, იშემიურ ტვინის ქსოვილში შეიძლება ზოგჯერ გამოიწვიოს მეორადი სისხლდენა [1, 8]. ეს ხშირად ვლინდება თავდაპირველად პეტექიური სისხლჩაქცევების (მცირე, წერტილოვანი სისხლდენების) სახით ინფარქტის ზონაში, რასაც ჰემორაგიული ტრანსფორმაცია ან ჰემორაგიული ინფარქტი ეწოდება [8]. უფრო იშვიათად, ეს მცირე სისხლჩაქცევები შეიძლება შეერთდეს და გაფართოვდეს, შექმნას უფრო დიდი, მოცულობითი ჰემორაგიული მასა [1, 8]. მნიშვნელოვანი ჰემორაგიული ტრანსფორმაცია უფრო სავარაუდოდ ითვლება მსხვილი სისხლძარღვების, მაგალითად, MCA-ის ღეროს ოკლუზიის შემდეგ, რაც იწვევს ვრცელ ინფარქტს (განსაკუთრებით მოიცავს რუხი და თეთრი ნივთიერების ღრმა სტრუქტურებს), განსაკუთრებით თუ რეპერფუზია ხდება დაგვიანებით [1, 8].
როდესაც გული ცალსახად იდენტიფიცირებულია, როგორც ემბოლიური წყარო, კვლევები მიუთითებენ თავის ტვინში განაწილების გარკვეულ პატერნზე. გულისმიერი ემბოლების დაახლოებით 80% მიდრეკილია გაიჭედოს ტვინის შუა არტერიის აუზში (რადგან ის იღებს საძილე არტერიის სისხლის ნაკადის ყველაზე დიდ ნაწილს), დაახლოებით 10-11% შეიძლება გადაადგილდეს ტვინის უკანა არტერიის აუზში (უკანა ცირკულაციის მეშვეობით), ხოლო დანარჩენი ნაწილდება ტვინის წინა არტერიის აუზში ან უშუალოდ ხერხემლის ან ბაზილარულ არტერიებში ან მათ ტოტებში [1, 2].
გულის პათოლოგიებით გამოწვეული ცერებრული ემბოლია ხშირად შემდგომში კლასიფიცირდება ძირითადი გულის პრობლემის მიხედვით, ტიპურად განასხვავებენ [1, 3]:
- არითმიულ მიზეზებს (მაგ., წინაგულთა ფიბრილაცია)
- გულის სტრუქტურული დაავადების მიზეზებს (მაგ., სარქვლოვანი დაავადება, მიოკარდიუმის ინფარქტი თრომბით, PFO)
| ემბოლუსის წყარო | ჩვეულებრივი მდგომარეობა | ტიპური სინდრომი |
|---|---|---|
| გულის | წინაგულების ფიბრილაცია | MCA ტერიტორია: ჰემიპარეზი, აფაზია/ნეგლექტი |
| არტერია-არტერიული | კაროტიდული ბალახი | ამაუროზის ფუგაქსი + MCA/ACA ინსულტი |
| პარადოქსული | PFO + DVT | ახალგაზრდა პაციენტი, კრიპტოგენური ინსულტი |
წინაგულთა ფიბრილაცია (AFib), როგორც კარდიოემბოლიური ინსულტის ძირითადი მიზეზი
სხვადასხვა ტიპის გულის არითმიები (გულის არარეგულარული რიტმი) შეიძლება ასოცირებული იყოს სიმპტომურ ცერებრულ ემბოლიასთან (ინსულტი ან TIA) და სისტემურ ემბოლიასთან (სხეულის სხვა ნაწილებში გადაადგილებული ემბოლები)[1, 3]. განსაკუთრებული ყურადღება უნდა მიექცეს ემბოლიის მნიშვნელოვნად მაღალ სიხშირეს ისეთი მდგომარეობების მქონე პაციენტებში, როგორიცაა სინუსური კვანძის სისუსტის სინდრომი (გულის ბუნებრივი რიტმის წამყვანის დარღვევა), წინაგულთა თრთოლვა და, განსაკუთრებით, წინაგულთა ფიბრილაცია (AFib) [3, 9]. AFib-თან ასოცირებული რისკი კიდევ უფრო იზრდება, როდესაც ის ვლინდება რევმატიული სარქვლოვანი დაავადების ფონზე (სარქვლოვანი AFib) [9]. ამ მაღალი რისკის გამო, ხანგრძლივი ანტიკოაგულაციური თერაპია, ტრადიციულად ვარფარინით ან ახლა უფრო ხშირად პირდაპირი ორალური ანტიკოაგულანტებით (DOACs), ძირითადად ნაჩვენებია მარცხენა წინაგულში თრომბის ფორმირების და შემდგომი ემბოლიის თავიდან ასაცილებლად AFib-ის მქონე შესაბამის პაციენტებში[9, 10]. კლინიკურად აშკარა ემბოლიური მოვლენები ყველაზე ხშირად აღინიშნება AFib-ის მქონე პაციენტებში, მიუხედავად მისი გამომწვევი მიზეზისა (სარქვლოვანი თუ არასარქვლოვანი) [3]. არანამკურნალები არასარქვლოვანი წინაგულთა ფიბრილაციის მქონე პაციენტებში ცერებრული ემბოლიის (ინსულტის) სავარაუდო წლიური სიხშირე მნიშვნელოვანია, ხშირად მოიხსენიება როგორც 4-7% ან უფრო მაღალი სხვა რისკ-ფაქტორების მიხედვით (როგორიცაა CHA₂DS₂-VASc სკალაში შემავალი ფაქტორები), და ერთმა ინსულტმაც კი შეიძლება გამოიწვიოს მნიშვნელოვანი გრძელვადიანი ინვალიდობა [9].
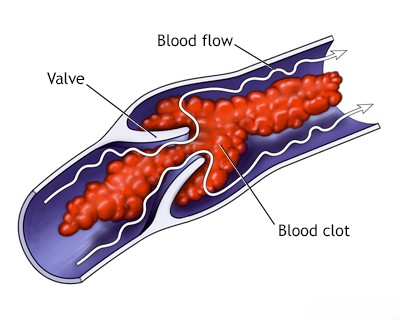
კიდევ ერთი მნიშვნელოვანი გულისმიერი ემბოლიის წყაროა პარიეტალური თრომბის (გულის საკნის შიდა კედელზე მიმაგრებული სისხლის კოლტის) ფორმირება. ეს შედარებით ხშირია ათეროსკლეროზული კარდიოვასკულური დაავადების მქონე პაციენტებში, განსაკუთრებით მიოკარდიუმის ინფარქტის შემდეგ, რომელიც აზიანებს გულის კედელს, ქმნის ზედაპირს, სადაც შეიძლება წარმოიქმნას კოლტები[1, 3]. რისკი არსებობს მიუხედავად ისეთი ასოცირებული გართულებების არსებობისა, როგორიცაა დვრილოვანი კუნთის დისფუნქცია, გულის შეგუბებითი უკმარისობა ან პარკუჭის ანევრიზმის (გამობერილობა გულის დასუსტებულ კედელზე) ფორმირება [1, 3].
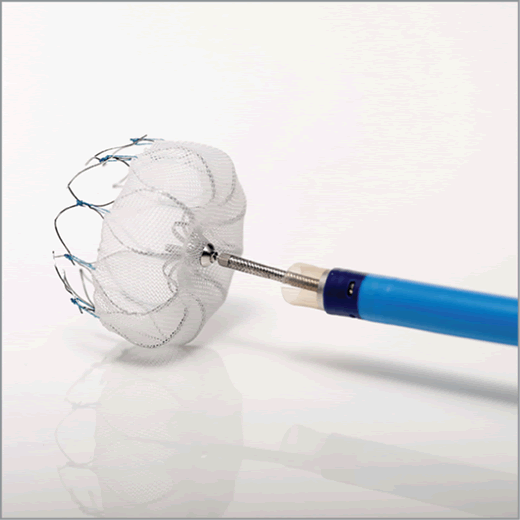
იმ პაციენტებისთვის არასარქვლოვანი წინაგულთა ფიბრილაციით, რომლებიც ითვლებიან ინსულტის მაღალი რისკის მქონედ, მაგრამ აქვთ უკუჩვენებები ხანგრძლივ ანტიკოაგულაციაზე (ან აქვთ ძლიერი უპირატესობა ალტერნატივის მიმართ), მარცხენა წინაგულის ყურის (LAA) დახურვის მოწყობილობები გვთავაზობენ მექანიკურ ალტერნატივას[10, 11]. LAA არის პატარა პარკი მარცხენა წინაგულში, სადაც AFib-ის მქონე პაციენტებში წარმოიქმნება ინსულტის გამომწვევი კოლტების უმეტესობა [11]. კათეტერიზაციის გზით იმპლანტირებული მოწყობილობები ეფექტურად ბეჭდავენ LAA-ს, ხელს უშლიან კოლტის მიგრაციას სისხლის მიმოქცევაში და ამით ამცირებენ იშემიური ინსულტის რისკს [11].
გულის ქირურგია, სხვა სისტემური მიზეზები და პარადოქსული ემბოლია
ზოგიერთი სამედიცინო პროცედურა ატარებს ემბოლიის რისკს [1]. გულის სარქვლის ჩანაცვლების ოპერაცია, განსაკუთრებით მექანიკური სარქველებით, ასოცირდება თრომბოემბოლიის შედარებით მაღალ რისკთან, თუ ანტიკოაგულაცია არაადეკვატურია [1, 3]. ცერებრული ემბოლიის ნაკლებად ხშირი პროცედურული მიზეზებია მანიპულაციები გულმკერდის ოპერაციის დროს (რამაც პოტენციურად შეიძლება გამოიწვიოს ფილტვის ვენური ემბოლია, თუმცა იშვიათია) და ჩარევები, რომლებიც მოიცავს თავს, კისერს, აორტას ან საძილე არტერიებს (რამაც შეიძლება მოწყვიტოს ათერომატოზული ნარჩენები ან თრომბი, რაც გამოიწვევს არტერიო-არტერიულ ემბოლიებს) [1]. ცხიმოვანი ემბოლია (ცხიმის გლობულების მოხვედრა სისხლის მიმოქცევაში) ან ჰაეროვანი ემბოლია შეიძლება წარმოიშვას ტრავმის შედეგად, როგორიცაა ლულოვანი ძვლების მოტეხილობები, რბილი ქსოვილების ვრცელი დაზიანება, გარკვეული ქირურგიული პროცედურები (განსაკუთრებით ორთოპედიული ან გულის), და იშვიათად სადიაგნოსტიკო ანგიოგრაფიის ან სხვა პროცედურების დროს, რომლებიც მოიცავს ინტრავასკულარული კონტრასტის შეყვანას ან კათეტერიზაციას [1]. ამ მდგომარეობებმა (ცხიმოვანი/ჰაეროვანი ემბოლია) შეიძლება პოტენციურად გამოიწვიოს მრავლობითი, მცირე ემბოლიური მოვლენები, ზოგჯერ ასოცირებული პეტექიურ სისხლჩაქცევებთან თავის ტვინში [1]. ხელოვნური გულის ან პარკუჭების დამხმარე მოწყობილობების (VAD) გამოყენება ასევე ატარებს მოწყობილობის ზედაპირებიდან ან მასთან დაკავშირებული თრომბის ფორმირებიდან წარმოშობილი ცერებრული ემბოლიის მნიშვნელოვან რისკს [3].
გულის თანდაყოლილი მანკები, რომლებიც ქმნიან კომუნიკაციას გულის მარჯვენა და მარცხენა მხარეებს შორის (მაგ., ღია ოვალური ხვრელი - PFO, წინაგულთაშუა ძგიდის დეფექტი - ASD, პარკუჭთაშუა ძგიდის დეფექტი - VSD), საშუალებას აძლევს ვენურ თრომბოემბოლს (კოლტს, რომელიც ტიპურად წარმოიქმნება ფეხის ვენებში, DVT) გვერდი აუაროს ფილტვის ცირკულაციას და შევიდეს სისტემურ არტერიულ მიმოქცევაში, რაც იწვევს პარადოქსულ ემბოლიას თავის ტვინში ან სხვა ორგანოებში[1, 3, 12]. სიმსივნური ემბოლები (გულის სიმსივნეების ფრაგმენტები, როგორიცაა წინაგულის მიქსომა, ან უფრო იშვიათად მეტასტაზური სიმსივნეები) შეიძლება მოხდეს[1]. გარდა ამისა, თრომბოზული, ინფექციური (სეპტიური) ან სტერილური (მარანტული/NBTE) ვეგეტაციები შეიძლება ჩამოყალიბდეს გულის საკნების ენდოკარდიულ ზედაპირებზე (შიდა ამომფენზე) ან, უფრო ხშირად, გულის სარქველებზე და შემდგომ განიცადოს ემბოლიზაცია [1, 3]. რევმატიული გულის დაავადების ან არაბაქტერიული თრომბოზული (მარანტული) ენდოკარდიტის დროს დაფიქსირებული სარქვლოვანი დაზიანებები ტიპურად აზიანებს აორტის და მიტრალურ სარქველებს და შეიძლება ასოცირებული იყოს სისტემურ ან ცერებრულ ემბოლიასთან; დიაგნოზი ეყრდნობა პაციენტის ანამნეზის, ფიზიკური გამოკვლევის მიგნებების (მაგ., შუილი), ვიზუალიზაციის (ექოკარდიოგრაფია) და შესაბამისი ლაბორატორიული შედეგების ინტეგრაციას [1, 3]. ლიბმან-საქსის ენდოკარდიტი, რომელიც ხასიათდება სტერილური სარქვლოვანი ვეგეტაციებით განსაკუთრებით მიტრალურ და აორტის სარქველებზე, არის სისტემური წითელი მგლურას (SLE) ცნობილი გამოვლინება და შეიძლება იყოს ცერებრული ემბოლიების წყარო [1, 3]. ანალოგიურად, ბაქტერიული ენდოკარდიტი (გულის სარქველების ინფექცია) არის კრიტიკული მოსაზრება [1, 3, 13].
ინფექციურმა (ბაქტერიულმა) ენდოკარდიტმა შეიძლება გამოიწვიოს თრომბოზული, ინფიცირებული ვეგეტაციების ფორმირება, რომლებიც გამოყოფენ სეპტიურ ემბოლებს [1, 13]. ამ სეპტიურმა ემბოლებმა შეიძლება გამოიწვიოს დიდი ცერებრული ინფარქტები, რომლებიც ვიზუალიზაციაზე ხშირად მსგავსია მაგისტრალური ცერებრული არტერიის ოკლუზიის შედეგად მიღებული არაგართულებული (არაინფექციური) ემბოლიური ინფარქტების [13]. თუმცა, სეპტიურმა ემბოლებმა ასევე შეიძლება გამოიწვიოს თავის ტვინის აბსცესების ან მრავლობითი მცირე მიკროაბსცესების ფორმირება [13]. სერიოზული გართულებაა მიკოზური ანევრიზმების განვითარება (ცერებრული არტერიის კედლის შესუსტება და გამობერვა სეპტიური ემბოლის მიერ იქ ჩატანილი ინფექციის გამო), რომლებიც ატარებენ გასკდომის მაღალ რისკს, რაც იწვევს სუბარაქნოიდულ და/ან ინტრაცერებრულ სისხლჩაქცევას [1, 13]. ამ მძიმე პოტენციური შედეგების გამო, ინფექციური ენდოკარდიტი ყოველთვის უნდა იყოს განხილული და გულდასმით გამორიცხული პაციენტებში, რომლებსაც აღენიშნებათ ინსულტის სიმპტომები, განსაკუთრებით თუ სახეზეა ცხელება ან ინფექციის სხვა ნიშნები [13].
გულის პირველადი სიმსივნეები, როგორიცაა წინაგულის მიქსომები, თუმცა იშვიათია, შეიძლება დაიშალოს და გამოიწვიოს სიმსივნური ემბოლია; ეს ემბოლები წარმოიშობა თავად სიმსივნის ზედაპირზე არსებული ნალექებიდან [1, 3]. დიფერენციალურ დიაგნოზში მიქსომაზე მიმანიშნებელი კვალი შეიძლება მოიცავდეს ფილტვის ჰიპერტენზიის ნიშნებს, ერითროციტების დალექვის სიჩქარის (ედს) მატებას და სისტემურ კონსტიტუციურ სიმპტომებს, როგორიცაა ცხელება ან სისუსტე [1]. მიტრალური სარქვლის პროლაფსი (MVP), გავრცელებული მდგომარეობა, როდესაც მიტრალური სარქვლის კარედები სისტოლის დროს მარცხენა წინაგულში იზნიქება, ზოგიერთ კვლევაში ასოცირებულია ცერებრულ ემბოლიასთან, თუმცა ზუსტი მექანიზმები (მაგ., ასოცირებული წინაგულთა ფიბრილაცია, თრომბის ფორმირება სარქველზე, ენდოთელური დისფუნქცია) ყოველთვის ბოლომდე გასაგები არ არის, რაც ართულებს ემბოლიის განმეორებითი რისკის პროგნოზირებას[1, 3]. ექოკარდიოგრაფია აუცილებელია დიაგნოსტიკისა და რისკის სტრატიფიკაციისთვის პაციენტებში საეჭვო MVP-ით და ნევროლოგიური მოვლენებით [3].
ცერებრულ ემბოლიასთან ასოცირებული კლინიკური სინდრომები
ცერებრული ემბოლიით გამოწვეული მწვავე იშემიური ინსულტი, როგორც წესი, ვლინდება ნევროლოგიური დეფიციტების უეცარი, მკვეთრი დაწყებით, რომლებიც ხშირად მაქსიმალურია თავიდანვე [1, 2]. თუმცა, კლინიკური მიმდინარეობა შეიძლება განსხვავდებოდეს. ზოგჯერ საწყისი დეფიციტები შეიძლება იყოს არასრული და შემდეგ გაუარესდეს ("მერყევი" ან პროგრესირებადი დასაწყისი), ან ისინი შეიძლება მნიშვნელოვნად იცვლებოდეს დაწყების შემდეგ, რაც შესაძლოა ასახავდეს ემბოლის მიგრაციას ან ფრაგმენტაციას დროებითი რეპერფუზიით [1]. ემბოლიური წარმოშობის ტრანზიტორული იშემიური შეტევები (TIA) შეიძლება გამოვლინდეს ნევროლოგიური დისფუნქციის ხანმოკლე ეპიზოდების სახით (გრძელდება წუთებიდან საათებამდე), რომლებიც სრულად ქრება, ზოგჯერ მეორდება დიდ ინსულტამდე [1].
სხვა სცენარებში, პაციენტს შეიძლება თავდაპირველად აღენიშნებოდეს მსუბუქი დეფიციტი, რომელიც შემდეგ საათების განმავლობაში პროგრესირებს უფრო ვრცელ ინფარქტამდე, რომელიც მოიცავს მაგისტრალური ცერებრული არტერიის აუზს, შესაძლოა საწყისი ემბოლიური ოკლუზიის დისტალურად თრომბის გავრცელების გამო[1]. დროითი პატერნის მიუხედავად, განვითარებული სპეციფიკური ნევროლოგიური დეფიციტი ასახავს დახშობილი არტერიით მომარაგებულ სისხლძარღვოვან აუზს, იქნება ეს დიდი სისხლძარღვი, პატარა ტოტი თუ წვრილი პერფორანტული არტერია [1, 2]. შედეგად მიღებული ნევროლოგიური სინდრომი შეესაბამება სისხლის ნაკადის ნაკლებობით დაზიანებული ტვინის ქსოვილის ლოკაციასა და მასშტაბს. როგორც ადრე აღვნიშნეთ, ემბოლის ზომა ზოგადად კარნახობს იმ სისხლძარღვის დიამეტრს, რომელსაც ის სავარაუდოდ დაახშობს [1].
ნევროლოგიური დეფიციტების გარკვეული პატერნები მკაცრად მიუთითებს ცერებრული არტერიის ემბოლიაზე, როგორც გამომწვევ მიზეზზე [1, 2]. ტვინის შუა არტერიის (MCA) აუზში ემბოლიასთან დაკავშირებული სინდრომები ხშირად მოიცავს:
- ფრონტალური ოპერკულარული სინდრომი: ხასიათდება კონტრალატერალური სახის სისუსტით (შუბლის დაზოგვით), ექსპრესიული ენის მძიმე სირთულით (აფაზია თუ დომინანტური ნახევარსფეროა, ან დისპროსოდია თუ არადომინანტურია) და ხშირად მძიმე დიზართრიით (გაურკვეველი მეტყველება), რაც ტიპურად გამოწვეულია MCA-ის ზედა დანაყოფის ტოტების ოკლუზიით.
- ბრაქიო-დომინანტური დამბლა: სისუსტე უპირატესად მოიცავს კონტრალატერალურ მკლავს (brachium), პოტენციურად მოიცავს მთელ მკლავს, წინამხარს, მაჯას ან მტევანს, ზოგჯერ ასოცირებული კორტიკალური სენსორული დეფიციტით (მაგ., დაქვეითებული სტერეოგნოზია, გრაფესთეზია), თუ პარიეტალური სენსორული ქერქი ჩართულია.
- იზოლირებული ვერნიკეს აფაზია (ენის გაგების დაქვეითება) ან ბროკას აფაზია (ენის წარმოქმნის დაქვეითება) პაციენტში დომინანტურ (ჩვეულებრივ მარცხენა) ნახევარსფეროში დაზიანებით, რაც ხშირად გამოწვეულია MCA-ის სპეციფიკური ქვედა (ვერნიკე) ან ზედა (ბროკა) დანაყოფის ტოტების ოკლუზიით.
- იზოლირებული კონტრალატერალური ჰემიანოფსია (მხედველობის ველის ნახევრის დაკარგვა) შეიძლება მოხდეს კეფის წილში მხედველობის რადიაციების ან პირველადი მხედველობის ქერქის დაზიანებით, რომლებიც ტიპურად მარაგდება ტვინის უკანა არტერიით (PCA), მაგრამ ზოგჯერ MCA-ის ტოტების ოკლუზიამ, რომელიც გავლენას ახდენს ტემპორალურ ან პარიეტალურ მხედველობის რადიაციებზე, შეიძლება გამოიწვიოს მხედველობის ველის დეფექტები.
სხვა მიმანიშნებელი სინდრომები მოიცავს: ჰემიანოფსიის უეცარი დაწყება, რაც პოტენციურად მიუთითებს ტვინის უკანა არტერიის (PCA) ემბოლიაზე; ფეხის მწვავე სისუსტე (კრურალური პარეზი), რომელიც არაპროპორციულად მოიცავს ფეხს უფრო მეტად, ვიდრე ხელს ან სახეს, რაც მიუთითებს ტვინის წინა არტერიის (ACA) ემბოლიაზე; და ვერტიგოს, სიარულის არასტაბილურობის, გულისრევის/ღებინების და კოორდინაციის დარღვევის (ატაქსიის) მწვავე დაწყება, რაც მიუთითებს უკანა ცირკულაციის ემბოლიაზე, რომელიც აზიანებს ნათხემს ან მის კავშირებს ტვინის ღეროსთან (ვერტებრალური ან ბაზილარული არტერიის ტოტები, როგორიცაა PICA, AICA)[1].
მცირე, ღრმა ინფარქტების (ლაკუნური ინსულტების) ზუსტი მიზეზის (ემბოლია, ათეროთრომბოზი ან მცირე სისხლძარღვთა დაავადება, როგორიცაა ლიპოჰიალინოზი) დადგენა მხოლოდ კლინიკურ სურათზე დაყრდნობით შეიძლება რთული იყოს, რადგან ლიპოჰიალინოზი სტატისტიკურად უფრო ხშირია ტიპური ლაკუნური სინდრომებისთვის [1, 6]. თუმცა, გარკვეული სპეციფიკური ლაკუნური-მსგავსი სინდრომები ძლიერ მიუთითებს ბაზილარული არტერიის მწვერვალზე ემბოლიაზე [1]. მაგალითად, ჰიპერსომნოლენციის (ჭარბი ძილიანობის), ზევით მზერის დარღვევის (ვერტიკალური მზერის პარეზი) და ორმხრივი პტოზის (დაშვებული ქუთუთოების) მწვავე დაწყება ძლიერ მიუთითებს ბაზილარული არტერიის მწვერვალზე გაჭედილ ემბოლზე, რაც პოტენციურად იწვევს ინფარქტს პერშერონის არტერიის (Artery of Percheron) ოკლუზიის გამო [1, 15]. პერშერონის არტერია არის PCA-დან მომდინარე ვარიანტული სისხლძარღვი, რომელიც უნიკალურად ამარაგებს ორივე თალამუსის მედიალურ ნაწილებს და ზოგჯერ სუბთალამუსს ორმხრივად[15].
გამოვლინებები შეიძლება ასევე იყოს არაფოკალური, განსაკუთრებით გარკვეული ტიპის ემბოლების დროს. ენდოკარდიტთან ასოცირებული სეპტიური ემბოლები ან გავრცელებული ცხიმოვანი ემბოლია ხშირად ვლინდება უფრო დიფუზური ნევროლოგიური სიმპტომებით, მათ შორის დეზორიენტაციით, კონფუზიით, აგიტაციით, დელირიუმით ან ცნობიერების დონის მერყეობით, ვიდრე მკაფიო ფოკალური დეფიციტით [1, 13].
გულის ქირურგიის შემდეგ დაფიქსირებული ნევროლოგიური სინდრომები შეიძლება მრავალფეროვანი იყოს. ხშირი გამოვლინებები მოიცავს ანესთეზიიდან დაგვიანებულ გამოღვიძებას, კოგნიტური პროცესების შენელებას (ბრადიფრენია), კონფუზიას, აგიტაციას, მეხსიერების დაქვეითებას და ზოგჯერ ვიზუალურ დარღვევებს ან ჰალუცინაციებს [1]. მიუხედავად იმისა, რომ ამ სიმპტომების უმეტესობა ქრება დღეებიდან ერთ კვირაში, მხედველობითი აღქმის მუდმივი დეფიციტი შეიძლება მიუთითებდეს პარიეტო-ოციპიტალურ ინფარქტზე, ხშირად MCA-ის აუზის წყალგამყოფ ზონებში, რაც პოტენციურად გამოწვეულია პერიოპერაციული ჰიპოტენზიით (დაბალი არტერიული წნევა) ან მრავლობითი მიკროემბოლიით (გულიდან, აორტიდან ან შუნტირების სისტემიდან) [1].
ინსულტის შემდეგ განვითარებული გულყრები სტატისტიკურად უფრო ხშირია ემბოლიური ინსულტების შემდეგ, ვიდრე თრომბოზულის, და ასევე შესაძლოა უფრო ხშირი იყოს ლაკუნური ინფარქტების დროს, რომლებიც აზიანებენ თეთრი ნივთიერების ღრმა გზებს, ვიდრე წმინდა რუხი ნივთიერების ლაკუნების დროს [1]. ნებისმიერი კორტიკალური სუპრატენტორიული ინფარქტი (რომელიც აზიანებს ტვინის ზედაპირს კარვის ზემოთ) ატარებს გულყრების გამოწვევის რისკს, მაგრამ მათი გამოვლენა არ არის სპეციფიკური (პათოგნომონური) ინსულტის რომელიმე კონკრეტული ეტიოლოგიისთვის [1]. აღსანიშნავია, რომ ახლადდაწყებული ეპილეფსია ხანდაზმულებში (კრიპტოგენური ეპილეფსია) ზოგჯერ შეიძლება გამოწვეული იყოს მანამდე ამოუცნობი ("ჩუმი") ქრონიკული კორტიკალური ინფარქტებით და ეს გულყრები ხშირად კარგად რეაგირებს სტანდარტულ ანტიკონვულსანტურ თერაპიაზე, როგორიცაა ფენიტოინი [1].
ცერებრული ემბოლია: კლინიკური გამოკვლევა და ლაბორატორიული/ვიზუალიზაციური კვლევები
გადამწყვეტია, სანამ დაიწყება ანტიკოაგულანტური თერაპია (სისხლის გამათხელებლები) პაციენტში, რომელსაც აქვს მწვავე ინსულტის სიმპტომები, რომლებიც მიუთითებს ცერებრულ ემბოლიაზე, აუცილებელია ჩატარდეს თავის ტვინის გადაუდებელი ვიზუალიზაცია, როგორც წესი, უკონტრასტო კომპიუტერული ტომოგრაფია (კტ)[16]. ამ საწყისი სკანირების მთავარი მიზანია ინტრაკრანიალური სისხლჩაქცევის (ჰემორაგიის) საიმედოდ გამორიცხვა, რადგან ანტიკოაგულანტები უკუნაჩვენებია ჰემორაგიული ინსულტის დროს და შეიძლება გააუარესოს სისხლდენა [16]. მიუხედავად იმისა, რომ კტ შესანიშნავია მწვავე სისხლის აღმოსაჩენად, მაგნიტურ-რეზონანსული ტომოგრაფია (მრტ) უფრო მგრძნობიარეა ადრეული იშემიური ცვლილებების აღმოსაჩენად და მწვავე და ქრონიკული სისხლჩაქცევების ან წინა ინფარქტების ერთმანეთისგან გასარჩევად [14, 16].
მწვავე ფოკალური ნევროლოგიური დეფიციტის დიფერენციალური დიაგნოზი (ინსულტის იმიტატორები) [1, 17]
| მდგომარეობა | ძირითადი მახასიათებლები / განმასხვავებელი ნიშნები | ტიპური გამოკვლევები / მიგნებები |
|---|---|---|
| იშემიური ინსულტი (ემბოლიური/თრომბოზული) | უეცრად დაწყებული ფოკალური ნევროლოგიური დეფიციტი, რომელიც შეესაბამება სისხლძარღვოვან აუზს. | თავის ტვინის უკონტრასტო კტ საწყის ეტაპზე უარყოფითია სისხლჩაქცევაზე. მრტ (DWI) დადებითია იშემიაზე ადრეულ ეტაპზე. კტა/მრა-მ შეიძლება აჩვენოს ოკლუზია/სტენოზი. რისკ-ფაქტორების/წყაროს იდენტიფიცირება. |
| ინტრაცერებრული სისხლჩაქცევა (ICH) | უეცრად დაწყებული ფოკალური ნევროლოგიური დეფიციტი, ხშირად თავის ტკივილით, ღებინებით, ცნობიერების დაქვეითებით, მძიმე ჰიპერტენზიით. | თავის ტვინის უკონტრასტო კტ აჩვენებს სისხლჩაქცევას. |
| გულყრა ტოდის პარალიჩით (Todd's Paralysis) | პოსტიქტალური (გულყრის შემდგომი) ფოკალური სისუსტე, რომელიც ინსულტის იმიტაციას ახდენს. ანამნეზში გულყრა. გაივლის საათებიდან 2 დღემდე პერიოდში. | ანამნეზი. ეგგ-მ შეიძლება აჩვენოს პათოლოგია. ვიზუალიზაცია ჩვეულებრივ ნორმალურია, თუ არ არის ძირითადი დაზიანება. ტრანზიტორული ხასიათი. |
| შაკიკი აურით (განსაკუთრებით ჰემიპლეგიური) | ტრანზიტორული ნევროლოგიური სიმპტომები (ხშირად თანდათანობით ვრცელდება), რომლებსაც მოსდევს/ახლავს თავის ტკივილი. მსგავსი ეპიზოდების ანამნეზი. სრული აღდგენა. | კლინიკური დიაგნოზი. ნორმალური გამოკვლევა შეტევებს შორის. ვიზუალიზაცია ჩვეულებრივ ნორმალურია. |
| ჰიპოგლიკემია | შეუძლია გამოიწვიოს ფოკალური ნევროლოგიური დეფიციტები, კონფუზია, გულყრები. მნიშვნელოვანია ანამნეზში დიაბეტი. | სისხლში გლუკოზის დაბალი დონე. სიმპტომები უმჯობესდება გლუკოზით. |
| თავის ტვინის სიმსივნე | შეიძლება გამოვლინდეს მწვავედ გულყრით ან სისხლჩაქცევით, რაც იწვევს ფოკალურ ნიშნებს, მაგრამ ხშირად წინ უძღვის პროგრესირებადი სიმპტომები. | მრტ კონტრასტით აჩვენებს მოცულობით წარმონაქმნს. |
| თავის ტვინის აბსცესი | ჩვეულებრივ ქვემწვავე დასაწყისი. ფოკალური ნიშნები, თავის ტკივილი, ცხელება, გულყრები. ინფექციის წყაროს ანამნეზი. | მრტ აჩვენებს რგოლისებრად კონტრასტირებად დაზიანებას, შეზღუდულ დიფუზიას. მომატებული ანთებითი მარკერები. |
| გაფანტული სკლეროზის რეციდივი | ფოკალური დეფიციტების მწვავე/ქვემწვავე დასაწყისი. შესაძლებელია წინა ეპიზოდების ანამნეზი. ჩვეულებრივ ახალგაზრდა მოზრდილებში. | მრტ აჩვენებს დემიელინიზებად დაზიანებებს. |
| სუბდურული ჰემატომა | კომპრესიის გამო შეუძლია გამოიწვიოს ფოკალური ნიშნები. თავის ტკივილი, შეცვლილი მენტალური სტატუსი. ტრავმის ანამნეზი (შეიძლება იყოს უმნიშვნელო/შორეული). | კტ/მრტ აჩვენებს სუბდურულ სითხის დაგროვებას. |
| მეტაბოლური ენცეფალოპათია | თავის ტვინის დიფუზური დისფუნქცია (კონფუზია, ლეთარგია). ფოკალური ნიშნები იშვიათია, თუ არ არის დამატებითი პრობლემა. იდენტიფიცირებადი სისტემური მიზეზი. | სპეციფიკური ლაბორატორიული დარღვევები. ვიზუალიზაცია ჩვეულებრივ არასპეციფიკურია. |
| ფუნქციური ნევროლოგიური აშლილობა | ნევროლოგიური სიმპტომები არ შეესაბამება ორგანულ პატერნებს. დადებითი კლინიკური ნიშნები (მაგ., ჰუვერის). | გამორიცხვის დიაგნოზი საფუძვლიანი გამოკვლევის შემდეგ. ნორმალური ვიზუალიზაცია/ლაბორატორიული მონაცემები. |
ლუმბალური პუნქცია (ზურგის ტვინის პუნქცია) ერითროციტებზე ცერებროსპინალური სითხის (ცსს) გამოსაკვლევად ზოგადად *არ არის* ნაჩვენები საეჭვო ემბოლიური ინსულტის რუტინულ შეფასებაში [1]. მისი სარგებლობა ძალიან შეზღუდულია და ძირითადად განიხილება მხოლოდ იშვიათ სიტუაციებში, როდესაც სუბარაქნოიდულ სისხლჩაქცევაზე ძლიერი ეჭვია, მაგრამ საწყისი კტ სკანირება უარყოფითი ან საეჭვოა, ან შესაძლოა ისტორიულად, როდესაც მოწინავე ვიზუალიზაცია მიუწვდომელი იყო და ტვინის ღეროს მცირე სისხლჩაქცევების (მაგ., ხიდის) დიფერენცირება ინფარქტებისგან რთული იყო [1]. ძვლის არტეფაქტებმა კტ სკანირებაზე, განსაკუთრებით უკანა ფოსოში (ტვინის ღერო და ნათხემი), შეიძლება ზოგჯერ დაფაროს მცირე სისხლჩაქცევები [14]. თანამედროვე მაგნიტურ-რეზონანსული ტომოგრაფია (მრტ), განსაკუთრებით სისხლის პროდუქტების მიმართ მგრძნობიარე რეჟიმები (როგორიცაა გრადიენტული ექო ან მგრძნობელობაზე შეწონილი ვიზუალიზაცია), ბევრად აღემატება მწვავე სისხლჩაქცევის გარჩევას ქრონიკულისგან და უაღრესად მგრძნობიარეა ადრეული იშემიური ცვლილებების (ინფარქტის) აღმოსაჩენად დაწყებიდან რამდენიმე საათში [14, 16].
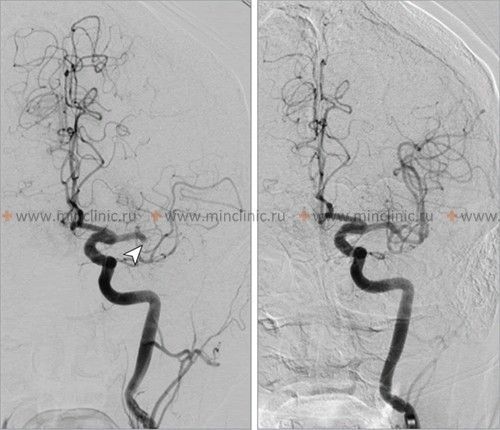
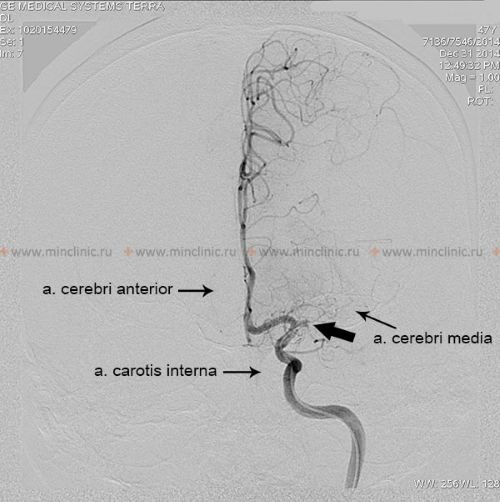
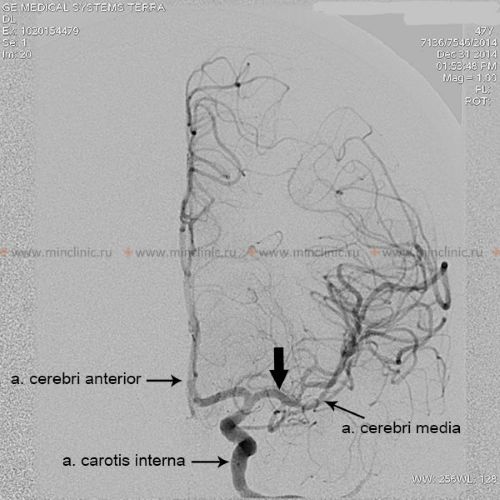
თუ ეჭვია ცერებრული არტერიის ემბოლიაზე, არტერიული ოკლუზიის ადგილმდებარეობის იდენტიფიცირება და ქვემოთმდებარე ტვინის ქსოვილის შეფასება კრიტიკულია მწვავე მკურნალობის (როგორიცაა თრომბექტომია) დასაგეგმად [16, 19]. არაინვაზიური სისხლძარღვოვანი ვიზუალიზაცია, როგორიცაა კტ ანგიოგრაფია (CTA) ან მრ ანგიოგრაფია (MRA), ჩვეულებრივ ტარდება გადაუდებლად [16]. კონვენციური კათეტერზე დაფუძნებული ცერებრული ანგიოგრაფია (ციფრული სუბტრაქციული ანგიოგრაფია - DSA) უზრუნველყოფს სისხლძარღვების უმაღლესი რეზოლუციის დეტალებს, მაგრამ არის ინვაზიური [14]. ის შეიძლება ჩატარდეს, თუ იგეგმება ენდოვასკულური მკურნალობა (თრომბექტომია) ან თუ არაინვაზიური ვიზუალიზაცია არასაკმარისად ინფორმატიულია [16, 19]. მნიშვნელოვანია აღინიშნოს, რომ რამდენიმე საათის ან დღის შემდეგ, ემბოლმა შეიძლება მიგრირება განიცადოს დისტალურად, ფრაგმენტაცია ან სპონტანური ლიზისი (დაშლა), რაც ნიშნავს, რომ მოგვიანებით ჩატარებულმა ანგიოგრაფიამ შეიძლება არ აჩვენოს თავდაპირველი ოკლუზია, რის გამოც ემბოლიური ინსულტის საბოლოო დიაგნოზი ზოგჯერ სავარაუდოა კლინიკური სურათისა და ინფარქტის პატერნის საფუძველზე [1]. სტანდარტული ინტრავენური კონტრასტის შეყვანა რუტინული კტ ან მრტ სკანირების დროს ზოგადად მოკლებულია იმ რეზოლუციას და დროით სიზუსტეს, რაც აუცილებელია სისხლძარღვებში მცირე ცერებრული ემბოლების უშუალო ვიზუალიზაციისთვის [14].
ცერებრული ემბოლიის მკურნალობა
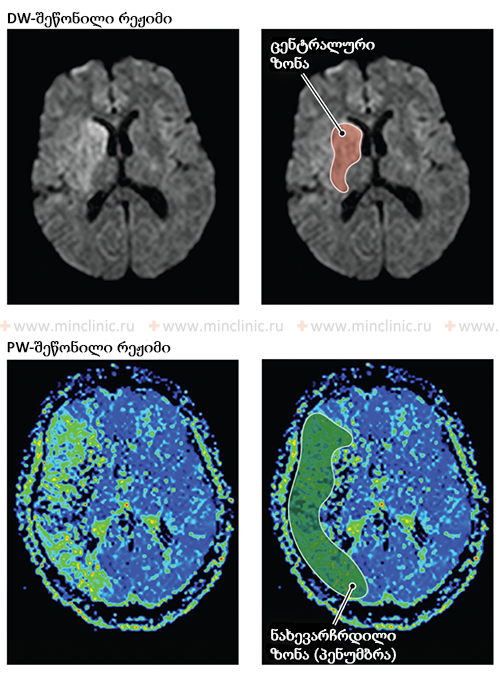
ცერებრული ემბოლიით გამოწვეული ინსულტის მკურნალობა მოიცავს მწვავე ფაზის მართვას თავის ტვინის დაზიანების მინიმუმამდე შესამცირებლად და მეორადი პრევენციის სტრატეგიების განხორციელებას სამომავლო ემბოლიური მოვლენების რისკის შესამცირებლად[1, 16]. მწვავე პერიოდში (პირველი საათებიდან დღეებამდე), ძირითადი აქცენტი ხშირად კეთდება ადეკვატური ცერებრული პერფუზიული წნევის შენარჩუნებაზე, რათა უზრუნველყოფილი იყოს სისხლის მიწოდება იშემიური პენუმბრასთვის (არე, რომელიც გარს აკრავს ინფარქტის ბირთვს, რომელიც რისკის ქვეშაა, მაგრამ პოტენციურად გადარჩენადია) [16]. მიმდინარე გაიდლაინები ზოგადად რეკომენდაციას უწევს პერმისიულ ჰიპერტენზიას (არტერიული წნევის გარკვეულწილად მომატების დაშვებას), თუ ის არ აღემატება ძალიან მაღალ ზღურბლებს (მაგ., >220/120 მმ.ვწყ.სვ, ან >185/110 მმ.ვწყ.სვ თუ თრომბოლიზი ტარდება) ან არ არსებობს სპეციფიკური უკუჩვენებები [16]. არტერიული წნევის აგრესიული დაქვეითება ზოგადად თავიდან უნდა იქნას აცილებული, თუ ეს არ არის აუცილებელი სპეციფიკური მდგომარეობებისთვის (მაგ., აორტის დისექცია, მწვავე გულის უკმარისობა) [16]. პირიქით, მნიშვნელოვანი ჰიპოტენზია (დაბალი არტერიული წნევა) უნდა განიკურნოს დაუყოვნებლივ, მაგრამ ფრთხილად, რადგან არტერიული წნევის ჭარბმა მატებამ შეიძლება გააუარესოს ტვინის შეშუპება ან გაზარდოს ჰემორაგიული ტრანსფორმაციის რისკი [1, 16]. თავის ტვინის შეშუპება (ედემა) ტიპურად ვითარდება 2-3 დღის განმავლობაში მნიშვნელოვანი ინფარქტის შემდეგ და შეიძლება მიაღწიოს პიკს მე-3-5 დღეს, პოტენციურად შენარჩუნდეს 10 დღემდე ან მეტხანს მძიმე შემთხვევებში [1].
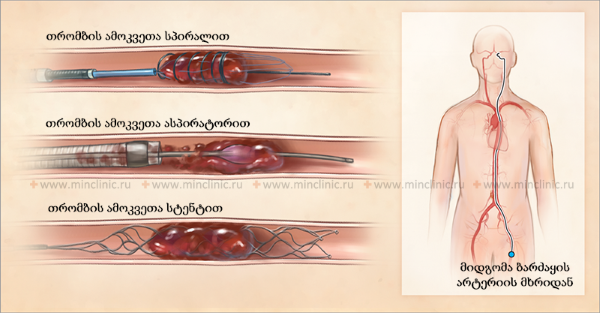
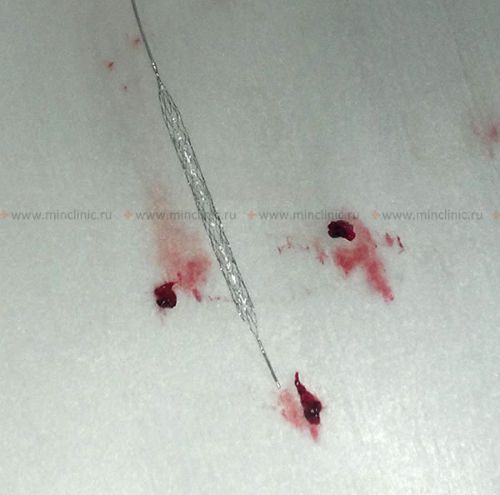
მიუხედავად იმისა, რომ რეპერფუზიული თერაპიები (როგორიცაა ინტრავენური თრომბოლიზი ან მექანიკური თრომბექტომია) მიზნად ისახავს სისხლის ნაკადის აღდგენას ემბოლის დაშლით ან ამოღებით[16, 19], არსებობს თეორიული შეშფოთება, რომ დაზიანებულ ქსოვილში რეპერფუზიამ შეიძლება გაზარდოს შეშუპება ან ჰემორაგიული ტრანსფორმაცია [1, 8]. თუმცა, დროული რეპერფუზიის სარგებელი პენუმბრას გადასარჩენად ზოგადად აღემატება ამ რისკებს შესაბამის პაციენტებში[16, 19]. ემბოლიური ინფარქტის დროს სიმპტომური ცერებრული შეშუპება მიდრეკილია მიჰყვეს ორ მთავარ პატერნს, რომლებსაც აქვთ მნიშვნელოვანი კლინიკური შედეგები [1]:
- სუპრატენტორიული შეშუპება: ემბოლიური ინფარქტების დროს, რომლებიც აზიანებს თავის ტვინის ნახევარსფეროებს (სუპრატენტორიული), ინფარქტის უფრო დიდი ზომა პირდაპირ კორელაციაშია ცერებრული შეშუპების გაზრდილ რისკთან და სიმძიმესთან. დიდი ემბოლების მიერ MCA-ის ღეროს ოკლუზია განსაკუთრებით მიდრეკილია გამოიწვიოს მნიშვნელოვანი შეშუპება ("ავთვისებიანი MCA სინდრომი"), რამაც შეიძლება გამოიწვიოს ქალასშიდა წნევის მომატება, შუა ხაზის ცდომა, ტვინის ჩაჭედვა (განსაკუთრებით საფეთქლის წილის ჩაჭედვა), კომა და სიკვდილი, თუ აგრესიულად არ იმართება. მცირე ტოტების დამაზიანებელი ემბოლები ტიპურად იწვევს ნაკლებ შეშუპებას.
- უკანა ფოსოს შეშუპება: შედარებით მცირე ნათხემის ინფარქტებმაც კი, განსაკუთრებით მათ, რომლებიც აზიანებენ ნათხემის ქვედა უკანა არტერიის (PICA) აუზს, შეიძლება გამოიწვიოს მნიშვნელოვანი შეშუპება უკანა ფოსოს შეზღუდულ სივრცეში. ამან შეიძლება სწრაფად გამოიწვიოს მეოთხე პარკუჭის კომპრესია (რაც იწვევს ობსტრუქციულ ჰიდროცეფალიას) და ტვინის ღეროს პირდაპირი კომპრესია, რაც პოტენციურად გამოიწვევს უეცარ ნევროლოგიურ გაუარესებას, კომას და სუნთქვის გაჩერებას. გადაუდებელი ნეიროქირურგიული კონსულტაცია შესაძლო ქირურგიული დეკომპრესიისთვის (მაგ., სუბოციპიტალური კრანიექტომია) შეიძლება აუცილებელი იყოს სიცოცხლისათვის საშიში უკანა ფოსოს შეშუპების შემთხვევებში.
ისეთ სიტუაციებში, როდესაც მნიშვნელოვანი ცერებრული შეშუპება იწვევს ქალასშიდა წნევის მომატებას, ნაჩვენებია მედიკამენტური მართვის სტრატეგიები, როგორიცაა თავის აწეულ მდგომარეობაში შენარჩუნება, ადეკვატური ოქსიგენაციისა და ვენტილაციის უზრუნველყოფა და ოსმოსური დიურეტიკების გამოყენება [1, 16]. ინტრავენური მანიტოლი ხშირად გამოიყენება ტვინის ქსოვილიდან სითხის გამოსადევნად პლაზმის ოსმოლარობის გაზრდით (სამიზნე ტიპურად 300-320 მოსმ/ლ), ჩვეულებრივ მიიღება წყვეტილი ბოლუსების სახით ყოველ რამდენიმე საათში ელექტროლიტებისა და თირკმლის ფუნქციის მონიტორინგის ფონზე [1].
ემბოლიური ინსულტის შემდეგ ანტიკოაგულანტური თერაპიის დაწყებისა და დროის შესახებ გადაწყვეტილება დიდად არის დამოკიდებული საეჭვო ან დადასტურებულ ემბოლიურ წყაროზე (მაგ., გულის თრომბი სხვების/უცნობის წინააღმდეგ) და პაციენტის ინდივიდუალურ რისკის პროფილზე[1, 10, 20]. ინფარქტის ზონაში ჰემორაგიული ტრანსფორმაციის გამოწვევის ან გაუარესების შესახებ შეშფოთებამ გამოიწვია განსხვავებული ისტორიული მოსაზრებები და პრაქტიკა[1, 20]. ზოგიერთი რეკომენდაციას უწევდა ანტიკოაგულაციის გადადებას რამდენიმე დღით ან კვირით, განსაკუთრებით დიდი ინფარქტების შემდეგ, მიუთითებდა რა ადრეული განმეორებითი ემბოლიის პოტენციურად დაბალ რისკზე ზოგიერთ სცენარში [1]. სხვები ამტკიცებენ, რომ კლინიკურად მნიშვნელოვანი ჰემორაგიული ტრანსფორმაცია შედარებით იშვიათია, ჩვეულებრივ გვხვდება ძირითადად ძალიან დიდი ინფარქტების დროს, რომლებიც მოიცავს ღრმა სტრუქტურებს (მაგ., ბაზალური განგლიების ჩართულობა MCA ღეროს ემბოლებით), და რომ ადრეული განმეორებითი ემბოლიის რისკი (განსაკუთრებით მაღალი რისკის გულისმიერი წყაროებიდან, როგორიცაა AFib ან პარიეტალური თრომბი) ხშირად აღემატება ანტიკოაგულაციასთან დაკავშირებულ სისხლდენის რისკს [1, 20]. მიმდინარე გაიდლაინები ზოგადად უპირატესობას ანიჭებს ანტიკოაგულაციის უფრო ადრეულ დაწყებას (ხშირად 4-14 დღის განმავლობაში, ინფარქტის ზომისა და სისხლდენის რისკის მიხედვით) მეორადი პრევენციისთვის კარდიოემბოლიური წყაროების მქონე პაციენტებში, როგორიცაა AFib, თუ არ არსებობს სპეციფიკური უკუჩვენებები ან ძალიან დიდი ინფარქტები[10, 20]. თუმცა, დაუყოვნებელი ანტიკოაგულაცია მკაცრად უკუნაჩვენებია ცნობილი ან საეჭვო სეპტიური ემბოლების პირობებში (მაგ., ენდოკარდიტიდან) ასოცირებული მიკოზური ანევრიზმებიდან სისხლჩაქცევის გამოწვევის მაღალი რისკის გამო[1, 13].
გამომწვევი წყარო კარნახობს გრძელვადიან მეორად პრევენციას[10, 20]. ყველაზე მნიშვნელოვანი კარდიოემბოლიური მოვლენები (შესაძლოა მარანტული, სეპტიური და სიმსივნური ემბოლების გამოკლებით) წარმოიქმნება გულში თრომბების ფორმირების შედეგად [3]. ეს შეიძლება იყოს მიკროთრომბები, რომლებიც წარმოიქმნება მარცხენა წინაგულის ყურში (განსაკუთრებით ხშირია წინაგულთა ფიბრილაციის დროს), უფრო დიდი პარიეტალური თრომბები, რომლებიც ვითარდება დაზიანებულ გულის კუნთზე მიოკარდიუმის ინფარქტის შემდეგ, ან თრომბოზული მასები, რომლებიც წარმოიქმნება პარკუჭის ანევრიზმების შიგნით ან დაავადებულ თუ პროთეზულ გულის სარქველებზე [3]. ასეთი თრომბების არსებობა ზოგადად მოითხოვს თერაპიულ ანტიკოაგულაციას, სანამ ძირითადი მდგომარეობა არ მოგვარდება ან განმეორებითი ემბოლიის რისკი არ ჩაითვლება საკმარისად დაბალად (ან განუსაზღვრელი ვადით, თუ ძირითადი მიზეზი შენარჩუნებულია) [3, 10, 20]. მაგალითად, ანტიკოაგულაცია ტიპურად რეკომენდებულია მინიმუმ 3-6 თვის განმავლობაში მწვავე მიოკარდიუმის ინფარქტის შემდეგ, თუ პარიეტალური თრომბი არსებობს, და ჩვეულებრივ განუსაზღვრელი ვადით პაციენტებისთვის პერსისტენტული ან პაროქსიზმული წინაგულთა ფიბრილაციით, რომლებიც აკმაყოფილებენ რისკის კრიტერიუმებს[3, 9, 10].
წინაგულთა ფიბრილაცია, რომელიც ვლინდება მნიშვნელოვანი რევმატიული სარქვლოვანი გულის დაავადების ფონზე (განსაკუთრებით მიტრალური სტენოზის), ხშირად მოითხოვს მთელი სიცოცხლის განმავლობაში ანტიკოაგულაციას, თუნდაც წინა დოკუმენტირებული ემბოლიური მოვლენის გარეშე, ინსულტის ძალიან მაღალი ასოცირებული რისკის გამო [9]. სხვა მიზეზებთან დაკავშირებული უსიმპტომო წინაგულთა ფიბრილაციის მართვა (როგორიცაა კორონარული არტერიის დაავადება ან ჰიპერტენზია) ხელმძღვანელობს ინსულტის რისკის სტრატიფიკაციის სკალებით (მაგ., CHA₂DS₂-VASc); პაციენტები, რომლებიც აღემატებიან გარკვეულ რისკის ზღურბლს, ზოგადად სარგებელს იღებენ ანტიკოაგულაციით [9, 10]. მიუხედავად იმისა, რომ ანტიკოაგულაცია აშკარად ამცირებს ინსულტის რისკს ამ პოპულაციებში მკურნალობის არარსებობასთან ან მხოლოდ ასპირინთან შედარებით [9], ანტიკოაგულაციის ოპტიმალური ხანგრძლივობა ზოგიერთ სპეციფიკურ სცენარში (მაგ., AFib აბლაციის წარმატების შემდეგ) რჩება მიმდინარე კვლევისა და დებატების საგნად [10].
იმ პაციენტებში, რომლებიც განიცდიან ცერებრულ ემბოლიას, სადაც წყარო რჩება დაუდგენელი (კრიპტოგენური) საფუძვლიანი გამოკვლევის მიუხედავად, გადაწყვეტილება გრძელვადიანი ანტიკოაგულაციის შესახებ რთულია [5, 20]. თუ საეჭვოა მაღალი რისკის წყარო, როგორიცაა პაროქსიზმული AFib ან PFO, მაგრამ არ არის ცალსახად დადასტურებული, შეიძლება განიხილებოდეს დაბალი დოზით ანტიკოაგულაცია (მაგ., ვარფარინით, რომელიც მიმართულია უფრო დაბალ INR-ზე, ან სულ უფრო ხშირად DOAC-ებით), განსაკუთრებით ახალგაზრდა პაციენტებში ან მორეციდივე მოვლენების მქონე პირებში, ყოველთვის პოტენციური სარგებლის აწონვით სისხლდენის რისკებთან და უკუჩვენებების გათვალისწინებით[5, 12, 20]. არ არსებობს საყოველთაოდ შეთანხმებული გაიდლაინები ანტიკოაგულაციის ოპტიმალური ხანგრძლივობის შესახებ ჭეშმარიტად კრიპტოგენური ემბოლიური ინსულტის დროს; თუმცა, ემპირიული მკურნალობა გარკვეული პერიოდის განმავლობაში (მაგ., 6 თვიდან 1 წლამდე), განსაკუთრებით 50 წლამდე ასაკის პაციენტებში, შეიძლება გონივრულად ჩაითვალოს ზოგიერთი კლინიცისტის მიერ, რასაც მოჰყვება გადაფასება [1, 5].
ლიტერატურა
- Ropper AH, Samuels MA, Klein JP, Prasad S. Adams and Victor's Principles of Neurology. 11th ed. McGraw Hill; 2019. თავი 34: ცერებროვასკულური დაავადებები (განყოფილება ემბოლიური ინფარქტის შესახებ).
- Grotta JC, Albers GW, Broderick JP, et al. Stroke: Pathophysiology, Diagnosis, and Management. 7th ed. Elsevier; 2021. თავი იშემიური ინსულტის მექანიზმების შესახებ.
- Hart RG, Halperin JL, Pearce LA, et al. Cardioembolic stroke. Lancet Neurol. 2017 Jun;16(6):489-500.
- Caplan LR. Caplan's Stroke: A Clinical Approach. 5th ed. Cambridge University Press; 2016. თავი მსხვილი არტერიების ათეროსკლეროზის შესახებ (არტერიო-არტერიული ემბოლიისთვის).
- Hart RG, Catanese L, Perera KS, Ntaios G, Connolly SJ. Embolic strokes of undetermined source: the case for a new clinical construct. Lancet Neurol. 2017 May;16(5):401-411.
- Caplan LR. Caplan's Stroke: A Clinical Approach. 5th ed. Cambridge University Press; 2016. თავი ლაკუნური და მცირე სისხლძარღვოვანი დაავადების ინსულტების შესახებ.
- Ropper AH, Samuels MA, Klein JP, Prasad S. Adams and Victor's Principles of Neurology. 11th ed. McGraw Hill; 2019. თავი 34: ცერებროვასკულური დაავადებები, განყოფილებები კოლატერალური ცირკულაციის შესახებ.
- Grotta JC, Albers GW, Broderick JP, et al. Stroke: Pathophysiology, Diagnosis, and Management. 7th ed. Elsevier; 2021. თავი იშემიური ინსულტის ჰემორაგიული ტრანსფორმაციის შესახებ.
- January CT, Wann LS, Calkins H, et al. 2019 AHA/ACC/HRS Focused Update of the 2014 AHA/ACC/HRS Guideline for the Management of Patients With Atrial Fibrillation: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2019 Jul 9;140(2):e125-e151.
- Kernan WN, Ovbiagele B, Black HR, et al; American Heart Association Stroke Council, Council on Cardiovascular and Stroke Nursing, Council on Clinical Cardiology, and Council on Peripheral Vascular Disease. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2014 Jul;45(7):2160-236.
- Holmes DR Jr, Reddy VY, Turi ZG, et al; PROTECT AF Investigators. Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomised non-inferiority trial. Lancet. 2009 Aug 15;374(9689):534-42.
- Saver JL, Carroll JD, Thaler DE, et al; RESPECT Investigators. Long-Term Outcomes of Patent Foramen Ovale Closure or Medical Therapy after Cryptogenic Stroke. N Engl J Med. 2017 Sep 14;377(11):1022-1032.
- Baddour LM, Wilson WR, Bayer AS, et al; American Heart Association Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the Council on Cardiovascular Disease in the Young, Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and Stroke Council. Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for Healthcare Professionals From the American Heart Association. Circulation. 2015 Oct 13;132(15):1435-86.
- Osborn AG, Hedlund GL, Salzman KL. Osborn's Brain: Imaging, Pathology, and Anatomy. 2nd ed. Elsevier; 2017. განყოფილება ინსულტისა და სისხლძარღვოვანი დაავადებების შესახებ.
- Lazzaro NA, Wright B, Castillo M, et al. Artery of Percheron infarction: imaging patterns and clinical spectrum. AJNR Am J Neuroradiol. 2010 Aug;31(7):1283-9.
- Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the Early Management of Patients With Acute Ischemic Stroke: 2019 Update to the 2018 Guidelines for the Early Management of Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-e418.
- Caplan LR. Stroke Mimics. Semin Neurol. 2016 Apr;36(2):203-12.
- Grotta JC, Albers GW, Broderick JP, et al. Stroke: Pathophysiology, Diagnosis, and Management. 7th ed. Elsevier; 2021. თავი იშემიური ინსულტის პათოფიზიოლოგიის შესახებ (პენუმბრა).
- Goyal M, Menon BK, van Zwam WH, et al; HERMES collaborators. Endovascular thrombectomy after large-vessel ischaemic stroke: a meta-analysis of individual patient data from five randomised trials. Lancet. 2016 Apr 23;387(10029):1723-31.
- Paciaroni M, Agnelli G, Falocci N, et al. Early Recurrence and Cerebral Bleeding in Patients With Acute Ischemic Stroke and Atrial Fibrillation: Effect of Anticoagulation and Its Timing: The RAF Study. Stroke. 2015 Aug;46(8):2175-82.
- Nogueira RG, Jadhav AP, Haussen DC, et al; DAWN Trial Investigators. Thrombectomy 6 to 24 Hours after Stroke with a Mismatch between Deficit and Infarct. N Engl J Med. 2018 Jan 4;378(1):11-21.
იხილეთ აგრეთვე
- სიგმოიდური სინუსის ჩირქოვანი თრომბოფლებიტი თრომბოზით
- სპონტანური ინტრაკრანიალური (სუბარაქნოიდული) და ინტრაცერებრული სისხლჩაქცევა:
- გიგანტური ინტრაკრანიალური ანევრიზმები
- თავის ტვინის არტერიოვენოზური მალფორმაციები
- ინტრაცერებრული სისხლჩაქცევის სხვა მიზეზები
- კომუნიკაციური ჰიდროცეფალია ინტრაცერებრული სისხლჩაქცევის შემდეგ გამსკდარი ანევრიზმით
- ლობარული ინტრაცერებრული სისხლჩაქცევა
- მიკოზური ინტრაკრანიალური ანევრიზმები
- საკულარული ანევრიზმა და სუბარაქნოიდული სისხლჩაქცევა
- ცერებრალური არტერიების ანთებითი დაავადებები (ცერებრალური არტერიიტი)
- ცერებრალური არტერიის ანევრიზმის განმეორებითი გასკდომა
- ცერებრალური ვაზოსპაზმი
- ჰიპერტენზიული ინტრაცერებრული სისხლჩაქცევა
- თავის ტვინის იშემიური დაავადება:
- ათეროსკლეროზული თრომბოზი
- ვერტებრობაზილარული და ტვინის უკანა არტერიების ათეროთრომბოზული ოკლუზია
- ძირითადი არტერიის ათეროთრომბოზული ოკლუზია
- იშემიური ინსულტის (ცერებრალური ინფარქტის) სხვა მიზეზები
- კაროტიდული ბიფურკაციის უსიმპტომო სტენოზი შუილით
- მცირე სისხლძარღვების ინსულტი (ლაკუნური ინფარქტი)
- ტვინის უკანა არტერიის ათეროთრომბოზული ოკლუზია
- ცერებრალური ემბოლია
- შიდა საძილე არტერიის ათეროთრომბოზული ოკლუზია
- ხერხემლისა და უკანა ქვედა ნათხემის არტერიების (PICA) ათეროთრომბოზული ოკლუზია
- იშემიური ინსულტი, ტრანზიტული იშემიური შეტევა (TIA), თავის ტვინის იშემია
- ვერტებრობაზილარული უკმარისობა (VBI) თავბრუსხვევის სიმპტომით
- ცერებროვასკულური დაავადებები - იშემიური ინსულტი, ტრანზიტული იშემიური შეტევა (TIA):

-in-close-proximity-to-the-tumor-on-gadolinium-enhanced-T1-weighted-MRI-sequences.jpg)