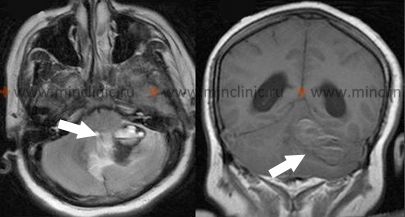
საერთო საძილე არტერიის აუზში გარდამავალი იშემიური შეტევების (მიკროინსულტის) მკურნალობა
ანტიკოაგულანტური თერაპია
პაციენტებში, რომლებსაც აღენიშნებათ ტრანზიტული იშემიური შეტევები (TIA), რომლებიც სავარაუდოდ გამოწვეულია შიდა საძილე არტერიის (ICA) ან შუა ტვინის არტერიის (MCA) მძიმე სტენოზით ან თითქმის ოკლუზიით, ოპტიმალური მწვავე სამედიცინო მართვის სტრატეგია გადამწყვეტია, მაგრამ შეიძლება იყოს რთული [1]. მიუხედავად იმისა, რომ ანტითრომბოციტული თერაპიის დაუყოვნებლივ დაწყება სტანდარტული პრაქტიკაა [2], მწვავე ანტიკოაგულაციის როლი ჰეპარინით სადავოა [1]. ისტორიულად, ჰეპარინი ზოგჯერ ემპირიულად გამოიყენებოდა მაღალი რისკის სიტუაციებში, როგორიცაა TIA-ების კრესჩენდო (მრავლობითი ხშირი TIA) ან საეჭვო მიმდინარე თრომბის ფორმირება/პროპაგაცია, მოსალოდნელი ინსულტის პრევენციის მიზნით საბოლოო დიაგნოზის ან ჩარევის მოლოდინში [1]. თუმცა, არ არსებობს მყარი მტკიცებულება, რომელიც აჩვენებს მწვავე ჰეპარინის უპირატესობას ანტითრომბოციტულ თერაპიასთან შედარებით ამ პირობებში [1, 2]. გარდა ამისა, ანტიკოაგულაცია ატარებს სისხლდენის თანდაყოლილ რისკს, ნებისმიერი პოტენციური მცირე ინფარქტის ჰემორაგიული გარდაქმნის ჩათვლით [1]. ამიტომ, მსხვილი არტერიების სტენოზთან დაკავშირებული TIA-ებისთვის მწვავე ჰეპარინის გამოყენების გადაწყვეტილებას ზოგადად იღებენ სპეციალისტები ინდივიდუალურად, მოსალოდნელი ინსულტის აღქმული რისკის შეწონვით ანტიკოაგულაციის რისკებთან, და ეს არ განიხილება როგორც რუტინული საწყისი თერაპია [1, 2].
გრძელვადიანი ორალური ანტიკოაგულაციის (როგორიცაა ვარფარინი) როლი ინსულტის მეორადი პრევენციისთვის ტრანზიტული იშემიური შეტევების (TIA) შემდეგ, რომლებიც კონკრეტულად უკავშირდება საძილე ან შუა ტვინის არტერიების ათეროსკლეროზულ სტენოზს (ანუ არა-კარდიოემბოლიური მიზეზები) ძალზე სადავოა და ზოგადად *არ* წარმოადგენს მოვლის სტანდარტს ანტითრომბოციტულ თერაპიასთან შედარებით [1, 2]. ძველ კვლევებზე დაყრდნობით ამ ჩვენებისთვის ანტიკოაგულაციის ეფექტურობის შეფასება რთულია შეზღუდვების გამო, მათ შორის [1]:
- ადეკვატური რანდომიზაციის ნაკლებობა, რომელიც ადარებს ანტიკოაგულანტებს უშუალოდ თანამედროვე ანტითრომბოციტულ რეჟიმებთან.
- ხშირად პაციენტთა მცირე რაოდენობა კონკრეტულ ქვეჯგუფებში.
- არათანმიმდევრული სადიაგნოსტიკო კრიტერიუმები და მეთოდები TIA ეტიოლოგიის დასადგენად კვლევებში.
ზოგიერთი ძველი კვლევის ინტერპრეტაცია ასევე შეიძლება გართულდეს პაციენტების ჩართვით, რომელთა სიმპტომები არ იყო ნამდვილად იშემიური ან პოტენციურად განპირობებული იყო დიდი არტერიების ათეროსკლეროზის გარდა სხვა მიზეზებით [1].
მიმდინარე გაიდლაინები მკაცრად უჭერენ მხარს ანტითრომბოციტულ აგენტებს გრძელვადიანი მეორადი პრევენციისთვის პაციენტებში TIA-ით ან იშემიური ინსულტებით, რომლებიც მიეკუთვნება დიდი არტერიების ათეროსკლეროზს [2]. მიუხედავად იმისა, რომ ისტორიულად ანტიკოაგულაცია ზოგჯერ განიხილებოდა პაციენტებისთვის, რომლებიც შეუფერებლად ითვლებოდნენ ქირურგიული ან ენდოვასკულური რევასკულარიზაციისთვის (მაგ., მიუწვდომელი დაზიანებების გამო, როგორიცაა მაღალი საძილე სიფონის სტენოზი ან MCA სტენოზი), ანტითრომბოციტული თერაპია ახლა მთავარია ასეთ შემთხვევებში, გარდა იმ შემთხვევისა, როდესაც არსებობს ანტიკოაგულაციის დამაჯერებელი ცალკე ჩვენება (მაგ., თანმხლები წინაგულების ფიბრილაცია) [1, 2].
მძიმე სიმპტომატური ინტრაკრანიალური სტენოზისთვის (როგორიცაა მნიშვნელოვანი MCA სტენოზი), ძირითადმა კლინიკურმა კვლევებმა (როგორიცაა SAMMPRIS [3]) აჩვენა, რომ ინტენსიური სამედიცინო მართვა, ორმაგი ანტითრომბოციტული თერაპიის ჩათვლით (ასპირინი და კლოპიდოგრელი) საწყისი პერიოდის განმავლობაში (მაგ., 90 დღე), რომელსაც მოსდევს გრძელვადიანი ერთიანი ანტითრომბოციტული თერაპია, კომბინირებული რისკ-ფაქტორების აგრესიულ კონტროლთან (განსაკუთრებით არტერიული წნევა და ლიპიდები), აღემატება ენდოვასკულურ სტენტირებას და რეკომენდებული მიდგომაა [3]. გრძელვადიანი ანტიკოაგულაცია ზოგადად არ არის რეკომენდებული ამ ჩვენებისთვის, ანტითრომბოციტულ საშუალებებთან შედარებით დადასტურებული სარგებლის არარსებობისა და სისხლდენის გაზრდილი რისკის გამო[1, 3].
თერაპიული ანტიკოაგულაცია ატარებს სისხლდენის მნიშვნელოვან რისკებს [1]. აბსოლუტური უკუჩვენებებია სიტუაციები, სადაც სისხლდენის რისკი აშკარად აღემატება პოტენციურ სარგებელს, და ზოგადად მოიცავს [1]:
- აქტიური, კლინიკურად მნიშვნელოვანი სისხლდენა.
- მძიმე არაკონტროლირებადი ჰიპერტენზია.
- ბოლოდროინდელი მძიმე ტრავმა ან ოპერაცია (განსაკუთრებით ინტრაკრანიალური ან სპინალური).
- ინტრაკრანიალური სისხლჩაქცევის მაღალი რისკი (მაგ., ბოლოდროინდელი დიდი ინფარქტი ჰემორაგიული გარდაქმნის რისკით, ცნობილი ცერებრალური ამილოიდური ანგიოპათია).
- მძიმე თრომბოციტოპენია ან ცნობილი კოაგულოპათია.
- ღვიძლის მძიმე დაავადება დარღვეული კოაგულაციით.
ფარდობითი უკუჩვენებები მოითხოვს რისკისა და სარგებლის ფრთხილ ინდივიდუალურ შეფასებას და მოიცავს ისეთ ფაქტორებს, როგორიცაა [1]:
- ხანდაზმული ასაკი.
- ზომიერი ან რთულად საკონტროლო ჰიპერტენზია.
- მნიშვნელოვანი კუჭ-ნაწლავის ან სხვა სისხლდენის ისტორია.
- დაცემის მაღალი რისკი.
- თირკმლის ქრონიკული დაავადება.
- სხვა მედიკამენტების ერთდროული გამოყენება, რომლებიც გავლენას ახდენენ სისხლდენის რისკზე (მაგ., არასტეროიდული ანთების საწინააღმდეგო საშუალებები - NSAIDs).
ჰეპარინით მოკლევადიანი ანტიკოაგულაცია ზოგჯერ შეიძლება განიხილებოდეს მწვავე პირობებში სპეციფიკური მაღალი რისკის სცენარებისთვის, როგორიცაა კრესჩენდო TIA-ები, რომლებიც სავარაუდოდ მეორადია კრიტიკული საძილე სტენოზის მიმართ, პოტენციურად, როგორც ხიდი გადაუდებელი რევასკულარიზაციის (მაგ., ენდარტერექტომია ან სტენტირება) მოლოდინში [1]. თუმცა, ეს არ არის რუტინული პრაქტიკა, მოითხოვს პაციენტთა ფრთხილად შერჩევას და უნდა დააბალანსოს აღქმული თრომბოზული რისკი სისხლდენის დაუყოვნებლივ რისკთან[1, 2].
თრომბოციტების ანტიაგრეგაციული თერაპია
ანტითრომბოციტული თერაპია არის სამედიცინო მართვის ქვაკუთხედი განმეორებითი იშემიური მოვლენების თავიდან ასაცილებლად ტრანზიტული იშემიური შეტევის (TIA) ან მცირე იშემიური ინსულტის შემდეგ, რომელიც მიეკუთვნება არა-კარდიოემბოლიურ მიზეზებს (როგორიცაა დიდი არტერიების ათეროსკლეროზი ან მცირე სისხლძარღვების დაავადება)[1, 2]. მიუხედავად იმისა, რომ მეორადი პრევენციის ნებისმიერი სტრატეგიის ეფექტურობა ექვემდებარება მიმდინარე კვლევასა და დახვეწას, ანტითრომბოციტული აგენტების ფუნდამენტური სარგებელი კარგად არის დადგენილი, განსხვავებით ანტიკოაგულანტების უფრო საკამათო როლისა ამ სპეციფიკური ჩვენებებისთვის [1, 2]. აცეტილსალიცილის მჟავა (ასპირინი) არის ყველაზე ფართოდ შესწავლილი ანტითრომბოციტული აგენტი ამ მიზნით [2]. მრავალრიცხოვანმა რანდომიზებულმა კონტროლირებადმა კვლევამ შეაფასა ასპირინის მონოთერაპია, ისევე როგორც ასპირინი სხვა ანტითრომბოციტულ აგენტებთან (როგორიცაა კლოპიდოგრელი ან დიპირიდამოლი) კომბინაციაში [2, 4]. ამ კვლევებმა თანმიმდევრულად აჩვენა, რომ ანტითრომბოციტული თერაპია, მარტო ასპირინის ჩათვლით, მნიშვნელოვნად ამცირებს განმეორებითი TIA-ს, ინსულტის და სხვა სისხლძარღვოვანი მოვლენების რისკს პაციენტებში, რომლებსაც აქვთ იშემიური ცერებროვასკულური სიმპტომები [2, 4]. მიმდინარე გაიდლაინები ხშირად გვირჩევენ ორმაგი ანტითრომბოციტული თერაპიის (DAPT, ტიპიურად ასპირინი პლუს კლოპიდოგრელი) დაწყებას მოკლე დროით (მაგ., 21-90 დღე) მაღალი რისკის TIA-ს ან მცირე იშემიური ინსულტის მქონე პაციენტებში, რასაც მოჰყვება გრძელვადიანი ერთიანი ანტითრომბოციტული თერაპია, ადრეული რისკის შემცირების შემდგომი ოპტიმიზაციისთვის[2, 5].
მიუხედავად იმისა, რომ ადრეული კვლევები, რომლებიც ადარებდნენ ასპირინს პლაცებოს ტრანზიტული იშემიური შეტევის (TIA) ან მცირე ინსულტის შემდეგ, ზოგჯერ მოიცავდა პაციენტებს, სადაც ზუსტი მიზეზი არ იყო საბოლოოდ დადგენილი ანგიოგრაფიით, ანტითრომბოციტული თერაპიის, განსაკუთრებით ასპირინის საერთო სარგებელი განმეორებითი არა-კარდიოემბოლიური იშემიური მოვლენების შემცირებაში კარგად არის დადგენილი [2]. ზოგიერთი ანალიზი ვარაუდობდა, რომ ასპირინმა შეიძლება უზრუნველყოს მეტი სარგებელი პაციენტებში, რომლებსაც აქვთ დადასტურებული ათეროსკლეროზული დაზიანებები საძილე არტერიებში, ვიდრე მათში, ვისაც ასეთი დაზიანებები არ აქვთ (სადაც კარდიოემბოლიური წყარო შეიძლება უფრო სავარაუდო იყოს), მაგრამ ანტითრომბოციტული თერაპია რჩება ნაჩვენები მეორადი პრევენციისთვის ორივე სცენარში, გარდა იმ შემთხვევისა, როდესაც ანტიკოაგულაციაა საჭირო (მაგ., წინაგულების ფიბრილაციისთვის) [1, 2]. მხოლოდ ასპირინით (სამედიცინო მართვა) მიღებული რისკის შემცირების შედარება კაროტიდული ენდარტერექტომიით (CEA) მიღწეულთან მოითხოვს ფრთხილ კონტექსტს: CEA უზრუნველყოფს არსებით რისკის შემცირებას *მხოლოდ* სამედიცინო თერაპიასთან შედარებით სპეციალურად პაციენტებში *მძიმე სიმპტომატური* საძილე სტენოზით (ტიპიურად 70-99%, ან ზოგჯერ 50-69% კონკრეტულ ფაქტორებზე დაყრდნობით)[6, 7].
ასპირინი (ან სხვა ანტითრომბოციტული აგენტები, როგორიცაა კლოპიდოგრელი) ითვლება ფუნდამენტურ სამედიცინო თერაპიად ათეროსკლეროზთან დაკავშირებული TIA-ს ან ინსულტის მქონე პაციენტებისთვის და არა მხოლოდ დანამატად ან ალტერნატივად [2]. იგი გამოიყენება დაავადების სიმძიმის სპექტრში, მათ შორის მსუბუქი სტენოზის, მძიმე სტენოზის შემთხვევებში, რომლებიც შეუფერებელია ჩარევისთვის ან მოლოდინის რეჟიმშია (მაგ., მიუწვდომელი დაზიანებების გამო, როგორიცაა მაღალი საძილე სიფონი ან MCA სტენოზი), ან რევასკულარიზაციის პროცედურების შემდეგ [2].
ასპირინი ახდენს თავის პირველად ანტითრომბოციტულ ეფექტს თრომბოციტების შიგნით ციკლოოქსიგენაზა-1 (COX-1) ფერმენტის შეუქცევადი ინჰიბირებით[8]. ეს მოქმედება ხელს უშლის თრომბოქსან A2-ის (TXA2) სინთეზს, რომელიც არის თრომბოციტების აგრეგაციის და ვაზოკონსტრიქციის ძლიერი პრომოტორი [8]. ასპირინი ასევე აფერხებს COX ფერმენტებს ენდოთელურ უჯრედებში, ამცირებს პროსტაციკლინის (PGI2) წარმოქმნას, რომელიც ნორმაში აფერხებს თრომბოციტების აგრეგაციას და იწვევს ვაზოდილატაციას [8]. ეს უკანასკნელი ეფექტი პოტენციურად არასასურველია, მაგრამ ასპირინის კლინიკური სარგებელი იმაზე მეტყველებს, რომ თრომბოციტების TXA2-ის დათრგუნვა ჭარბობს, განსაკუთრებით დაბალ დოზებში [8].
იმის გამო, რომ თრომბოციტების COX-1-ის ინჰიბირება ეფექტურად მიიღწევა დაბალ დოზებშიც კი, და უფრო მაღალმა დოზებმა შეიძლება გაზარდოს სისხლდენის რისკი და პოტენციურად უფრო მნიშვნელოვნად დათრგუნოს პროსტაციკლინი, ინსულტის მეორადი პრევენციისთვის სტანდარტული დოზები ტიპიურად დაბალია (მაგ., 75-100 მგ დღეში, ან 81-325 მგ დღეში, რეგიონალური გაიდლაინების და კონკრეტული კლინიკური სიტუაციების მიხედვით) [2, 8].
დიპირიდამოლი არის კიდევ ერთი ანტითრომბოციტული აგენტი, რომლის მექანიზმი მოიცავს ფოსფოდიესტერაზას ინჰიბირებას (ზრდის თრომბოციტების cAMP-ს) და პოტენციურად ადენოზინის შეწოვას, რაც საბოლოოდ ამცირებს თრომბოციტების აგრეგაციას[8]. მიუხედავად იმისა, რომ დიპირიდამოლის მონოთერაპიის მტკიცებულებები შეზღუდულია, გახანგრძლივებული გამოთავისუფლების დიპირიდამოლის კომბინაცია ასპირინთან კვლევებში ნაჩვენებია, რომ ეფექტურია ინსულტის მეორადი პრევენციისთვის და წარმოადგენს დადგენილ მკურნალობის ვარიანტს, თუმცა მისი გამოყენება სხვა აგენტებთან მიმართებაში, როგორიცაა კლოპიდოგრელი, დროთა განმავლობაში იცვლებოდა[2, 4].
კლოპიდოგრელი არის ფართოდ გამოყენებული ანტითრომბოციტული აგენტი, რომელიც შეუქცევადად ბლოკავს P2Y12 ადენოზინდიფოსფატის (ADP) რეცეპტორს თრომბოციტებზე, ხელს უშლის ADP-ით შუამავლობით თრომბოციტების აქტივაციას და აგრეგაციას [8]. ის ხშირად გამოიყენება როგორც ასპირინის ალტერნატივა პაციენტებისთვის, რომლებიც ვერ იტანენ ასპირინს, ან ასპირინთან კომბინაციაში (ორმაგი ანტითრომბოციტული თერაპია - DAPT) შეზღუდული ვადით გარკვეული მაღალი რისკის TIA-ების ან მცირე ინსულტების შემდეგ [2, 5]. სულფინპირაზონს აქვს ანტითრომბოციტული ეფექტები, მაგრამ არ არის სტანდარტული თერაპია TIA/ინსულტის პრევენციისთვის. კლოფიბრატი არის ლიპიდების დამწევი აგენტი და მიუხედავად იმისა, რომ არასტეროიდულ ანთების საწინააღმდეგო საშუალებებს, როგორიცაა იბუპროფენი, აქვთ გარკვეული ანტითრომბოციტული ეფექტი, ისინი არ გამოიყენება ინსულტის მეორადი პრევენციისთვის და შეიძლება ხელი შეუშალონ ასპირინის ეფექტურობას ან გაზარდონ სისხლდენის რისკი [8].
| თერაპიის ტიპი | ჩვენება (სიმპტომური საძილე არტერიის TIA) | ძირითადი სარგებელი / ვადები |
|---|---|---|
| ორმაგი ანტიაგრეგანტული თერაპია (ასპირინი + კლოპიდოგრელი) | მაღალი რისკის TIA / მცირე ინსულტი | ადრეული ეტაპი (21–90 დღე), შემდეგ გადასვლა ერთ პრეპარატზე |
| საძილე არტერიის ენდარტერექტომია (CEA) | მძიმე სიმპტომური სტენოზი (≥70%, ხშირად 50–69%) | მდგრადი მდგომარეობისას 2 კვირის განმავლობაში; ამცირებს ინსულტის რისკს |
| საძილე არტერიის სტენტირება (CAS) | მაღალი ქირურგიული რისკი ან არახელსაყრელი ანატომია | CEA-ს ალტერნატივა; გამოიყენება ემბოლიისგან დამცავი საშუალებები |
| ანტიკოაგულაცია (მაგ. ჰეპარინი/ვარფარინი) | არ არის რუტინული (მხოლოდ AF ან სხვა მკაფიო ჩვენებისას) | სისხლდენის რისკი, როგორც წესი, აღემატება სარგებელს |
ქირურგიული თერაპია
კაროტიდული ენდარტერექტომია
კაროტიდული ენდარტერექტომია (CEA) არის კარგად დამკვიდრებული ქირურგიული პროცედურა შიდა საძილე არტერიის მნიშვნელოვანი ათეროსკლეროზული სტენოზის სამკურნალოდ, განსაკუთრებით მაშინ, როდესაც მან გამოიწვია ისეთი სიმპტომები, როგორიცაა ტრანზიტული იშემიური შეტევა (TIA) ან მცირე ინსულტი [1, 9]. პირველად ჩატარებული 1950-იან წლებში, ოპერაცია გულისხმობს არტერიიდან დაგროვილი ფოლაქის ქირურგიულ მოცილებას ნორმალური სისხლის ნაკადის აღსადგენად და, რაც მთავარია, მომავალი ინსულტების თავიდან ასაცილებლად [9]. ნებისმიერი დიდი ოპერაციის მსგავსად, CEA ატარებს თანდაყოლილ რისკებს, მათ შორის პერიოპერაციული ინსულტის, სიკვდილის, კრანიალური ნერვის დაზიანების და მიოკარდიუმის ინფარქტის [9]. თუმცა, გამოცდილ ცენტრებში, რომლებიც ასრულებენ პროცედურას სათანადოდ შერჩეულ პაციენტებზე, ძირითადი გართულებების რისკი, როგორიცაა პერიოპერაციული ინსულტი ან სიკვდილი, ზოგადად დაბალია (ხშირად მოხსენიებულია როგორც <6% სიმპტომატური პაციენტებისთვის და <3% უსიმპტომო პაციენტებისთვის, თუმცა რეალური შედეგები განსხვავდება)[2, 9]. გადამწყვეტად მნიშვნელოვანია, რომ საეტაპო რანდომიზებულმა კონტროლირებადმა კვლევებმა (როგორიცაა NASCET [6] და ECST [7]) ათწლეულების წინ საბოლოოდ აჩვენა, რომ პაციენტებისთვის მძიმე (ტიპიურად 70-99%) სიმპტომატური საძილე სტენოზით, CEA უზრუნველყოფს მნიშვნელოვან გრძელვადიან სარგებელს ინსულტის რისკის შესამცირებლად მხოლოდ სამედიცინო თერაპიასთან შედარებით [6, 7]. სარგებელი ასევე შეიძლება არსებობდეს ფრთხილად შერჩეული პაციენტებისთვის ზომიერი (50-69%) სიმპტომატური სტენოზით [6]. ამიტომ, პროცედურული რისკების მიუხედავად, CEA ითვლება სასიცოცხლო და ეფექტურ მკურნალობად ინსულტის პრევენციისთვის სათანადოდ შერჩეულ პირებში, რადგან გრძელვადიანი სარგებელი აშკარად აღემატება ქირურგიულ რისკებს ამ მაღალი რისკის პოპულაციაში[2, 6, 7].
პაციენტებს, რომლებსაც უტარდებათ კაროტიდული ენდარტერექტომია (CEA), ემუქრებათ პერიოპერაციული ინსულტის გაზრდილი რისკი, თუ მათ აქვთ გარკვეული ანატომიური ან ფიზიოლოგიური ფაქტორები, რომლებიც აფერხებენ ცერებრალურ კოლატერალურ ცირკულაციას [1, 9]. ეს ფაქტორები მოიცავს კონტრალატერალური საძილე არტერიის მძიმე სტენოზს ან ოკლუზიას, ან არაადეკვატურ კოლატერალურ გზებს ვილისის წრის მეშვეობით [1]. ინტრაოპერაციული ნეირომონიტორინგი, როგორიცაა უწყვეტი ელექტროენცეფალოგრაფიის (EEG) მონიტორინგი ან სომატოსენსორული გამოწვეული პოტენციალები (SSEPs), ხშირად გამოიყენება პროცედურის დროს [9]. მონიტორინგი მიზნად ისახავს აღმოაჩინოს ცერებრალური იშემიის ნიშნები, რომლებიც შეიძლება მოხდეს საძილე არტერიის დროებითი დაკეტვისას [9]. თუ აღმოჩენილია იშემიის მიმანიშნებელი მნიშვნელოვანი ცვლილებები, ქირურგმა შეიძლება აირჩიოს დროებითი შუნტის დაყენება ფოლაქის ამოღების დროს ტვინში სისხლის ნაკადის შესანარჩუნებლად [9].
პაციენტებს, რომლებსაც ესაჭიროებათ CEA, ხშირად აქვთ მნიშვნელოვანი თანმხლები დაავადებები, რაც ასახავს ათეროსკლეროზის სისტემურ ბუნებას [9]. არტერიული ჰიპერტენზია, კორონარული არტერიის დაავადება (CAD) და პერიფერიული სისხლძარღვების დაავადება გავრცელებულია [9]. გარკვეული პირობები მნიშვნელოვნად ზრდის ოპერაციის რისკს და შეიძლება წარმოადგენდეს ფარდობით ან აბსოლუტურ უკუჩვენებებს [9]. ესენია არასტაბილური სტენოკარდია, ბოლოდროინდელი მიოკარდიუმის ინფარქტი (ტიპიურად ბოლო რამდენიმე თვის განმავლობაში), და მძიმე შეგუბებითი გულის უკმარისობა ან მკვეთრად შემცირებული განდევნის ფრაქცია [9]. მიუხედავად იმისა, რომ მნიშვნელოვანი ჰიპერტენზია იდეალურად კონტროლირებადი უნდა იყოს დაგეგმილ ოპერაციამდე, არტერიული წნევის გადაჭარბებული დაქვეითება კრიტიკული საძილე სტენოზის მქონე პაციენტებში თავიდან უნდა იქნას აცილებული, რადგან ჰიპოტენზიამ შეიძლება გამოიწვიოს თრომბოზი სტენოზურ ადგილას ან გამოიწვიოს ცერებრალური ჰიპოპერფუზია, რამაც პოტენციურად შეიძლება გამოიწვიოს იშემიური ინსულტი [1].
რესტენოზი, ანუ საძილე არტერიის ნამკურნალები სეგმენტის ხელახალი შევიწროება, შეიძლება მოხდეს კაროტიდული ენდარტერექტომიის (CEA) შემდეგ, თუმცა მნიშვნელოვანი, ნაკადის შემზღუდველი რესტენოზი შედარებით იშვიათია [9]. ადრეული რესტენოზი (ტიპიურად პირველი 1-2 წლის განმავლობაში) ხშირად მიეწერება პირველ რიგში ნეოინტიმალურ ჰიპერპლაზიას (გადაჭარბებული შეხორცების პასუხი, რომელიც მოიცავს გლუვი კუნთოვანი უჯრედების პროლიფერაციას და მატრიქსის დეპონირებას)[9]. მოგვიანებითი რესტენოზი (ხდება 2 წლის შემდეგ) უფრო ხშირად განპირობებულია პროგრესირებადი ათეროსკლეროზით ნამკურნალებ სეგმენტში ან მიმდებარე უბნებში [9]. მიუხედავად იმისა, რომ კლინიკურად მნიშვნელოვანმა რესტენოზმა შეიძლება გამოიწვიოს განმეორებითი სიმპტომები, განმეორებითი ქირურგიული ჩარევა (ხელახალი CEA) ტექნიკურად უფრო რთულია საწყისი ოპერაციის შედეგად ნაწიბუროვანი ქსოვილის ფორმირების გამო, რაც პოტენციურად ზრდის პროცედურულ რისკებს [9]. ენდოვასკულური მკურნალობა ანგიოპლასტიკით და სტენტირებით ხშირად განიხილება როგორც ალტერნატივა მნიშვნელოვანი რესტენოზის მართვისთვის [9, 10].
ტანდემური დაზიანებების მართვა, სადაც მნიშვნელოვანი სტენოზი არსებობს როგორც საძილე ბიფურკაციაში (შიდა საძილე არტერიის საწყისი), ასევე უფრო დისტალურად ინტრაკრანიალურ სეგმენტში (მაგ., საძილე სიფონი), წარმოადგენს რთულ გამოწვევას [1]. მკურნალობის გადაწყვეტილებები უაღრესად ინდივიდუალიზებულია და დამოკიდებულია ისეთ ფაქტორებზე, როგორიცაა თითოეული სტენოზის სიმძიმე და ლოკაცია, პაციენტის სიმპტომები, საერთო სისხლძარღვოვანი ჯანმრთელობა და პროცედურული რისკები [1]. მხოლოდ დიამეტრის მარტივი გაზომვები არასაკმარისია გადაწყვეტილების მისაღებად. ვარიანტები შეიძლება მოიცავდეს CEA-ს ბიფურკაციის დაზიანებისთვის კომბინირებულს ინტენსიურ სამედიცინო მართვასთან სიფონის დაზიანებისთვის, ერთი ან ორივე დაზიანების ენდოვასკულურ მკურნალობას (სტენტირება) (თუმცა ინტრაკრანიალურ სტენტირებას აქვს სპეციფიკური რისკები და ჩვენებები [3]), ან მხოლოდ ინტენსიურ სამედიცინო მართვას ანტითრომბოციტული აგენტებით და რისკ-ფაქტორების აგრესიული კონტროლით [1, 2]. არ არსებობს საყოველთაო კონსენსუსი ოპტიმალურ მიდგომაზე ყველა ტანდემური დაზიანებისთვის, და მართვა ხშირად მოიცავს მულტიდისციპლინურ განხილვას [1].
ენდოვასკულური თერაპია (სტენტირება და ბალონური ანგიოპლასტიკა)
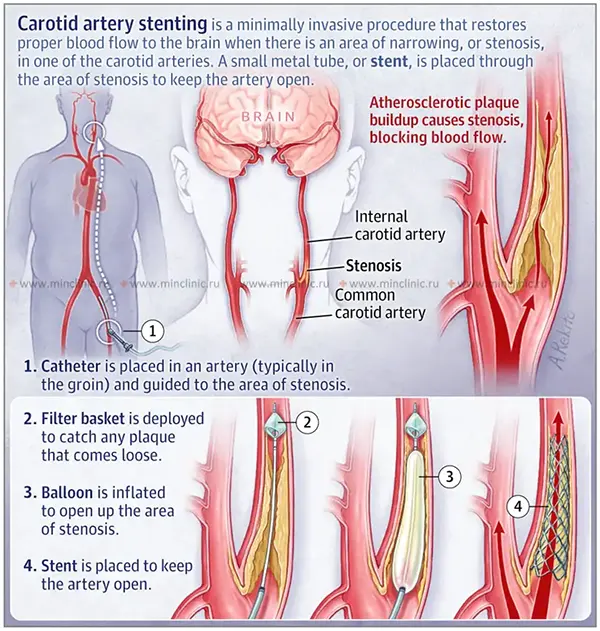
ენდოვასკულური მკურნალობა, კერძოდ საძილე არტერიის სტენტირება (CAS) ხშირად კომბინირებული ბალონურ ანგიოპლასტიკასთან, არის დადგენილი მინიმალურად ინვაზიური ვარიანტი საძილე არტერიის სტენოზის სამკურნალოდ, რომელიც გამოიყენება კაროტიდული ენდარტერექტომიის (CEA) ალტერნატივად შერჩეულ პაციენტებში[2, 10]. იგი სრულდება სათანადოდ გაწვრთნილი სპეციალისტების მიერ (მათ შორის ინტერვენციული რადიოლოგების, ნევროლოგების, კარდიოლოგების და სისხლძარღვთა ქირურგების). CAS გულისხმობს სტენტის განთავსებას სტენოზურ დაზიანებაზე, რათა გაფართოვდეს არტერიის სანათური და შენარჩუნდეს გამავლობა, რითაც უმჯობესდება ტვინში სისხლის ნაკადი [10]. ეს ტექნიკა შეიძლება გამოყენებულ იქნას სტენოზის დროს, რომელიც მდებარეობს:
- საძილე ბიფურკაციაში (სადაც საერთო საძილე იყოფა შიდა და გარე საძილე არტერიებად).
- შიდა საძილე არტერიის საშვილოსნოს ყელის სეგმენტებში (ქალას ფუძის ქვემოთ).
- შერჩეულ დაზიანებებში შიდა საძილე არტერიის ინტრაკრანიალურ სეგმენტებში (თუმცა ჩვენებები და რისკები მნიშვნელოვნად განსხვავდება ინტრაკრანიალური სტენტირებისთვის ექსტრაკრანიალურ CAS-თან შედარებით) [3].
ათერექტომიის მოწყობილობის მაგალითი, რომელიც ზოგჯერ გამოიყენება პერიფერიული ან სხვა არტერიული დაავადებების ენდოვასკულურ მკურნალობაში (დაკავშირებულია ათეროსკლეროზული სისხლძარღვოვანი დაავადების მართვასთან). შენიშვნა: ათერექტომია განსხვავდება სტანდარტული საძილე სტენტირებისგან.
საძილე არტერიის სტენტირება (CAS) ხშირად განიხილება იმ პაციენტებისთვის, რომლებიც ითვლებიან კაროტიდული ენდარტერექტომიისთვის (CEA) მაღალი რისკის მქონედ სპეციფიკური ანატომიური ფაქტორების (მაგ., წინა რადიკალური კისრის ოპერაცია ან დასხივება, რესტენოზი წინა CEA-ს შემდეგ, კონტრალატერალური ხორხის ნერვის პარეზი, დაზიანების ლოკაცია მაღლა კისერში ან ლავიწის ქვემოთ) ან მნიშვნელოვანი სამედიცინო თანმხლები დაავადებების (მაგ., გულის ან ფილტვის მძიმე დაავადება) გამო [2, 10]. CAS-ის დროს, ემბოლიური დაცვის მოწყობილობა (EPD) ტიპიურად გამოიყენება პროცედურის დროს მოწყვეტილი პოტენციური ნამსხვრევების (ემბოლიების) დასაჭერად, რაც ამცირებს ინსულტის რისკს [10]. ძირითადმა რანდომიზებულმა კვლევებმა (როგორიცაა CREST[11]) შეადარეს CAS (EPD-ით) და CEA [10, 11]. ძირითადი აღმოჩენები ზოგადად მიუთითებს იმაზე, რომ მიუხედავად იმისა, რომ ორივე პროცედურა ეფექტურია ინსულტის გრძელვადიან პრევენციაში შესაბამისი კანდიდატებისთვის, არსებობს განსხვავებები პერიპროცედურულ რისკებში: CAS-ს აქვს მცირე პერიპროცედურული ინსულტის ოდნავ მაღალი რისკი, მაშინ როცა CEA-ს აქვს პერიპროცედურული მიოკარდიუმის ინფარქტის ოდნავ მაღალი რისკი [11]. ძირითადი მოვლენების (ინსულტი, MI, სიკვდილი) საერთო კომპოზიტური რისკი პერიპროცედურულ პერიოდში და გრძელვადიანი შედეგები ხშირად შესადარებელია ორ პროცედურას შორის, როდესაც სრულდება გამოცდილი ოპერატორების მიერ შესაბამის პაციენტებზე [11]. პაციენტის ასაკი და სპეციფიკური რისკ-ფაქტორები გავლენას ახდენენ ფარდობით რისკებზე, და არჩევანი CAS-სა და CEA-ს შორის მოითხოვს ფრთხილ ინდივიდუალურ შეფასებას და განხილვას[2, 10, 11].
ექსტრაკრანიალური-ინტრაკრანიალური შუნტირების ოპერაცია
ექსტრაკრანიალური-ინტრაკრანიალური (EC-IC) შუნტირების (Bypass) ოპერაცია, რომელიც ტიპიურად მოიცავს სკალპის არტერიის, როგორიცაა ზედაპირული საფეთქლის არტერიის (STA), ანასტომოზს (დაკავშირებას) შუა ტვინის არტერიის (MCA) კორტიკალურ ტოტთან, შეიქმნა როგორც მეთოდი მძიმე სტენოზის ან ოკლუზიის დისტალურად ტვინის რეგიონებში სისხლის ნაკადის გასაზრდელად [1, 12]. ისტორიულად, ეს პროცედურა შეთავაზებული იყო პაციენტებისთვის სიმპტომატური ათეროსკლეროზული დაავადებით, როგორიცაა შიდა საძილე არტერიის (ICA) ოკლუზია ან მძიმე MCA სტენოზი, რომლებიც აგრძელებდნენ ტრანზიტულ იშემიურ შეტევებს (TIAs) ან მცირე ინსულტებს სამედიცინო მართვის მიუხედავად [1]. თუმცა, ძირითადმა საერთაშორისო რანდომიზებულმა კონტროლირებადმა კვლევამ, EC/IC Bypass კვლევამ, რომელიც გამოქვეყნდა 1985 წელს [13], შეადარა STA-MCA შუნტირების ოპერაცია პლუს სამედიცინო თერაპია მხოლოდ სამედიცინო თერაპიას სიმპტომატური ICA ან MCA ათეროსკლეროზული დაავადების მქონე პაციენტებისთვის. კვლევამ ცნობილია, რომ ვერ აღმოაჩინა რაიმე სარგებელი ოპერაციისგან; ოპერაციაზე რანდომიზებულ პაციენტებს არ ჰქონდათ შემდგომი ინსულტის ან სიკვდილის უფრო დაბალი რისკი იმ პაციენტებთან შედარებით, რომლებიც იღებდნენ მხოლოდ სამედიცინო თერაპიას (რაც მოიცავდა იმ დროს ხელმისაწვდომ ანტითრომბოციტულ აგენტებს) [13]. ამ საეტაპო კვლევის შედეგად, EC-IC შუნტირება ზოგადად *არ* ითვლება ეფექტურ მკურნალობად ტიპიურ ინტრაკრანიალურ ან ექსტრაკრანიალურ ათეროსკლეროზულ ოკლუზიურ დაავადებასთან დაკავშირებული ინსულტის თავიდან ასაცილებლად [1, 12]. მიუხედავად იმისა, რომ პროცედურას მაინც შეიძლება ჰქონდეს სპეციფიკური ნიშური გამოყენება ნეიროქირურგიაში (მაგ., მოიამოიას დაავადებისთვის, რთული ანევრიზმებისთვის, რომლებიც საჭიროებენ სისხლძარღვის გაწირვას, ქალას ფუძის გარკვეული სიმსივნეებისთვის), ის არ არის სტანდარტული მკურნალობა 1985 წლის კვლევაში თავდაპირველად შესწავლილი ათეროსკლეროზული ჩვენებებისთვის [12].
დაუყოვნებელი მართვის სტრატეგია იშემიური ინსულტის შემდეგ შიდა საძილე არტერიის (ICA) ტერიტორიაზე დიდად არის დამოკიდებული ინსულტის საწყის სიმძიმეზე და დაწყებიდან გასულ დროზე [1]. დიდი, დამანგრეველი ინსულტების შემთხვევაში, რომლებიც ვლინდება მძიმე დეფიციტით, როგორიცაა მჭიდრო ჰემიპლეგია, გლობალური აფაზია, ან ღრმა უგულებელყოფა/ანოსოგნოზია (რაც მიუთითებს ვრცელ ინფარქტზე, ხშირად მოიცავს შუა ტვინის არტერიის ტერიტორიის დიდ ნაწილს), მწვავე ფოკუსი გადადის ამ ტერიტორიაზე დაუყოვნებელი რეციდივის პრევენციიდან მხარდამჭერ ზრუნვაზე [1]. პრიორიტეტები მოიცავს პაციენტის სტაბილიზაციას, არტერიული წნევის ფრთხილად მართვას (ხშირად ნებადართულია პერმისიული ჰიპერტენზია თავდაპირველად, გარდა იმ შემთხვევისა, როდესაც არ ტარდება თრომბოლიზი ან თრომბექტომია), გართულებების პრევენციასა და მკურნალობას, როგორიცაა ცერებრალური შეშუპება, ასპირაციული პნევმონია და ღრმა ვენების თრომბოზი [1, 14].
მწვავე ანტიკოაგულაციის (მაგ., ჰეპარინით) როლი იშემიური ინსულტის შემდეგ დაუყოვნებლივ რჩება სადავო და ზოგადად *არ* არის რეკომენდებული ინსულტის უმეტესი ტიპებისთვის, განსაკუთრებით დიდებისთვის, ჰემორაგიული ტრანსფორმაციის გაზრდილი რისკის გამო[1, 14]. მიუხედავად იმისა, რომ ისტორიულად დაობდნენ "პროგრესირებად ინსულტზე" ან მერყევ დეფიციტებზე, მიმდინარე პრაქტიკა ტიპიურად უპირატესობას ანიჭებს ანტითრომბოციტული თერაპიის ადრეულ დაწყებას [2, 14]. ინტრავენური თრომბოლიზი (როგორიცაა ალტეპლაზა) ან ენდოვასკულური თრომბექტომია არის პირველადი ჰიპერმწვავე მკურნალობა, რომელიც მიზნად ისახავს რეპერფუზიას, თუ პაციენტი გამოცხადდება შესაბამის დროის ფანჯარაში და აკმაყოფილებს დასაშვებობის კრიტერიუმებს [14, 15].
ანტიკოაგულაციის დაწყება მცირე ინსულტიდან ან TIA-დან მალევე ახლად დიაგნოზირებული მძიმე ICA სტენოზის ან ოკლუზიის ფონზე, ასევე ზოგადად არ არის სტანდარტული პრაქტიკა, თუ არ არსებობს მკაფიო თანმხლები ჩვენება (როგორიცაა წინაგულების ფიბრილაცია) [1, 2]. მიუხედავად იმისა, რომ თეორიული მიზანი შეიძლება იყოს თრომბის პროპაგაციის ან ადრეული რეციდივის პრევენცია, მცირე ინფარქტების ჰემორაგიული გარდაქმნის რისკიც კი არსებობს [1]. ანტითრომბოციტული თერაპია არის მთავარი ამ სიტუაციებში [2].
პაციენტებისთვის, რომლებმაც განიცადეს მცირე ინსულტი ან TIA, რომელიც მიეწერება იფსილატერალური ICA-ს მძიმე (ტიპიურად 70-99%, ან ზოგჯერ 50-69% კონკრეტულ კრიტერიუმებზე დაყრდნობით), სიმპტომატურ სტენოზს, კაროტიდული ენდარტერექტომია (CEA) არის კარგად დადგენილი მეორადი პრევენციის სტრატეგია[2, 6, 7]. საეტაპო კვლევებმა (როგორიცაა NASCET[6] და ECST [7]) აჩვენა, რომ CEA მნიშვნელოვნად ამცირებს ინსულტის გრძელვადიან რისკს მხოლოდ სამედიცინო თერაპიასთან შედარებით სათანადოდ შერჩეულ პაციენტებში [6, 7]. მისაღები პერიოპერაციული რისკი (ინსულტი ან სიკვდილი) CEA-სთვის სიმპტომატურ პაციენტებში ზოგადად ითვლება <6% გამოცდილ ცენტრებში[2]. კონტრალატერალური საძილე სტენოზის ან ოკლუზიის არსებობამ შეიძლება გაზარდოს პერიოპერაციული რისკი, რაც მოითხოვს ფრთხილ შეფასებას და დაგეგმვას [1, 9]. მხოლოდ სამედიცინო მართვა მძიმე სიმპტომატური სტენოზისთვის ატარებს განმეორებითი ინსულტის მნიშვნელოვან რისკს [6, 7].
ბოლოდროინდელი ინფარქტის ჰემორაგიული ტრანსფორმაცია არის პოტენციური გართულება CEA-ს შემდეგ, თუმცა შედარებით იშვიათია, თუ ოპერაცია სათანადოდ არის დაგეგმილი დროში და თავიდან აცილებულია პოსტოპერაციული ჰიპერტენზია [1, 9]. მიმდინარეობს დებატები CEA-ს ოპტიმალური დროის შესახებ მწვავე ინსულტის შემდეგ [2, 9]. მიუხედავად იმისა, რომ ოპერაციის გადადება რამდენიმე კვირით (მაგ., 2-6 კვირა) იძლევა ინფარქტის სტაბილიზაციის საშუალებას და ამცირებს სისხლდენის რისკს, გახანგრძლივებული დაყოვნება ზრდის განმეორებითი ინსულტის რისკს ჩარევამდე [2]. უფრო ადრეული ჩარევა (დღეებიდან 2 კვირამდე) შეიძლება განიხილებოდეს, განსაკუთრებით იმ პაციენტებისთვის, რომლებსაც აქვთ TIA-ები ან ძალიან მცირე ინსულტები, რომლებიც სტაბილიზირდნენ, ოპერაციის რისკების დაბალანსებით რეციდივის მაღალ ადრეულ რისკთან [2].
გადაუდებელი CEA ან საძილე სტენტირება მწვავე ICA ოკლუზიისთვის, რომელიც იწვევს დიდ ინსულტს, ტარდება უაღრესად სპეციალიზებულ ცენტრებში, მაგრამ არ არის რუტინული; ენდოვასკულური თრომბექტომია, რომელიც მიმართულია ინტრაკრანიალურ ოკლუზიაზე, არის უფრო გავრცელებული ჰიპერმწვავე ჩარევა მსხვილი სისხლძარღვის ოკლუზიური ინსულტისთვის [14, 15]. ნებისმიერი ჩარევის შედეგები დადგენილი დიდი ინფარქტების ფონზე ხშირად ცუდია [1].
პაციენტებისთვის სიმპტომატური ICA ოკლუზიით (და არა სტენოზით), რომელიც იწვევს მსუბუქ ან ზომიერ ინსულტს, გრძელვადიანი მართვა ტიპიურად მოიცავს ანტითრომბოციტულ თერაპიას და რისკ-ფაქტორების აგრესიულ კონტროლს [1, 2]. გრძელვადიანი ანტიკოაგულაცია ზოგადად დაცულია პაციენტებისთვის თანმხლები ჩვენებით, როგორიცაა წინაგულების ფიბრილაცია; მისი რუტინული გამოყენება მხოლოდ ICA ოკლუზიისთვის არ არის მხარდაჭერილი ძლიერი მტკიცებულებებით [1, 2]. ქირურგიული ვარიანტები ICA ოკლუზიისთვის შეზღუდულია; ECA ენდარტერექტომია იშვიათად არის ნაჩვენები ინსულტის პრევენციისთვის და EC-IC შუნტირება არ არის ეფექტური ათეროსკლეროზული დაავადებისთვის (როგორც ადრე განვიხილეთ) [1, 13]. სავარაუდო მექანიზმის გამოკვლევამ (მაგ., დისტალური ემბოლია ნარჩენიდან vs. ჰემოდინამიკური კომპრომისი) შეიძლება გავლენა მოახდინოს მართვის ნიუანსებზე, მაგრამ ანტითრომბოციტული თერაპია რჩება ცენტრალური [1, 2].
სიმპტომატური ინტრაკრანიალური სტენოზის (მაგ., საძილე სიფონის ან MCA ღეროს სტენოზი) მართვა ასევე მოითხოვს სპეციფიკურ მიდგომას [1, 3]. SAMMPRIS-ის მსგავს კვლევებზე დაყრდნობით [3], აგრესიული სამედიცინო მართვა აღემატება სტენტირებას პაციენტების უმეტესობისთვის მნიშვნელოვანი სიმპტომატური ინტრაკრანიალური სტენოზით [3]. ეს სამედიცინო მართვა მოიცავს ორმაგ ანტითრომბოციტულ თერაპიას (DAPT - ტიპიურად ასპირინი და კლოპიდოგრელი) საწყისი პერიოდის განმავლობაში (მაგ., 90 დღე), რომელსაც მოსდევს ერთიანი ანტითრომბოციტული თერაპია გრძელვადიანად, არტერიული წნევის და ქოლესტერინის ინტენსიურ კონტროლთან ერთად [3]. გრძელვადიანი ანტიკოაგულაცია (ვარფარინი) ზოგადად *არ* არის რეკომენდებული ინტრაკრანიალური ათეროსკლეროზული სტენოზისთვის სისხლდენის გაზრდილი რისკისა და ანტითრომბოციტულ საშუალებებზე დადასტურებული უპირატესობის არარსებობის გამო [1, 3].
სისხლის სიბლანტის შემცირება (ჰემოდილუცია) არ არის სტანდარტული მწვავე ან ქრონიკული ინსულტის მკურნალობა; მიუხედავად იმისა, რომ თეორიულად მიმზიდველია, კვლევებმა არ აჩვენა თანმიმდევრული სარგებელი და ის ატარებს პოტენციურ რისკებს [1]. ანალოგიურად, აგენტები, როგორიცაა ოპიატური ანტაგონისტი ნალოქსონი, გამოკვლეულია მწვავე ინსულტის დროს, მაგრამ არ აღმოჩნდა ეფექტური და არ გამოიყენება სტანდარტულ პრაქტიკაში [1]. იშემიური პენუმბრას კონცეფცია (რისკის ქვეშ მყოფი ქსოვილი ბირთვის ინფარქტის გარშემო) ცენტრალურია ჰიპერმწვავე რეპერფუზიული თერაპიებისთვის (თრომბოლიზი, თრომბექტომია), რომელიც მიზნად ისახავს ამ ქსოვილის გადარჩენას შეუქცევადი ინფარქტის დადგომამდე[1, 14].
იშემიური მოვლენები, რომლებიც პირველ რიგში აზიანებს წინა ტვინის არტერიის (ACA) ტერიტორიას, ნაკლებად ხშირია, ვიდრე MCA ან უკანა მიმოქცევის ტერიტორიებზე [1]. მართვა ტიპიურად მიჰყვება იშემიური ინსულტის ზოგად პრინციპებს, მათ შორის ანტითრომბოციტულ თერაპიას და რისკ-ფაქტორების კონტროლს, გარდა იმ შემთხვევისა, როდესაც სპეციფიკური მაღალი რისკის წყარო (როგორიცაა კარდიოემბოლიზმი) არ კარნახობს ანტიკოაგულაციას [1, 2]. ქირურგიული ვარიანტები, რომლებიც კონკრეტულად მიმართულია ACA სტენოზზე, ზოგადად არ არის ხელმისაწვდომი ან ნაჩვენები [1].
ლიტერატურა
- Ropper AH, Samuels MA, Klein JP, Prasad S. Adams and Victor's Principles of Neurology. 11th ed. McGraw Hill; 2019. Chapter 34: Cerebrovascular Diseases.
- Kernan WN, Ovbiagele B, Black HR, et al; American Heart Association Stroke Council, Council on Cardiovascular and Stroke Nursing, Council on Clinical Cardiology, and Council on Peripheral Vascular Disease. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2014 Jul;45(7):2160-236. (Or more recent updates).
- Chimowitz MI, Lynn MJ, Derdeyn CP, et al; SAMMPRIS Trial Investigators. Stenting versus aggressive medical therapy for intracranial arterial stenosis. N Engl J Med. 2011 Sep 15;365(11):993-1003.
- Diener HC, Bogousslavsky J, Brass LM, et al; European Stroke Prevention Study 2. Aspirin and extended-release dipyridamole for prevention of ischemic stroke. N Engl J Med. 2006 Jun 8;354(23):2493-4; author reply 2494-5. (Example trial comparing antiplatelets).
- Johnston SC, Easton JD, Farrant M, et al; CHANCE Investigators. Clopidogrel and Aspirin in Acute Ischemic Stroke and High-Risk TIA. N Engl J Med. 2013 Jul 4;369(1):11-9. (Example DAPT trial).
- North American Symptomatic Carotid Endarterectomy Trial Collaborators. Beneficial effect of carotid endarterectomy in symptomatic patients with high-grade carotid stenosis. N Engl J Med. 1991 Aug 15;325(7):445-53.
- European Carotid Surgery Trialists' Collaborative Group. MRC European Carotid Surgery Trial: interim results for symptomatic patients with severe (70-99%) or with mild (0-29%) carotid stenosis. Lancet. 1991 May 25;337(8752):1235-43.
- Patrono C, García Rodríguez LA, Landolfi R, Baigent C. Low-dose aspirin for the prevention of atherothrombosis. N Engl J Med. 2005 Dec 1;353(22):2373-83. (Review on aspirin mechanism/dosing).
- Greenberg MS. Handbook of Neurosurgery. 9th ed. Thieme; 2019. Chapter 41: Carotid Endarterectomy.
- Brott TG, Halperin JL, Abbara S, et al. 2011 ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/SVM/SVS guideline on the management of patients with extracranial carotid and vertebral artery disease. Stroke. 2011 Aug;42(8):e464-540. (Covers CEA and CAS indications).
- Brott TG, Howard G, Roubin GS, et al; CREST Investigators. Long-Term Results of Stenting versus Endarterectomy for Carotid-Artery Stenosis. N Engl J Med. 2016 Mar 17;374(11):1021-31.
- Greenberg MS. Handbook of Neurosurgery. 9th ed. Thieme; 2019. Chapter 42: Extracranial-Intracranial Bypass.
- The EC/IC Bypass Study Group. Failure of extracranial-intracranial arterial bypass to reduce the risk of ischemic stroke. Results of an international randomized trial. N Engl J Med. 1985 Nov 7;313(19):1191-200.
- Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the Early Management of Patients With Acute Ischemic Stroke: 2019 Update to the 2018 Guidelines for the Early Management of Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2019 Dec;50(12):e344-e418.
- Goyal M, Menon BK, van Zwam WH, et al; HERMES collaborators. Endovascular thrombectomy after large-vessel ischaemic stroke: a meta-analysis of individual patient data from five randomised trials. Lancet. 2016 Apr 23;387(10029):1723-31.
იხილეთ აგრეთვე
- იშემიური ინსულტი, თავის ტვინის იშემია
- ვერტებრობაზილარული უკმარისობა (VBI) თავბრუსხვევის სიმპტომით
- სომატოფორმული ავტონომიური დისფუნქცია
- თავბრუსხვევა, ყურის დაგუბება და ტინიტუსი
- თავის ტვინის იშემიური დაავადება:
- ათეროსკლეროზული თრომბოზი
- შიდა საძილე არტერიის ათეროთრომბოზული ოკლუზია
- კაროტიდული ბიფურკაციის უსიმპტომო სტენოზი შუილით
- ვერტებრობაზილარული და ტვინის უკანა არტერიების ათეროთრომბოზული ოკლუზია
- ტვინის უკანა არტერიის ათეროთრომბოზული ოკლუზია
- ხერხემლისა და უკანა ქვედა ნათხემის არტერიების (PICA) ათეროთრომბოზული ოკლუზია
- ძირითადი არტერიის ათეროთრომბოზული ოკლუზია
- მცირე სისხლძარღვების ინსულტი (ლაკუნური ინფარქტი)
- იშემიური ინსულტის (ცერებრალური ინფარქტის) სხვა მიზეზები
- ცერებრალური ემბოლია
- სპონტანური ინტრაკრანიალური (სუბარაქნოიდული) და ინტრაცერებრული სისხლჩაქცევა:
- თავის ტვინის არტერიოვენოზური მალფორმაციები
- ჰიპერტენზიული ინტრაცერებრული სისხლჩაქცევა
- ცერებრალური არტერიების ანთებითი დაავადებები (ცერებრალური არტერიიტი)
- გიგანტური ინტრაკრანიალური ანევრიზმები
- ინტრაცერებრული სისხლჩაქცევის სხვა მიზეზები
- ლობარული ინტრაცერებრული სისხლჩაქცევა
- საკულარული ანევრიზმა და სუბარაქნოიდული სისხლჩაქცევა
- მიკოზური ინტრაკრანიალური ანევრიზმები
- ცერებრალური არტერიის ანევრიზმის განმეორებითი გასკდომა
- კომუნიკაციური ჰიდროცეფალია ინტრაცერებრული სისხლჩაქცევის შემდეგ გამსკდარი ანევრიზმით
- ცერებრალური ვაზოსპაზმი
- ცერებროვასკულური დაავადებები - იშემიური ინსულტი, ტრანზიტული იშემიური შეტევა (TIA):
- ტრანზიტული იშემიური შეტევა (TIA)
- სიგმოიდური სინუსის ჩირქოვანი თრომბოფლებიტი თრომბოზით