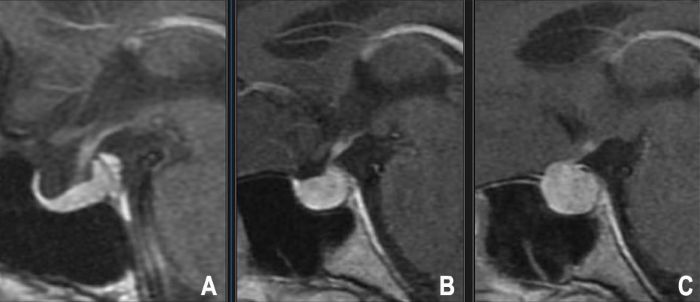
ჰიპოფიზის მიკროადენომა, მაკროადენომა და არაფუნქციონირებადი ადენომა (NFPAs), ჰიპერპროლაქტინემიის სინდრომი
- ჰიპოფიზის ადენომა (მიკროადენომა, მაკროადენომა), ჰიპერპროლაქტინემიის სინდრომის მიმოხილვა
- ჰიპოფიზის მიკროადენომები:
- ჰიპოფიზის მაკროადენომები:
- ჰიპოფიზის არაფუნქციონირებადი ადენომები (NFPAs)
- ჰიპოფიზის ადენომისა და ჰიპერპროლაქტინემიის სინდრომის დიაგნოსტიკა
- ჰიპოფიზის ადენომისა და ჰიპერპროლაქტინემიის სინდრომის მკურნალობა
- ჰიპოფიზის არაფუნქციონირებადი ადენომების (NFPAs) მკურნალობა
- ლიტერატურა
ჰიპოფიზის ადენომა (მიკროადენომა, მაკროადენომა), ჰიპერპროლაქტინემიის სინდრომის მიმოხილვა
ჰიპოფიზის ადენომები, როგორც წესი, კეთილთვისებიანი (არასიმსივნური) სიმსივნეებია, რომლებიც წარმოიქმნება წინა ჰიპოფიზის ჯირკვლის (ადენოჰიპოფიზი) ჰორმონის მწარმოებელი უჯრედებიდან, რომელიც მდებარეობს ტვინის ფუძეზე ძვლოვან სტრუქტურაში, რომელსაც ეწოდება თურქული კეხი [1]. ეს ადენომები კლასიფიცირდება ზომის (მიკროადენომა მაკროადენომას წინააღმდეგ) და ჰორმონალური აქტივობის (ფუნქციონირებადი არაფუნქციონირებადის წინააღმდეგ) საფუძველზე.
ჰიპერპროლაქტინემიის სინდრომი გულისხმობს პროლაქტინის, ჰორმონის, რომელიც ჩვეულებრივ მონაწილეობს ლაქტაციაში, მუდმივად მომატებული დონის კლინიკურ შედეგებს. პროლაქტინომები (პროლაქტინის გამომყოფი ჰიპოფიზის ადენომები) ფუნქციონირებადი ჰიპოფიზის ადენომის ყველაზე გავრცელებული ტიპია და ჰიპერპროლაქტინემიის ხშირი მიზეზია [2]. ქალებში სიმპტომები, როგორც წესი, მოიცავს გალაქტორეას (რძის შეუსაბამო წარმოქმნა), მენსტრუალურ დარღვევებს (ოლიგომენორეა ან ამენორეა) და უნაყოფობას. მამაკაცებში ჰიპერპროლაქტინემია ხშირად იწვევს ლიბიდოს დაქვეითებას, ერექციულ დისფუნქციას, უნაყოფობას ოლიგოსპერმიის გამო, გინეკომასტიას (მკერდის გადიდება) და ნაკლებად ხშირად, გალაქტორეას. მომატებული პროლაქტინი აფერხებს გონადოტროპინის რილიზინგ ჰორმონის (GnRH) სეკრეციას ჰიპოთალამუსიდან, რაც იწვევს მეორად ჰიპოგონადიზმს.
ჰიპოფიზის ადენომებთან დაკავშირებული სიმპტომები წარმოიქმნება ან ჭარბი ჰორმონის სეკრეციის შედეგად (ფუნქციონირებად ადენომებში) ან სიმსივნის ფიზიკური ზომისა და მიმდებარე სტრუქტურებზე ზეწოლის შედეგად (მასის ეფექტი), განსაკუთრებით მაკროადენომების დროს. ჰორმონის სიჭარბის სინდრომები მოიცავს:
ჭარბი ჰორმონი |
შედეგად გამოწვეული მდგომარეობა და ძირითადი ჯანმრთელობის პრობლემები |
|---|---|
| პროლაქტინი (PRL) |
ჰიპერპროლაქტინემია: - ქალები: მენსტრუალური დისფუნქცია (ოლიგომენორეა, ამენორეა), გალაქტორეა, უნაყოფობა, ძვლის სიმკვრივის დაქვეითება. - მამაკაცები: ლიბიდოს დაქვეითება, ერექციული დისფუნქცია, უნაყოფობა, გინეკომასტია (ნაკლებად გავრცელებული), ძვლის სიმკვრივის დაქვეითება. [2] |
| ზრდის ჰორმონი (GH) |
აკრომეგალია (მოზრდილები) / გიგანტიზმი (ბავშვები): - ხელების, ფეხების, სახის ნაკვთების გადიდება (ყბა, წარბი). - რბილი ქსოვილების შეშუპება, ჭარბი ოფლიანობა. - ოსტეოართრიტი, მაჯის გვირაბის სინდრომი. - ძილის აპნოე. - ჰიპერტენზია, კარდიომიოპათია. - შაქრიანი დიაბეტი ან გლუკოზისადმი ტოლერანტობის დარღვევა. - კოლორექტალური პოლიპების/კიბოს გაზრდილი რისკი. [3] |
| ადრენოკორტიკოტროპული ჰორმონი (ACTH) |
კუშინგის დაავადება (ჰიპოფიზზე დამოკიდებული კუშინგის სინდრომი): - ცენტრალური სიმსუქნე (ღეროს ცხიმი, მთვარისებრი სახე, კამეჩის კუზი), თხელი კანი, ადვილად დალურჯება, იისფერი სტრიები. - კუნთების სისუსტე (პროქსიმალური მიოპათია), ოსტეოპოროზი. - განწყობის ცვლილებები (შფოთვა, დეპრესია, ფსიქოზი). - ჰიპერტენზია, შაქრიანი დიაბეტი. - ინფექციებისადმი გაზრდილი მგრძნობელობა. - მენსტრუალური დარღვევები (ქალები). [4] |
| თირეოტროპული ჰორმონი (TSH) |
TSH-ომა (იშვიათი): - მეორადი ჰიპერთირეოზი: სიმპტომები მოიცავს სიცხის აუტანლობას, ოფლიანობას, ტაქიკარდიას/გულისცემის შეგრძნებას (არითმიები, როგორიცაა წინაგულების ფიბრილაცია), ტრემორს, შფოთვას/გაღიზიანებადობას, წონის უნებლიე კლებას მადის მატების მიუხედავად, ჩიყვს. ხასიათდება შეუსაბამოდ ნორმალური ან მომატებული TSH-ით მომატებული თავისუფალი T4/T3 დონეებით. [5] |
| გონადოტროპინები (LH, FSH) |
გონადოტროფული ადენომა (ხშირად კლინიკურად არაფუნქციონირებადი): - ჩვეულებრივ გამოყოფენ არააქტიურ ან ხელუხლებელ ჰორმონის ფრაგმენტებს (მაგ., ალფა-ქვეერთეული, ბეტა-FSH, ნაკლებად ხშირად ხელუხლებელი FSH/LH). - შეიძლება იშვიათად გამოიწვიოს საკვერცხეების ჰიპერსტიმულაცია (ქალები) ან სათესლე ჯირკვლის გადიდება/ნაადრევი სქესობრივი მომწიფება (მამაკაცები). - ყველაზე ხშირად ვლინდება მასის ეფექტის გამო ან შემთხვევით აღმოჩნდება. [6] |
ჰიპოფიზის არაფუნქციონირებადი ადენომები (NFPAs) არ გამოყოფენ აქტიური ჰორმონების კლინიკურად მნიშვნელოვან რაოდენობას, თუმცა ბევრი აწარმოებს ჰორმონის ქვეერთეულებს, რომლებიც აღმოჩენადია სპეციალური ტესტებით. ისინი, როგორც წესი, იწვევენ სიმპტომებს მასის ეფექტის გამო, როდესაც ისინი ხდებიან მაკროადენომები, აკომპრესირებენ მიმდებარე სტრუქტურებს, როგორიცაა მხედველობის ჯვარედინი (იწვევს მხედველობის ველის დეფექტებს, კლასიკურად ბიტემპორალურ ჰემიანოფსიას), კრანიალურ ნერვებს კავერნოზულ სინუსში (იწვევს ორმაგ მხედველობას) ან ნორმალურ ჰიპოფიზის ქსოვილს (იწვევს ჰიპოპიტუიტარიზმს - ერთი ან მეტი ჰიპოფიზის ჰორმონის დეფიციტს). თავის ტკივილი ასევე ხშირია მაგარი გარსის დაჭიმვის ან თურქულ კეხში წნევის გაზრდის გამო.
ჰიპოფიზის მიკროადენომები
ჰიპოფიზის მიკროადენომების აღწერა
ჰიპოფიზის მიკროადენომა განიმარტება როგორც ჰიპოფიზის ადენომა მაქსიმალური დიამეტრით 10 მილიმეტრზე ნაკლები (1 სმ-ზე ნაკლები)[7]. ეს სიმსივნეები შემოფარგლულია თურქული კეხის შიგნით და, როგორც წესი, არ იწვევს მასის ეფექტის სიმპტომებს, როგორიცაა მხედველობის დაკარგვა. მიკროადენომები შეიძლება იყოს როგორც ფუნქციონირებადი (ჰორმონის გამომყოფი), ასევე არაფუნქციონირებადი. ფუნქციონირებადი მიკროადენომები იწვევენ სიმპტომებს, რომლებიც დაკავშირებულია სპეციფიკურ ჰორმონთან, რომელსაც ისინი ჭარბად აწარმოებენ (მაგ., პროლაქტინომა, რომელიც იწვევს ჰიპერპროლაქტინემიას, ACTH-სეკრეტორული, რომელიც იწვევს კუშინგის დაავადებას, GH-სეკრეტორული, რომელიც იწვევს აკრომეგალიას).
თუმცა, ბევრი მიკროადენომა კლინიკურად არაფუნქციონირებადია და შემთხვევით აღმოჩნდება სხვა მიზეზების გამო (მაგ., თავის ტკივილი, თავბრუსხვევა, ტრავმა) ჩატარებული ტვინის ვიზუალიზაციისას (მაგნიტურ-რეზონანსული ტომოგრაფია - მრტ ან კტ). მათ ხშირად მოიხსენიებენ როგორც ჰიპოფიზის "ინციდენტალომებს". მიუხედავად იმისა, რომ უმრავლესობა არის კეთილთვისებიანი აღმოჩენა, რომელიც მოითხოვს მხოლოდ მონიტორინგს, ზოგჯერ მცირე შემთხვევითმა მიკროადენომებმაც კი შეიძლება გამოიწვიოს დახვეწილი ჰორმონალური დისბალანსი (სუბკლინიკური კუშინგი, მსუბუქი ჰიპერპროლაქტინემია) ან, იშვიათად (რამდენიმე წლის განმავლობაში < 10%), გაიზარდოს დროთა განმავლობაში [8].
მრტ გადოლინიუმის კონტრასტით, განსაკუთრებით დინამიური კონტრასტით გაძლიერებული მიმდევრობების გამოყენებით და ჰიპოფიზის ფოსოს თხელი ჭრილებით, არის არჩევითი ვიზუალიზაციის მოდალობა მიკროადენომების გამოსავლენად. ისინი ხშირად ჩნდებიან როგორც მცირე, კეროვანი დაზიანებები, რომლებიც ნაკლებად ძლიერად ან უფრო გვიან კონტრასტდებიან, ვიდრე მიმდებარე ნორმალური ჰიპოფიზის ჯირკვლის ქსოვილი (ტიპიურად ჰიპოინტენსიურია ადრეულ პოსტ-კონტრასტულ T1 გამოსახულებებზე) [9].
კლინიკურად მნიშვნელოვანი მიკროადენომები ყველაზე ხშირად პროლაქტინომებია, რასაც მოჰყვება ACTH-სეკრეტორული ადენომები, რომლებიც იწვევენ კუშინგის დაავადებას, და GH-სეკრეტორული ადენომები, რომლებიც იწვევენ აკრომეგალიას. არაფუნქციონირებადი მიკროადენომები ხშირად არის გონადოტროფული ადენომები იმუნოჰისტოქიმიით, მაგრამ არ აქვთ კლინიკური ჰორმონის სიჭარბე. დიფერენციალური დიაგნოზი ვიზუალიზაციაზე მოიცავს რატკეს ჯიბის კისტებს, ჰიპოფიზის ჰიპერპლაზიას, მეტასტაზებს ან ანთებით პროცესებს (ჰიპოფიზიტი), თუმცა მათ ხშირად აქვთ განსხვავებული მახასიათებლები ან კლინიკური კონტექსტი.
ჰიპოფიზის მიკროადენომების პათოფიზიოლოგია
ჰიპოფიზის ადენომები, მიკროადენომების ჩათვლით, ზოგადად განიხილება როგორც მონოკლონური ნეოპლაზმები, რაც ნიშნავს, რომ ისინი წარმოიქმნება ერთი მუტირებული წინა ჰიპოფიზის უჯრედის კლონური გაფართოებისგან [10]. სპეციფიკური მაინიცირებელი მუტაციები და შემდგომი გენეტიკური/ეპიგენეტიკური მოვლენები, რომლებიც იწვევს ადენომის ფორმირებას, რთული და მრავალფეროვანია, მაგრამ რამდენიმე ფაქტორი და გზა არის ჩართული.
სპეციფიკური გერმინაციული გენეტიკური სინდრომები განაპირობებს ინდივიდების მიდრეკილებას ჰიპოფიზის ადენომებისადმი: მრავლობითი ენდოკრინული ნეოპლაზიის 1 ტიპი (MEN1), გამოწვეული მუტაციებით MEN1 სიმსივნის სუპრესორულ გენში, ხშირად მოიცავს პროლაქტინომებს ან GH-სეკრეტორულ ადენომებს. მაკკიუნ-ოლბრაითის სინდრომი, მოზაიკური მააქტივირებელი მუტაციების გამო GNAS გენში, რომელიც აკოდირებს Gs-ალფა ცილის ქვეერთეულს, ხშირად იწვევს GH-სეკრეტორულ ადენომებს (სომატოტროპინომები). კერნის კომპლექსი (PRKAR1A მუტაციები) შეიძლება მოიცავდეს ჰიპოფიზის ადენომებს (ჩვეულებრივ GH-სეკრეტორული). მუტაციები AIP (არილის ნახშირწყალბადის რეცეპტორთან ურთიერთქმედების პროტეინი) გენში განაპირობებს ოჯახურ იზოლირებულ ჰიპოფიზის ადენომებს (FIPA), განსაკუთრებით GH-სეკრეტორულ ან პროლაქტინ-სეკრეტორულ სიმსივნეებს, რომლებიც ხშირად ვლინდება ახალგაზრდა ასაკში და არის უფრო დიდი/აგრესიული [11].
სპორადული (არაოჯახური) ადენომები ასევე მოიცავს სომატურ გენეტიკურ და ეპიგენეტიკურ ცვლილებებს. გამააქტიურებელი სომატური მუტაციები GNAS-ში გვხვდება სპორადული GH-სეკრეტორული ადენომების დაახლოებით 40 პროცენტში. USP8-ის მუტაციები ხშირია ACTH-სეკრეტორულ ადენომებში [12]. სხვა სომატური მუტაციები და ეპიგენეტიკური ცვლილებები, რომლებიც გავლენას ახდენენ უჯრედული ციკლის რეგულატორებზე (მაგ., CDKN1B/p27-ის ფუნქციის დაკარგვა, p53-ის, RB გზების ცვლილებები), ზრდის ფაქტორის გზებზე (მაგ., FGFR4-ის ზედმეტი ექსპრესია) და ჰიპოფიზის სპეციფიკურ ტრანსკრიფციის ფაქტორებზე, ხელს უწყობს სიმსივნის ფორმირებას და ჰორმონების გამომუშავებას. ასევე შეინიშნება ჰეტეროზიგოტურობის დაკარგვა გარკვეულ ქრომოსომულ ლოკაციებზე (მაგ., 11q13, სადაც მდებარეობს MEN1).
პროლაქტინომები, ყველაზე გავრცელებული ტიპი, წარმოიქმნება ლაქტოტროფული უჯრედებიდან. კორტიკოტროპინომები, რომლებიც იწვევენ კუშინგის დაავადებას, წარმოიქმნება კორტიკოტროფული უჯრედებიდან. სომატოტროპინომები, რომლებიც იწვევენ აკრომეგალიას, წარმოიქმნება სომატოტროფული უჯრედებიდან. გონადოტროპინომები, როგორც წესი, წარმოიქმნება გონადოტროფული უჯრედებიდან და ხშირად გამოყოფენ არააქტიურ ჰორმონის ქვეერთეულებს (ალფა-ქვეერთეული, ბეტა-FSH, ბეტა-LH). თირეოტროპინომები, რომლებიც იწვევენ ჰიპერთირეოზს, წარმოიქმნება თირეოტროფული უჯრედებიდან და იშვიათია.
კლინიკურად არაფუნქციონირებადი ადენომების უმეტესობა იმუნოპოზიტიურია გონადოტროპინის ქვეერთეულებისთვის (FSH, LH, ალფა-ქვეერთეული), მაგრამ არ იწვევს ჰორმონის სიჭარბის კლინიკურ სინდრომებს. ზოგიერთი შეიძლება იყოს "ნულოვანი უჯრედის" ადენომა სპეციფიკური ჰორმონის შეღებვის გარეშე, ან ჩუმი კორტიკოტროფული/სომატოტროფული ადენომა.
ჰიპოფიზის მიკროადენომების ეპიდემიოლოგია
ჰიპოფიზის მიკროადენომების სიხშირე
ჰიპოფიზის მიკროადენომები საოცრად გავრცელებული შემთხვევითი აღმოჩენებია. აუტოფსიის კვლევებმა აჩვენა მიკროსკოპული ან მცირე ადენომები (ხშირად < 3 მმ) იმ პირთა 27 პროცენტში, რომლებსაც არ ჰქონდათ ჰიპოფიზის ცნობილი დაავადება [13, 14]. მაღალი რეზოლუციის ვიზუალიზაციის კვლევები (მრტ) ავლენს ჰიპოფიზის ინციდენტალომებს (რომელთა უმეტესობა არის მიკროადენომები < 10 მმ) ზოგადი პოპულაციის დაახლოებით 10-20 პროცენტში, რომლებსაც უტარდებათ ტვინის სკანირება სხვა მიზეზების გამო [15].
ამ შემთხვევით აღმოჩენილი მიკროადენომების აბსოლუტური უმრავლესობა არაფუნქციონირებადია და რჩება სტაბილური ან იზრდება ძალიან ნელა, არასოდეს იწვევს კლინიკურ სიმპტომებს. ფუნქციონირებადი მიკროადენომები გაცილებით ნაკლებად გავრცელებულია, მაგრამ არის ჰიპოფიზის ჰორმონის სიჭარბის სინდრომების ჩვეულებრივი მიზეზი, როგორიცაა ჰიპერპროლაქტინემია (პროლაქტინომა არის ყველაზე ხშირი კლინიკურად დიაგნოზირებული ტიპი, სავარაუდო გავრცელება ~10-50 100,000 მოსახლეზე [16]), კუშინგის დაავადება და აკრომეგალია.
ჰიპოფიზის მიკროადენომები შეიძლება გამოვლინდეს ნებისმიერ ასაკში, მაგრამ ყველაზე ხშირად დიაგნოზირებულია ახალგაზრდა და შუა ხნის მოზრდილებში (20-დან 50 წლამდე). ქალების ჭარბობაა პროლაქტინომების (ქ:მ თანაფარდობა ~10:1) და კუშინგის დაავადების დროს (~3-5:1), ხოლო GH-სეკრეტორულ ადენომებს აქვთ უხეშად თანაბარი გენდერული განაწილება.
მრტ-ს ფართოდ გამოყენებამდე, სისხლის ანალიზით გამოვლენილი ჰიპერპროლაქტინემია იყო მთავარი გასაღები ძირითადი, ხშირად უხილავი, პროლაქტინის გამომყოფი მიკროადენომების. მრტ ახლა იძლევა პირდაპირი ვიზუალიზაციის საშუალებას.
შემთხვევით აღმოჩენილი მიკროადენომების მაღალი გავრცელება კლინიკურად მნიშვნელოვანი ჰიპოფიზის დაავადების ან მაკროადენომების დაბალ გავრცელებასთან შედარებით იმაზე მეტყველებს, რომ მიკროადენომების უმეტესობა არ პროგრესირებს, რათა გახდეს დიდი ან სიმპტომური სიმსივნეები.
ჰიპოფიზის მაკროადენომები
ჰიპოფიზის მაკროადენომების აღწერა
ჰიპოფიზის მაკროადენომა განისაზღვრება, როგორც ჰიპოფიზის ადენომა, რომლის მაქსიმალური დიამეტრი არის 10 მილიმეტრი (1 სმ) ან მეტი [3]. მიკროადენომებისგან განსხვავებით, მაკროადენომები ხშირად ვრცელდება თურქული კეხის საზღვრებს გარეთ, რაც პოტენციურად აკომპრესირებს მიმდებარე ნერვულ და სისხლძარღვოვან სტრუქტურებს.
ისინი შეიძლება იყოს როგორც ფუნქციონირებადი (ჰორმონის გამომყოფი), ასევე არაფუნქციონირებადი. არაფუნქციონირებადი ჰიპოფიზის ადენომები (NFPAs) არის მაკროადენომის ყველაზე გავრცელებული ტიპი, რომელიც კლინიკურად დიაგნოზირებულია [6]. ფუნქციონირებადი მაკროადენომები მოიცავს დიდ პროლაქტინომებს, GH-სეკრეტორულ ადენომებს, რომლებიც იწვევენ აკრომეგალიას და ნაკლებად ხშირად, დიდ ACTH-სეკრეტორულ ადენომებს (ხშირად ასოცირდება ნელსონის სინდრომთან ადრენალექტომიის შემდეგ) ან TSH-სეკრეტორულ ადენომებს.
მაკროადენომები ხშირად ვლინდება სიმპტომებით, რომლებიც დაკავშირებულია მასის ეფექტთან მათი ზომის გამო:
- მხედველობის დარღვევები: ჰიპოფიზის ზემოთ მდებარე მხედველობის ჯვარედინის კომპრესია ხშირია სუპრასელარული გაფართოებით, კლასიკურად იწვევს ბიტემპორალურ ჰემიანოფსიას (პერიფერიული მხედველობის დაკარგვა ორივე გარე საფეთქლის ველში). მხედველობის ნერვების ან ტრაქტების კომპრესიამ შეიძლება გამოიწვიოს მხედველობის დაკარგვის სხვა პატერნები ან მხედველობის სიმახვილის დაქვეითება.
- კრანიალური ნერვების დამბლა: გვერდითმა გაფართოებამ კავერნოზულ სინუსში შეიძლება შეკუმშოს კრანიალური ნერვები III (თვალის მამოძრავებელი), IV (ჭაღისებრი), V (სამწვერა - V1 ოფთალმოლოგიური და V2 ზედა ყბის ტოტები) და VI (განმზიდველი), რაც იწვევს ორმაგ მხედველობას (დიპლოპია), ქუთუთოს დავარდნას (პტოზი), გუგის ცვლილებებს ან სახის დაბუჟებას/ტკივილს. CN III და VI ყველაზე ხშირად ზიანდება კლინიკურად.
- თავის ტკივილი: ხშირად არასპეციფიკურია, პოტენციურად გამოწვეულია მაგარი გარსის დაჭიმვით, რომელიც ფარავს კეხს (diaphragma sellae) ან გაზრდილი ინტრასელარული წნევით.
- ჰიპოპიტუიტარიზმი: ნორმალური ჰიპოფიზის ქსოვილის კომპრესიამ და დესტრუქციამ შეიძლება გამოიწვიოს ერთი ან მეტი წინა ჰიპოფიზის ჰორმონის დეფიციტი (GH დეფიციტი ხშირად ყველაზე ადრეა, რასაც მოჰყვება გონადოტროპინები LH/FSH, რაც იწვევს ჰიპოგონადიზმს, შემდეგ TSH, რაც იწვევს მეორად ჰიპოთირეოზს და ბოლოს ACTH, რაც იწვევს მეორად თირკმელზედა ჯირკვლის უკმარისობას) ან, ნაკლებად ხშირად, უკანა ჰიპოფიზის დისფუნქციას (ანტიდიურეზული ჰორმონის - ADH დეფიციტი, რომელიც იწვევს ცენტრალურ უშაქრო დიაბეტს, უფრო ხშირად გვხვდება ღეროს კომპრესიით ან უკან წარმოშობილი დაზიანებებით).
- ჰიპოფიზის აპოპლექსია: მწვავე სამედიცინო გადაუდებელი მდგომარეობა, რომელიც გამოწვეულია უეცარი სისხლჩაქცევით ან ინფარქტით ჰიპოფიზის ადენომის შიგნით (გაცილებით ხშირია მაკროადენომებში, ვიდრე მიკროადენომებში). ვლინდება უეცარი ძლიერი თავის ტკივილით, მხედველობის სწრაფი დაკარგვით, კრანიალური ნერვების დამბლით, შეცვლილი ცნობიერებით და ხშირად მწვავე ჰიპოპიტუიტარიზმით (მოითხოვს სტეროიდების გადაუდებელ ჩანაცვლებას).
ფუნქციონირებადი მაკროადენომები ასევე იწვევს სიმპტომებს, რომლებიც დაკავშირებულია ჰორმონების ჭარბწარმოებასთან, ხშირად უფრო მძიმე ვიდრე მიკროადენომების შემთხვევაში სიმსივნის დიდი მოცულობის გამო, როგორც ადრე იყო აღწერილი.
ჰიპოფიზის მაკროადენომების პათოფიზიოლოგია
ძირითადი პათოფიზიოლოგია მოიცავს მუტირებული ადენოჰიპოფიზური უჯრედების კლონურ გაფართოებას, მიკროადენომების მსგავსად. ფაქტორები, რომლებიც განაპირობებენ მიკროადენომიდან მაკროადენომაზე პროგრესირებას ან მაკროადენომების დე ნოვო განვითარებას, ბოლომდე არ არის განმარტებული, მაგრამ სავარაუდოდ მოიცავს დამატებითი გენეტიკური (მაგ., მუტაციები სიმსივნის სუპრესორულ გენებში, როგორიცაა p53, ქრომოსომული არასტაბილურობა) ან ეპიგენეტიკური ცვლილებების დაგროვებას, რომლებიც ხელს უწყობენ გაზრდილ პროლიფერაციას, შემცირებულ აპოპტოზს, ანგიოგენეზს და ზოგჯერ ინვაზიურობას [10].
მაკროადენომები ხშირად ავლენენ ჰორმონის სეკრეციის მაკონტროლებელი ნორმალური უკუკავშირის მექანიზმების დაკარგვას (განსაკუთრებით ფუნქციონირებადი). მათი ზრდა იწვევს მიმდებარე ნორმალური ჰიპოფიზის უჯრედების კომპრესიას და განადგურებას, რაც იწვევს ჰიპოპიტუიტარიზმს. ზემოთ გაფართოება აკომპრესირებს მხედველობის ჯვარედინს და პოტენციურად ჰიპოთალამუსს (რაც იწვევს უშაქრო დიაბეტს ან მადის/ტემპერატურის დისრეგულაციას). ლატერალური გაფართოება იჭრება კავერნოზულ სინუსში, პოტენციურად ფარავს შიდა საძილე არტერიას და კრანიალურ ნერვებს III, IV, V1, V2 და VI. ქვედა გაფართოებამ შეიძლება გაანადგუროს თურქული კეხის ფსკერი სფენოიდულ სინუსში, რაც ზოგჯერ იწვევს CSF რინორეას.
გენეტიკური საფუძველი მოიცავს მიკროადენომებისთვის ნახსენებ ფაქტორებს, მათ შორის გერმინაციულ სინდრომებს (MEN1, GNAS, AIP, კერნის კომპლექსი) და სომატურ მუტაციებს (GNAS, USP8). დამატებითი ცვლილებები, რომლებიც დაკავშირებულია უფრო დიდ ან უფრო აგრესიულ სიმსივნეებთან, შეიძლება მოიცავდეს უჯრედული ციკლის რეგულატორების (p53, RB), ზრდის ფაქტორის რეცეპტორების (FGFR4) ან ადჰეზიური მოლეკულების მუტაციებს. მიუხედავად იმისა, რომ ჰისტოლოგიურად კეთილთვისებიანია (მიტოზური მაჩვენებელი დაბალია, ციტოლოგიური ატიპია ჩვეულებრივ არ არის), ზოგიერთი მაკროადენომა ავლენს ინვაზიური ზრდის პატერნებს მიმდებარე სტრუქტურებში (მაგარი გარსი, ძვალი, კავერნოზული სინუსი), რაც ართულებს სრულ ქირურგიულ რეზექციას. ნამდვილი პირველადი ჰიპოფიზის კარცინომები, რომლებიც განისაზღვრება კრანიოსპინალური ან სისტემური მეტასტაზების არსებობით, ძალზე იშვიათია.
ასოცირებული კლინიკური სინდრომები, როგორიცაა MEN1, McCune-Albright და Carney-ის კომპლექსი, შეიძლება მოიცავდეს მაკროადენომებს, ხშირად GH-სეკრეტორულს ან პროლაქტინ-სეკრეტორულს.
ჰიპოფიზის მაკროადენომების ეპიდემიოლოგია
ჰიპოფიზის მაკროადენომების სიხშირე
მიუხედავად იმისა, რომ შემთხვევითი მიკროადენომები ძალიან ხშირია, კლინიკურად მნიშვნელოვანი ჰიპოფიზის სიმსივნეები, რომლებიც საჭიროებენ შეფასებას და პოტენციურ მკურნალობას, ნაკლებად ხშირია. კლინიკურად აშკარა ჰიპოფიზის ადენომების საერთო პრევალენტობა შეფასებულია დაახლოებით 78-94-ად 100,000 ინდივიდზე, ან დაახლოებით 1-ად 1000-ში[17, 18]. მაკროადენომები წარმოადგენენ ამ კლინიკურად რელევანტური სიმსივნეების მნიშვნელოვან პროპორციას, რაც სავარაუდოდ წარმოადგენს დიაგნოსტირებული ადენომების 30-50%-ს, განსაკუთრებით არაფუნქციონირებად ადენომებს შორის, რომლებიც ხშირად ვლინდება ზომის გამო.
მოსახლეობაზე დაფუძნებული კვლევები ვარაუდობენ ახლად დიაგნოზირებული ჰიპოფიზის ადენომების საერთო წლიურ სიხშირეს დაახლოებით 4-ს 100,000 მოსახლეზე[18], პრევალენტობის მაჩვენებლები იზრდება ვიზუალიზაციით გაუმჯობესებული აღმოჩენის გამო. შემთხვევები, რომლებიც საჭიროებენ ნეიროქირურგიულ ჩარევას, მერყეობს დაახლოებით 1-დან 7-მდე 100,000-ზე წელიწადში, სადაც მაკროადენომები, რომლებიც იწვევენ მასის ეფექტს ან ჰორმონის სიჭარბეს, რომელიც რეფრაქტერულია სამედიცინო თერაპიის მიმართ, არის ოპერაციის პირველადი ჩვენება.
ავადობა და სიკვდილიანობა ჰიპოფიზის მაკროადენომების დროს
ჰიპოფიზის მაკროადენომებთან დაკავშირებული ავადობა ძირითადად გამომდინარეობს მასის ეფექტებიდან (მხედველობის დაკარგვა, კრანიალური ნერვის დამბლა, დამამშვიდებელი თავის ტკივილი), ჰორმონალური დისფუნქციიდან (ჰიპოპიტუიტარიზმი, რომელიც მოითხოვს მთელი ცხოვრების განმავლობაში ჩანაცვლებას, ან ჰორმონის სიჭარბის სინდრომების სისტემური შედეგები, როგორიცაა აკრომეგალია ან კუშინგის დაავადება) და მკურნალობის პოტენციური გართულებებიდან (მაგ., ქირურგიული რისკები, როგორიცაა CSF გაჟონვა, მენინგიტი, სისხლძარღვოვანი დაზიანება, ჰიპოპიტუიტარიზმის გაუარესება; რადიაციის გრძელვადიანი ეფექტები, როგორიცაა ჰიპოპიტუიტარიზმი, მეორადი სიმსივნეები, კოგნიტური ცვლილებები). მხედველობის დაქვეითება, განსაკუთრებით მუდმივი დეფიციტი ქიაზმური კომპრესიის დაგვიანებული მკურნალობის შედეგად, მნიშვნელოვან გავლენას ახდენს ცხოვრების ხარისხზე. ჰიპოპიტუიტარიზმი მოითხოვს ფრთხილ მართვას და ატარებს საკუთარ რისკებს, თუ არაადეკვატურად განიკურნება (მაგ., თირკმელზედა ჯირკვლის კრიზი). უკონტროლო ჰორმონის სიჭარბის გართულებები (მაგ., გულ-სისხლძარღვთა დაავადება, დიაბეტი, ოსტეოპოროზი, კიბოს გაზრდილი რისკი აკრომეგალიისა და კუშინგის დროს) მნიშვნელოვან წვლილს შეიტანს გრძელვადიან ავადობასა და სიკვდილიანობაში, თუ ეფექტურად არ იმართება [19, 20].
უშუალოდ ჰიპოფიზის მაკროადენომების კეთილთვისებიან ბუნებასთან დაკავშირებული სიკვდილიანობა ზოგადად დაბალია. თუმცა, სიკვდილიანობის გაზრდილი რისკი კარგად არის დოკუმენტირებული პაციენტებში უკონტროლო აკრომეგალიით და კუშინგის დაავადებით, პირველ რიგში გულ-სისხლძარღვთა გართულებების (ჰიპერტენზია, გულის უკმარისობა, ინსულტი, არითმიები), მეტაბოლური პრობლემების (დიაბეტი) და ინფექციების (კუშინგი) გამო. ჰიპოფიზის აპოპლექსია, თუმცა იშვიათია, შეიძლება ფატალური იყოს, თუ დროულად არ იქნა აღიარებული და ნამკურნალები. ქირურგიის გართულებებმა (თუმცა სიკვდილიანობა დაბალია, <1%, გამოცდილ ცენტრებში) ან სხივური თერაპიის გრძელვადიანმა ეფექტებმა ასევე შეიძლება ხელი შეუწყოს ამას. მაკროადენომების მქონე პაციენტების საერთო გადარჩენა ზოგადად კარგია თანამედროვე მულტიდისციპლინარული მართვით, რომელიც აკონტროლებს ჰორმონების დონეს და მასის ეფექტს, თუმცა ცხოვრების ხარისხზე შეიძლება გავლენა იქონიოს ნარჩენმა სიმპტომებმა ან მკურნალობის გვერდითმა ეფექტებმა.
ჰიპოფიზის მაკროადენომები არ ავლენენ მნიშვნელოვან რასობრივ მიდრეკილებას.
მიუხედავად იმისა, რომ აუტოფსიის კვლევები აჩვენებს შემთხვევითი ადენომების თანაბარ გავრცელებას სქესებს შორის, კლინიკურად დიაგნოზირებული პროლაქტინომები და ACTH-სეკრეტორული ადენომები (კუშინგის დაავადება) მნიშვნელოვნად უფრო ხშირია რეპროდუქციული ასაკის ქალებში, შესაძლოა სიმპტომების უფრო ადრეული ამოცნობის გამო (მენსტრუალური დარღვევები, გალაქტორეა). GH-სეკრეტორულ ადენომებს (აკრომეგალია) და კლინიკურად გამოვლენილ NFPA-ებს უფრო თანაბარი გენდერული განაწილება აქვთ. ჰიპოფიზის მაკროადენომები შეიძლება გამოვლინდეს ნებისმიერ ასაკში, მაგრამ ყველაზე ხშირად დიაგნოზირებულია მოზრდილებში, სიხშირის პიკით მესამედან მეექვსე დეკადამდე.
ჰიპოფიზის არაფუნქციონირებადი ადენომები (NFPAs)
ჰიპოფიზის არაფუნქციონირებადი ადენომები (NFPAs) არის ჰიპოფიზის სიმსივნეები, რომლებიც არ იწვევენ ჰორმონის ჭარბი სეკრეციის კლინიკურ სინდრომს. ისინი წარმოადგენენ კლინიკურად დიაგნოზირებული ჰიპოფიზის ყველა ადენომის დაახლოებით 15-30 პროცენტს და არიან მაკროადენომების ყველაზე გავრცელებული ტიპი [22]. მიუხედავად იმისა, რომ ეწოდება "არაფუნქციონირებადი", იმუნოჰისტოქიმიური შეღებვა ავლენს, რომ NFPA-ების უმეტესობა წარმოიქმნება გონადოტროფული უჯრედებიდან და ხშირად აწარმოებს გონადოტროპინის ჰორმონებს (ფოლიკულომასტიმულირებელი ჰორმონი - FSH, მალუტეინიზებელი ჰორმონი - LH) ან მათ ქვეერთეულებს (განსაკუთრებით ალფა-ქვეერთეული ან FSH-ბეტა ქვეერთეული), მაგრამ ეს ჰორმონები, როგორც წესი, ბიოლოგიურად არააქტიურია, გამოიყოფა არაეფექტურად ან გამოიყოფა არანორმალური თანაფარდობით, რითაც არ იწვევს ჰორმონის სიჭარბის კლინიკურ სიმპტომებს [6]. ზოგიერთი შეიძლება იყოს ნამდვილი "ნულოვანი უჯრედის" ადენომები ან სხვა ჰორმონის მწარმოებელი უჯრედების ჩუმი ვარიანტები.
ვინაიდან მათ არ აქვთ ჰორმონის ჰიპერსეკრეციის სინდრომები, NFPA-ები ჩვეულებრივ ვლინდება უფრო გვიან, ვიდრე ფუნქციონირებადი ადენომები, ხშირად როდესაც ისინი იზრდებიან საკმარისად (მაკროადენომები), რომ გამოიწვიონ სიმპტომები მასის ეფექტის გამო:
- მხედველობის ველის დეფექტები (ჩვეულებრივ ბიტემპორალური ჰემიანოფსია მხედველობის ჯვარედინის კომპრესიის გამო).
- თავის ტკივილი (არასპეციფიკური, მაგარი გარსის დაჭიმვის ან თურქულ კეხში წნევის გამო).
- ჰიპოპიტუიტარიზმი (ნორმალური ჰიპოფიზის ქსოვილის კომპრესიის გამო, ყველაზე ხშირად მოქმედებს GH და გონადოტროპინის სეკრეციაზე ჯერ, რასაც მოჰყვება TSH და ACTH).
- კრანიალური ნერვების დამბლა (ნაკლებად გავრცელებული, კავერნოზულ სინუსში შეჭრის გამო, იწვევს დიპლოპიას ან სახის დაბუჟებას).
- ჰიპოფიზის აპოპლექსია (მწვავე სისხლჩაქცევა/ინფარქტი სიმსივნის შიგნით).
ბევრი პატარა NFPA შემთხვევით აღმოჩნდება (მრტ ან კტ) როგორც ჰიპოფიზის ინციდენტალომები. აუტოფსიისა და ვიზუალიზაციის კვლევები მიუთითებს ჩუმი მიკროადენომების მაღალ გავრცელებაზე (1-დან 6-მდე ადამიანი პოტენციურად ატარებს მას), მაგრამ უმეტესობა რჩება მცირე და უსიმპტომო მთელი ცხოვრების განმავლობაში.
სიმპტომატური NFPA-ების პირველადი მკურნალობა, რომლებიც იწვევენ მასის ეფექტს ან პროგრესირებად ჰიპოპიტუიტარიზმს, არის ქირურგიული რეზექცია, ჩვეულებრივ ტრანსსფენოიდული გზით. ძირითადი მიზნებია მიმდებარე სტრუქტურების დეკომპრესია (განსაკუთრებით მხედველობის აპარატის, მხედველობის გასაუმჯობესებლად/შესანარჩუნებლად) და სიმსივნის მაქსიმალური უსაფრთხო მოცილება მასის ეფექტის შესამცირებლად და პოტენციურად ჰიპოფიზის ფუნქციის გასაუმჯობესებლად. უსიმპტომო შემთხვევითი NFPA-ების მართვა მოიცავს მონიტორინგს სერიული ვიზუალიზაციით და ენდოკრინული/ვიზუალური შეფასებებით [23].
ჰიპოფიზის ადენომისა და ჰიპერპროლაქტინემიის სინდრომის დიაგნოსტიკა
სელარული/სუპრასელარული მასების დიფერენციალური დიაგნოზი
| მდგომარეობა | ძირითადი მახასიათებლები / განმასხვავებელი ნიშნები | ტიპიური ვიზუალიზაციის აღმოჩენები (მრტ) |
|---|---|---|
| ჰიპოფიზის ადენომა (მიკრო/მაკრო) | ენდოკრინული სიმპტომები (სიჭარბე/დეფიციტი) ან მასის ეფექტი (მხედველობის დაკარგვა, თავის ტკივილი, CN დამბლა). წარმოიქმნება კეხის შიგნით, აადგილებს ჯირკვალს, შეიძლება გავრცელდეს სუპრა/პარასელარულად. | მიკრო: კეროვანი დაზიანება <10მმ, ტიპიურად T1 ჰიპოინტენსიური, კონტრასტდება ნაკლებად/გვიან ვიდრე ნორმალური ჯირკვალი. მაკრო: სელარული მასა ≥10მმ, ცვალებადი კონტრასტირება (ხშირად ნაკლები ვიდრე ჯირკვალი), შეიძლება აჩვენოს სისხლჩაქცევა/კისტა, ვრცელდება სუპრა/პარასელარულად, შეიძლება გაანადგუროს ძვალი. |
| კრანიოფარინგიომა | ბიმოდალური ასაკობრივი პიკი (ბავშვები/ხანდაზმულები). სუპრასელარული ლოკაცია ხშირია. თავის ტკივილი, მხედველობის დაკარგვა, ენდოკრინული დისფუნქცია (GH დეფიციტი, DI ხშირია), ჰიდროცეფალია. | ხშირად შერეული კისტოზური (T1 ცვალებადი/T2 ჰიპერ) და მყარი კომპონენტები. კალციფიკაცია ძალიან ხშირია (კტ საუკეთესოა). კონტრასტდება (მყარი ნაწილები, სქელი კისტის კედელი). ტიპიურად სუპრასელარული ეპიცენტრი, შეიძლება მიეკრას მიმდებარე სტრუქტურებს. |
| მენინგიომა (სელარული/სუპრასელარული/კავერნოზული სინუსი) | მოზრდილები, Q>მ ტიპიურად. ნელა მზარდი, მაგარ გარსზე დაფუძნებული (planum sphenoidale, tuberculum sellae, დიაფრაგმა, კავერნოზული სინუსის კედელი). მასის ეფექტი (მხედველობის დაკარგვა, CN დამბლა), თავის ტკივილი, კრუნჩხვები. იშვიათად მნიშვნელოვანი ენდოკრინული დისფუნქცია, თუ ძალიან დიდი არ არის. | ხშირად იზოინტენსიური T1/T2, ინტენსიური ჰომოგენური კონტრასტირება კონტრასტის შემდეგ, დამახასიათებელი "დურალური კუდის" ნიშანი ხშირია. შეიძლება გამოიწვიოს ჰიპეროსტოზი (ძვლის გასქელება) ან შემოერტყას სისხლძარღვებს. |
| რატკეს ჯიბის კისტა | კეთილთვისებიანი ეპითელური კისტა (რატკეს ჯიბის ნარჩენი), ხშირად შემთხვევითი. შეიძლება გამოიწვიოს თავის ტკივილი, მხედველობის დარღვევა ან ჰიპოპიტუიტარიზმი, თუ დიდია. ჩვეულებრივ ინტრასელარული ან ინტრა/სუპრასელარული შუა ხაზის ლოკაცია. | კარგად განსაზღვრული არაკონტრასტირებადი კისტა (ჩვეულებრივ). სიგნალი ძალიან განსხვავდება (T1 ჰიპერ/იზო/ჰიპო, T2 ჩვეულებრივ ჰიპერ) ცილოვანი შიგთავსის მიხედვით. თხელი, გლუვი კედელი, ჩვეულებრივ არ არის მყარი კომპონენტი ან კონტრასტირება (შეიძლება აჩვენოს თხელი რგოლი). ინტრაკისტოზური კვანძი (ცილოვანი/ჰემორაგიული) შესაძლებელია (<30%). |
| ჰიპოფიზის ჰიპერპლაზია | ნორმალური ჯირკვლის ქსოვილის გადიდება. ფიზიოლოგიური (ორსულობა, ლაქტაცია, სქესობრივი მომწიფება) ან პათოლოგიური (პასუხი სამიზნე ორგანოს უკმარისობაზე, როგორიცაა პირველადი ჰიპოთირეოზი, პირველადი თირკმელზედა ჯირკვლის უკმარისობა). | დიფუზურად გადიდებული ჯირკვალი (>10-12მმ სიმაღლე შესაძლებელია), ჩვეულებრივ კონტრასტდება ჰომოგენურად და ინტენსიურად. კეხი შეიძლება გადიდდეს სიმეტრიულად. ჯირკვლის ფორმა შენარჩუნებულია (ჩაზნექილი ზედა საზღვარი დაკარგულია). ქრება ძირითადი მიზეზის მკურნალობის შემთხვევაში. |
| ჰიპოფიზიტი (ლიმფოციტური, გრანულომატოზური, IgG4) | ჰიპოფიზის/ღეროს ანთება. თავის ტკივილი, მხედველობის დარღვევა, ჰიპოპიტუიტარიზმი (ხშირად სწრაფი დაწყება, მრავალი ღერძი), უშაქრო დიაბეტი (DI) ხშირია (განსაკუთრებით ღეროს ჩართულობა). ლიმფოციტური ხშირად მშობიარობის შემდგომ/აუტოიმუნურ კონტექსტში. | ხშირად სიმეტრიული ჯირკვლის/ღეროს გადიდება და გასქელება, დიფუზური ინტენსიური კონტრასტირება. შეიძლება მიბაძოს ადენომას, მაგრამ ხშირად ღეროს უფრო ინფილტრაციული იერი აქვს. კლინიკური კონტექსტი გადამწყვეტია (სწრაფი დაწყების ჰიპოპიტუიტარიზმი/DI). |
| მეტასტაზი | პირველადი კიბოს ისტორია (ძუძუს, ფილტვის ყველაზე გავრცელებული). სწრაფი დაწყების ჰიპოპიტუიტარიზმი, DI ხშირია (უკანა ჰიპოფიზის/ღეროს პრედილექცია). თავის ტკივილი, მხედველობის დაკარგვა, CN დამბლა შესაძლებელია. | კონტრასტირებადი დაზიანება, ხშირად ინფილტრაციული, ხშირად მოიცავს უკანა ჰიპოფიზს ან ღეროს. შეიძლება იყოს მრავლობითი ინტრაკრანიალური დაზიანებები. პირველადი ავთვისებიანი სიმსივნის ძიება არის საკვანძო. |
| ანევრიზმა (კავერნოზული/სუპრასელარული ICA) | შეუძლია მიბაძოს სელარულ მასას, განსაკუთრებით თუ ნაწილობრივ თრომბოზირებულია. შეიძლება გამოიწვიოს CN დამბლა (III, IV, V, VI კავერნოზული სინუსის მდებარეობის გამო), თავის ტკივილი. გასკდომის რისკი (SAH). | მრტ აჩვენებს დამახასიათებელ ნაკადის სიცარიელეს (თუ ღიაა), თრომბის ლამინირებულ სიგნალს (თუ არსებობს), კედლის კონტრასტირებას. MRA/CTA/DSA ადასტურებს დიაგნოზს და ასახავს სისხლძარღვოვან ანატომიას. |
| ქორდომა / ქონდროსარკომა | იშვიათი ავთვისებიანი/ადგილობრივად აგრესიული თავის ქალას ფუძის სიმსივნეები, რომლებიც წარმოიქმნება ნოტოქორდის ნარჩენებისგან (ქორდომა) ან ხრტილისგან (ქონდროსარკომა). შეიძლება გავრცელდეს კეხში/სუპრასელარულ რეგიონში კლივუსიდან/კლდოვანი ნაწილის მწვერვალიდან. ხშირად იწვევს ფართო ძვლის დესტრუქციას, CN დამბლებს. | კტ აჩვენებს ძვლის დესტრუქციას. მრტ აჩვენებს ადგილობრივად დესტრუქციულ კონტრასტირებად მასას, ხშირად T2 ჰიპერინტენსიურს (განსაკუთრებით ქორდომა ფიზალიფორიული უჯრედების გამო). მდებარეობა ტიპიურად ცენტრირებულია კლივუსზე ან პეტროკლივურ შეერთებაზე. |
| გერმინომა (სუპრასელარული) | იშვიათი ჩანასახოვანი უჯრედების სიმსივნე, ჩვეულებრივ ბავშვები/ახალგაზრდები. კლასიკური ტრიადა: DI, მხედველობის დაკარგვა, ჰიპოპიტუიტარიზმი. შეიძლება მოიცავდეს ფიჭვისებრ რეგიონს ერთდროულად ("ორმაგი შუა ხაზის სიმსივნეები"). | ჰომოგენურად კონტრასტირებადი სუპრასელარული მასა, ხშირად მოიცავს მხედველობის ჯვარედინს, ღეროს/ჰიპოთალამუსს. ლიკვორის/შრატის სიმსივნური მარკერები (AFP, β-hCG) შეიძლება იყოს მომატებული (თუმცა ხშირად ნორმალურია წმინდა გერმინომის დროს). უაღრესად რადიომგრძნობიარე. |
დიაგნოსტიკა ხშირად მოიცავს ჰიპოფიზის ჯირკვლის მაგნიტურ-რეზონანსულ ტომოგრაფიას (მრტ), ოქროს სტანდარტს ადენომების (მიკროადენომები, მაკროადენომები, პროლაქტინომების ჩათვლით) ვიზუალიზაციისთვის, მათი ზომის, მასშტაბის, მიმდებარე სტრუქტურებთან ურთიერთობის შესაფასებლად, როგორიცაა მხედველობის ჯვარედინი და კავერნოზული სინუსები, და ეხმარება სხვა სელარული დაზიანებებისგან დიფერენცირებაში.
სადიაგნოსტიკო მიდგომა აერთიანებს კლინიკურ შეფასებას, ჰორმონალურ ტესტირებას და ვიზუალიზაციას:
- კლინიკური ეჭვი: დაფუძნებულია ჰორმონის სიჭარბის სიმპტომებზე (მაგ., აკრომეგალიის მახასიათებლები, კუშინგოიდური ნიშნები, გალაქტორეა/ამენორეა), მასის ეფექტზე (მხედველობის ცვლილებები, თავის ტკივილი, კრანიალური ნერვის დამბლა), ჰიპოპიტუიტარიზმზე (დაღლილობა, ჰიპოგონადიზმი, სიცივის აუტანლობა და ა.შ.) ან შემთხვევით აღმოჩენაზე ვიზუალიზაციისას.
- ჰორმონალური შეფასება: წინა ჰიპოფიზის ჰორმონების და მათი სამიზნე ორგანოს ჰორმონების ბაზალური დონის გაზომვა აუცილებელია ჰორმონის სიჭარბის ან დეფიციტის იდენტიფიცირებისთვის. ძირითადი ტესტები მოიცავს:
- პროლაქტინი (PRL): მომატებული დონე მიუთითებს ჰიპერპროლაქტინემიაზე. მკვეთრად მომატებული დონე (>200-250 ნგ/მლ ან მკგ/ლ) ძლიერ მიუთითებს პროლაქტინომაზე (განსაკუთრებით მაკროადენომაზე). ზომიერად მომატებული დონე (25-150 ნგ/მლ) მოითხოვს სხვა მიზეზების შეფასებას (მედიკამენტები, ჰიპოთირეოზი, ღეროს ეფექტი და ა.შ.). შეამოწმეთ "კაუჭის ეფექტი" გაზავებული ნიმუშით, თუ არსებობს მაკროადენომა და PRL მოულოდნელად დაბალი/ნორმალურია [24].
- ზრდის ჰორმონი (GH) / ინსულინის მსგავსი ზრდის ფაქტორი 1 (IGF-1): მომატებული ასაკთან და სქესთან შესაბამისი IGF-1 არის საუკეთესო სკრინინგ ტესტი აკრომეგალიისთვის. დიაგნოზი დასტურდება GH-ის დათრგუნვის წარუმატებლობით (< 0.4 ან < 1 ნგ/მლ ანალიზის მიხედვით) გლუკოზის ტოლერანტობის ორალური ტესტის (OGTT) დროს. ბაზალური GH დონეები ნაკლებად სანდოა პულსაციურობის გამო.
- ACTH / კორტიზოლი: კუშინგის სინდრომის სკრინინგი მოიცავს ისეთ ტესტებს, როგორიცაა გვიან ღამით ნერწყვის კორტიზოლი, 24-საათიანი შარდის თავისუფალი კორტიზოლი (UFC) ან დაბალი დოზით (1მგ) ღამის დექსამეტაზონის სუპრესიის ტესტი. თუ დადებითია, პლაზმის ACTH დონეები ეხმარება ACTH-ზე დამოკიდებული (ჰიპოფიზური/ექტოპიური) და დამოუკიდებელი (თირკმელზედა ჯირკვლის) მიზეზების დიფერენცირებას. მაღალი დოზით დექსამეტაზონის სუპრესიის ტესტები და/ან CRH სტიმულაციის ტესტები, ზოგჯერ შერწყმული ქვედა კლდოვანი სინუსის შერჩევასთან (IPSS), ეხმარება ჰიპოფიზური წარმოშობის დადასტურებას (კუშინგის დაავადება) [4].
- TSH / თავისუფალი T4/T3: მომატებული ან შეუსაბამოდ ნორმალური TSH მომატებული თავისუფალი T4/T3-ით მიუთითებს იშვიათ TSH-ომაზე. ტესტირება ასევე ატარებს სკრინინგს პირველად ჰიპოთირეოზზე (მაღალი TSH, დაბალი FT4), რომელიც არის მეორადი ჰიპერპროლაქტინემიის პოტენციური მიზეზი.
- LH / FSH / ტესტოსტერონი (მამაკაცები) / ესტრადიოლი (ქალები): შეაფასეთ გონადების ფუნქცია. დაბალი დონე მიუთითებს ჰიპოგონადიზმზე (მეორადი, თუ LH/FSH ასევე დაბალი/ნორმალურია). მომატებული ალფა-ქვეერთეული ხშირია გონადოტროფულ ადენომებში.
- ჰიპოპიტუიტარიზმის შეფასება: თუ მასის ეფექტი ან სიმპტომები მიუთითებს დეფიციტზე, შეამოწმეთ საწყისი დილის კორტიზოლი და ACTH, TSH და თავისუფალი T4, LH/FSH და ტესტოსტერონი/ესტრადიოლი (როგორც საჭიროა), IGF-1 (GH ღერძისთვის). დინამიური სტიმულაციის ტესტები (მაგ., ACTH სტიმულაციის ტესტი, ინსულინის ტოლერანტობის ტესტი - ოქროს სტანდარტი, მაგრამ სარისკო, GHRH-არგინინის ტესტი) შეიძლება იყოს საჭირო დახვეწილი დეფიციტის დასადასტურებლად. შეაფასეთ უშაქრო დიაბეტი (DI), თუ ჩართულია უკანა ჰიპოფიზი (პოლიურია, პოლიდიფსია, შრატის/შარდის ოსმოლარობა).
- ვიზუალიზაცია:
- ჰიპოფიზის მრტ: გადოლინიუმის კონტრასტით და მის გარეშე, თხელი ჭრილებით (≤3მმ) კეხის გავლით კორონალურ და საგიტალურ სიბრტყეებში. დინამიური კონტრასტით გაძლიერებული მიმდევრობები განსაკუთრებით სასარგებლოა მიკროადენომების გამოსავლენად, რომლებიც ხშირად ჩნდებიან დაგვიანებული კონტრასტირების კეროვან უბნებად, სწრაფად კონტრასტირებად ნორმალურ წინა ჰიპოფიზის ჯირკვალთან შედარებით. მრტ ზუსტად განსაზღვრავს სიმსივნის ზომას, ურთიერთობას მხედველობის ჯვარედინთან, კავერნოზულ სინუსში შეჭრას (Knosp კლასიფიკაცია) და ღეროს გადახრას [25].
- კტ სკანირება: ნაკლებად მგრძნობიარეა თავად ადენომებისთვის, მაგრამ უკეთესია კეხის ფსკერის ან კლინოიდური მორჩების ძვლოვანი ეროზიის და კალციფიკაციების (უფრო ხშირია კრანიოფარინგიომებში) საჩვენებლად. გამოსადეგია, თუ მრტ უკუნაჩვენებია.
- ოფთალმოლოგიური შეფასება: ფორმალური მხედველობის ველის ტესტირება (ტიპიურად ავტომატიზებული პერიმეტრია, მაგ., ჰამფრის მხედველობის ველი) სავალდებულოა, თუ ადენომა ახლოს არის ან აწვება მხედველობის ჯვარედინს (მაკროადენომები), მაშინაც კი, თუ პაციენტი არ აღნიშნავს მხედველობის სიმპტომებს. მხედველობის სიმახვილის და მხედველობის ნერვის იერსახის შეფასება (ფუნდუსკოპია სიფერმკრთალის/ატროფიის ან პაპილედემისთვის) ასევე სტანდარტულია.
- ჰიპერპროლაქტინემიის დიფერენციალური დიაგნოზი: თუ აღმოჩენილია მომატებული პროლაქტინი, სისტემატურად გამორიცხეთ სხვა მიზეზები პროლაქტინომის დიაგნოზამდე, განსაკუთრებით თუ დონე მხოლოდ ზომიერად მაღალია (<150 ნგ/მლ) ან ვიზუალიზაცია ნორმალური/ორაზროვანია. განიხილეთ:
- ფიზიოლოგიური მიზეზები: ორსულობა, ლაქტაცია, სტრესი, ძილი (შეამოწმეთ დილის დონეები), ვარჯიში, დვრილის სტიმულაცია, სქესობრივი კავშირი.
- მედიკამენტები: გადახედეთ მიმდინარე მედიკამენტებს (ანტიფსიქოტიკები - განსაკუთრებით რისპერიდონი, ტიპიური; ანტიდეპრესანტები - SSRIs, TCAs; ღებინების საწინააღმდეგო საშუალებები - მეტოკლოპრამიდი, დომპერიდონი; ანტიჰიპერტენზიული საშუალებები - ვერაპამილი, მეთილდოპა; ოპიოიდები; ესტროგენები). შეაჩერეთ საეჭვო პრეპარატი, თუ შესაძლებელია და გადაამოწმეთ PRL ~3 დღის შემდეგ (ან უფრო გრძელი ნახევარგამოყოფის პერიოდის შემდეგ).
- სისტემური პირობები: პირველადი ჰიპოთირეოზი (შეამოწმეთ TSH/FT4), თირკმლის ქრონიკული დაავადება (შეამოწმეთ კრეატინინი), ღვიძლის მძიმე ციროზი, საკვერცხეების პოლიკისტოზური სინდრომი (PCOS), გულმკერდის კედლის დაზიანებები (ჰერპეს ზოსტერი, ქირურგიული ნაწიბურები, პირსინგი).
- ჰიპოფიზის ღეროს ეფექტი: ჰიპოფიზის ღეროს კომპრესია არაპროლაქტინის გამომყოფი სიმსივნეებით (NFPAs, კრანიოფარინგიომები, მენინგიომები) ან ანთებითი დაზიანებები წყვეტს დოფამინის მიწოდებას ჰიპოთალამუსიდან ლაქტოტროფებამდე, რაც იწვევს მსუბუქ/საშუალო ჰიპერპროლაქტინემიას (ჩვეულებრივ <150 ნგ/მლ). ვიზუალიზაცია საკვანძოა.
- მაკროპროლაქტინემია: დიდი, ბიოლოგიურად ნაკლებად აქტიური პროლაქტინის კომპლექსების არსებობა; მოითხოვს სპეციფიკურ ლაბორატორიულ ტესტირებას (PEG პრეციპიტაცია); კლინიკურად უმნიშვნელოა, როგორც წესი.
შრატის პროლაქტინის ნორმალური დონე ოდნავ განსხვავდება ლაბორატორიისა და ანალიზის მიხედვით, მაგრამ ზოგადად არის (მიახლოებითი დიაპაზონი):
პაციენტთა ჯგუფი |
პროლაქტინის მიახლოებითი ნორმალური დიაპაზონი (ნგ/მლ ან მკგ/ლ) |
(მიახლოებითი SI ერთეულები: mIU/L) |
|---|---|---|
ბავშვები (პრე-პუბერტატული) |
ცვალებადია, ზოგადად < 15-20 | ~ < 300-400 |
ზრდასრული მამაკაცები |
< 15-20 | ~ < 300-400 |
არაორსული ზრდასრული ქალები |
< 25-30 | ~ < 500-600 |
ორსული ქალები |
მნიშვნელოვნად მომატებულია, იზრდება ორსულობის განმავლობაში (მაგ., 200-400+ ნგ/მლ-მდე) | ~ 4000-8000+ mIU/L-მდე |
მშობიარობის შემდგომ (მეძუძური) |
მომატებულია, დონე მერყეობს ძუძუთი კვებასთან ერთად, თანდათან მცირდება, თუ არ კვებავს | ცვალებადია, შეიძლება თავდაპირველად ძალიან მაღალი იყოს |
კონვერსიის ფაქტორი მიახლოებითია (1 ნგ/მლ ≈ 21 mIU/L WHO სტანდარტებზე დაყრდნობით, მაგრამ განსხვავდება ანალიზის მიხედვით).
ჰიპოფიზის ადენომისა და ჰიპერპროლაქტინემიის სინდრომის მკურნალობა
ჰიპოფიზის ადენომების მკურნალობის მიზნებია ჰორმონების დონის ნორმალიზება (თუ გადაჭარბებულია), მასის ეფექტის სიმპტომების შემსუბუქება (მხედველობის დაკარგვა, თავის ტკივილი, კრანიალური ნერვის დამბლა), ჰიპოფიზის ნორმალური ფუნქციის შენარჩუნება ან აღდგენა და სიმსივნის რეციდივის პრევენცია. კონკრეტული მიდგომა დიდად არის დამოკიდებული ადენომის ტიპზე (ფუნქციონირებადი არაფუნქციონირებადის წინააღმდეგ), ზომაზე (მიკრო მაკროს წინააღმდეგ), გამოყოფილ ჰორმონზე, მასის ეფექტის არსებობასა და სიმძიმეზე, პაციენტის ასაკზე, რეპროდუქციულ მიზნებსა და თანმხლებ დაავადებებზე[26, 2, 4, 23].
- პროლაქტინომები (ჰიპერპროლაქტინემია):
- მედიკამენტური თერაპია (პირველი რიგის): დოფამინის აგონისტები (DA) უაღრესად ეფექტურია და წარმოადგენს სასურველ საწყის მკურნალობას პრაქტიკულად ყველა პროლაქტინომისთვის, მათ შორის დიდი მაკროადენომებისთვის, რომლებიც იწვევენ მხედველობის ველის დეფექტებს (გარდა იმ შემთხვევისა, როდესაც მხედველობის დაკარგვა მძიმეა/სწრაფად პროგრესირებს).
- კაბერგოლინი: ზოგადად უპირატესობა ენიჭება უფრო მაღალი ეფექტურობის გამო პროლაქტინის ნორმალიზებასა და სიმსივნეების შემცირებაში, უფრო გრძელი ნახევარგამოყოფის პერიოდის გამო, რაც იძლევა კვირაში ერთხელ ან ორჯერ მიღების საშუალებას, და უკეთესი ტოლერანტობის გამო ბრომოკრიპტინთან შედარებით.
- ბრომოკრიპტინი: ძველი აგენტი, მოითხოვს ყოველდღიურ დოზირებას, უფრო მეტად ასოცირდება გულისრევასთან/პოსტურალურ ჰიპოტენზიასთან, მაგრამ აქვს უსაფრთხოების უფრო გრძელი ჩანაწერი, განსაკუთრებით ორსულობის დროს.
- ქირურგია (ნეიროქირურგიული ჩარევა - ტრანსსფენოიდული ქირურგია): ნაჩვენებია ძირითადად პაციენტებისთვის, რომლებიც ვერ იტანენ ან რეზისტენტულნი არიან დოფამინის აგონისტების მიმართ, მათთვის, ვისაც აქვს ჰიპოფიზის აპოპლექსია პროლაქტინომაში, იშვიათი შემთხვევებისთვის დიდი კისტოზური/ჰემორაგიული კომპონენტებით, რომლებიც არ რეაგირებენ DA-ებზე, ან ზოგჯერ ქალებისთვის, რომლებსაც სურთ ორსულობა და ვერ იტანენ ან სურთ თავიდან აიცილონ DA-ები. განკურნების მაჩვენებლები უფრო მაღალია მიკროადენომებისთვის (~70-90%), ვიდრე ინვაზიური მაკროადენომებისთვის (~30-50%).
- სხივური თერაპია (სტერეოტაქსიური რადიოქირურგია ან ფრაქციული RT): დაცულია ინვაზიური/აგრესიული პროლაქტინომების იშვიათი შემთხვევებისთვის, რომლებიც რეზისტენტულია ან მეორდება მაქსიმალური სამედიცინო და ქირურგიული თერაპიის შემდეგ. გამოიყენება ძირითადად სიმსივნის გასაკონტროლებლად, რადგან პროლაქტინის დონეზე ეფექტი ნელია და ხშირად არასრული; ჰიპოპიტუიტარიზმის მაღალი რისკი.
- მედიკამენტური თერაპია (პირველი რიგის): დოფამინის აგონისტები (DA) უაღრესად ეფექტურია და წარმოადგენს სასურველ საწყის მკურნალობას პრაქტიკულად ყველა პროლაქტინომისთვის, მათ შორის დიდი მაკროადენომებისთვის, რომლებიც იწვევენ მხედველობის ველის დეფექტებს (გარდა იმ შემთხვევისა, როდესაც მხედველობის დაკარგვა მძიმეა/სწრაფად პროგრესირებს).
- აკრომეგალია (GH-სეკრეტორული ადენომები):
- ქირურგია (ზოგადად პირველი რიგის): ტრანსსფენოიდული ქირურგია არის პირველადი მკურნალობა, რომელიც მიზნად ისახავს სრულ რეზექციას და ბიოქიმიურ განკურნებას (ასაკთან/სქესთან შესაბამისი IGF-1-ის ნორმალიზაცია და GH-ის დათრგუნვა OGTT-ის დროს). განკურნების მაჩვენებლები დამოკიდებულია სიმსივნის ზომაზე, ინვაზიურობაზე და ქირურგის გამოცდილებაზე.
- მედიკამენტური თერაპია: გამოიყენება ქირურგიის შემდეგ მუდმივი დაავადებისთვის, პაციენტებისთვის, რომლებიც შეუფერებელია ქირურგიისთვის, ან ზოგჯერ ოპერაციამდე ქირურგიული შედეგების გასაუმჯობესებლად. ვარიანტები მოიცავს:
- სომატოსტატინის რეცეპტორების ლიგანდები (SRLs): პირველი თაობა (ოკტრეოტიდი LAR, ლანრეოტიდი Autogel) აწესრიგებს IGF-1/GH-ს ~50-60%-ში და შეიძლება შეამციროს სიმსივნეები. მეორე თაობა (პასირეოტიდი LAR) შეიძლება იყოს ეფექტური, თუ პირველი თაობის SRL მარცხდება, მაგრამ ჰიპერგლიკემიის მაღალი რისკია.
- GH რეცეპტორის ანტაგონისტი (პეგვისომანტი): უაღრესად ეფექტურია IGF-1-ის ნორმალიზებაში (~80-90%) რეცეპტორზე GH მოქმედების ბლოკირებით; არ ამცირებს სიმსივნეს და მოითხოვს ღვიძლის ფუნქციისა და სიმსივნის ზომის მონიტორინგს.
- დოფამინის აგონისტები (კაბერგოლინი): ნაკლებად ეფექტურია, აწესრიგებს IGF-1-ს მხოლოდ ~10-30%-ში, ძირითადად გამოიყენება როგორც დამატებითი თერაპია, განსაკუთრებით თუ სიმსივნე ერთდროულად გამოყოფს პროლაქტინს.
- სხივური თერაპია (სტერეოტაქსიური ან ფრაქციული): ეფექტურია სიმსივნის ზრდის გასაკონტროლებლად და GH/IGF-1 დონის ნელა შესამცირებლად პაციენტებში ნარჩენი/მორეციდივე დაავადებით, რომლებიც არ რეაგირებენ სამედიცინო თერაპიაზე. დაგვიანებული ჰიპოპიტუიტარიზმის მაღალი რისკი.
- კუშინგის დაავადება (ACTH-სეკრეტორული ადენომები):
- ქირურგია (პირველი რიგის): ტრანსსფენოიდული სელექტიური ადენომექტომია არის არჩევითი მკურნალობა, რომელიც მიზნად ისახავს ბიოქიმიურ რემისიას ნორმალური ჰიპოფიზის ფუნქციის შენარჩუნებით. რემისიის მაჩვენებლები არის ~70-90% მიკროადენომებისთვის გამოცდილ ცენტრებში [27].
- მედიკამენტური თერაპია: გამოიყენება ოპერაციამდე მძიმე ჰიპერკორტიზოლიზმის გასაკონტროლებლად, პოსტოპერაციულად მუდმივი/მორეციდივე დაავადებისთვის RT-ის ეფექტის მოლოდინში, ან როგორც პირველადი თერაპია, თუ ქირურგია მარცხდება/უკუნაჩვენებია. მედიკამენტები მიზნად ისახავს თირკმელზედა ჯირკვლის სტეროიდოგენეზს (კეტოკონაზოლი, მეტირაპონი, ეტომიდატი, ოსილოდროსტატი), ჰიპოფიზის ACTH სეკრეციას (პასირეოტიდი, კაბერგოლინი) ან გლუკოკორტიკოიდული რეცეპტორების ბლოკადას (მიფეპრისტონი).
- სხივური თერაპია (სტერეოტაქსიური ან ფრაქციული): ეფექტურია ოპერაციის შემდეგ მუდმივი/მორეციდივე დაავადებისთვის, მაგრამ ბიოქიმიური რემისია დაგვიანებულია (თვეებიდან წლებამდე).
- ორმხრივი ადრენალექტომია: უზრუნველყოფს ჰიპერკორტიზოლიზმის საბოლოო განკურნებას, თუ ჰიპოფიზზე მიმართული თერაპიები მარცხდება, მაგრამ იწვევს მუდმივ თირკმელზედა ჯირკვლის უკმარისობას, რომელიც მოითხოვს გლუკოკორტიკოიდების/მინერალოკორტიკოიდების მთელი ცხოვრების განმავლობაში ჩანაცვლებას და შეიცავს ნელსონის სინდრომის რისკს (პროგრესირებადი ზრდა/პიგმენტაცია ჰიპოფიზის ACTH-სეკრეტორული სიმსივნისგან).
- TSH-ომები (იშვიათი):
- ქირურგია (პირველი რიგის): ტრანსსფენოიდული რეზექცია არის სასურველი მკურნალობა.
- მედიკამენტური თერაპია: სომატოსტატინის რეცეპტორების ლიგანდები (ოკტრეოტიდი, ლანრეოტიდი) ხშირად ეფექტურია TSH სეკრეციის დათრგუნვაში და სიმსივნეების შემცირებაში ოპერაციამდე ან ნარჩენი დაავადებისთვის. ანტითირეოიდული პრეპარატები (მეთიმაზოლი, PTU) მართავენ ჰიპერთირეოზის სიმპტომებს, მაგრამ არ მკურნალობენ სიმსივნეს.
- სხივური თერაპია: ნარჩენი/მორეციდივე სიმსივნეებისთვის, რომლებიც არ რეაგირებენ სხვა თერაპიებზე.
- ჰიპოფიზის არაფუნქციონირებადი ადენომები (NFPAs): იხილეთ სექცია ქვემოთ.
მართვის გადაწყვეტილებები უნდა იყოს ინდივიდუალიზებული და ხშირად მოითხოვს მულტიდისციპლინურ გუნდურ მიდგომას ენდოკრინოლოგების, ნეიროქირურგების, ნეირორადიოლოგების, ოფთალმოლოგების და ზოგჯერ რადიაციული ონკოლოგების მონაწილეობით.
ჰიპოფიზის არაფუნქციონირებადი ადენომების (NFPAs) მკურნალობა
ვინაიდან NFPA-ები ტიპიურად არ იწვევენ ჰორმონის სიჭარბის სინდრომებს, მკურნალობა ნაჩვენებია პირველ რიგში, როდესაც ისინი იწვევენ მასის ეფექტს (მხედველობის დაქვეითება, კრანიალური ნერვის დამბლა, კლინიკურად მნიშვნელოვანი თავის ტკივილი, რომელიც მიეკუთვნება სიმსივნეს) ან ჰიპოპიტუიტარიზმს, ან თუ ისინი აჩვენებენ მნიშვნელოვან ზრდას სერიულ ვიზუალიზაციაზე [22, 23].
- უსიმპტომო შემთხვევითი NFPA-ები:
- მიკროადენომები (<10მმ): ზოგადად იმართება კონსერვატიულად პერიოდული მრტ ზედამხედველობით (მაგ., მრტ 1 წელიწადში, შემდეგ 1-2 წელიწადში, შემდეგ უფრო იშვიათად, თუ სტაბილურია) და საბაზისო ენდოკრინული შეფასებით (ჰიპოპიტუიტარიზმის სკრინინგი და ჰიპერპროლაქტინემია ღეროს ეფექტის გამო). უმეტესობა (~90-95%) მნიშვნელოვნად არ იზრდება [8].
- მაკროადენომები (≥10მმ) მასის ეფექტის გარეშე (არ არის მხედველობის დეფიციტი, ჰიპოფიზის ნორმალური ფუნქცია, არ ებჯინება ქიაზმას): მართვა ინდივიდუალიზებულია. ვარიანტები მოიცავს მჭიდრო მონიტორინგს მრტ-ით (მაგ., 6 თვეში, შემდეგ ყოველწლიურად, თუ სტაბილურია) და რეგულარულ ენდოკრინულ/ვიზუალურ შეფასებებს, ან ქირურგიის განხილვას, განსაკუთრებით თუ სიმსივნე დიდია ან ძალიან ახლოს არის მხედველობის ჯვარედინთან, მომავალი ზრდის/გართულებების პოტენციალის გათვალისწინებით. ჩარევა ნაჩვენებია, თუ დაფიქსირდა სიმსივნის ზრდა, სიმპტომების განვითარება (მხედველობის დაკარგვა, ჰიპოპიტუიტარიზმი), ან თუ სიმსივნე ებჯინება/აკომპრესირებს მხედველობის ჯვარედინს [23].
- სიმპტომატური NFPA-ები (იწვევენ მასის ეფექტს ან ჰიპოპიტუიტარიზმს):
- ქირურგიული ჩარევა (პირველი რიგის): ტრანსსფენოიდული ქირურგია არის პირველადი მკურნალობა. ძირითადი მიზნებია მხედველობის აპარატის დეკომპრესია მხედველობის გასაუმჯობესებლად/შესანარჩუნებლად და სიმსივნის მაქსიმალური უსაფრთხო მოცილება მასის ეფექტის შესამსუბუქებლად და პოტენციურად ჰიპოფიზის ფუნქციის აღდგენის დასაშვებად (ნაკლებად სავარაუდოა, თუ დეფიციტი დიდი ხნისაა). ენდოსკოპიური ენდონაზალური მიდგომები ახლა ჩვეულებრივ გამოიყენება. სრული რეზექცია ხშირად რთულია დიდი ან ინვაზიური (მაგ., კავერნოზულ სინუსში) სიმსივნეებისთვის.
- სხივური თერაპია (სტერეოტაქსიური რადიოქირურგია - SRS ან ფრაქციული RT): ნაჩვენებია პირველ რიგში, როგორც დამხმარე მკურნალობა მნიშვნელოვანი ნარჩენი სიმსივნისთვის ოპერაციის შემდეგ (განსაკუთრებით თუ იზრდება ან დიდი ნარჩენი მოცულობაა), ან მორეციდივე სიმსივნეებისთვის. პირველადი RT იშვიათად გამოიყენება, თუ ქირურგია არ არის უკუნაჩვენები. RT უზრუნველყოფს სიმსივნის გრძელვადიანი კონტროლის შესანიშნავ მაჩვენებლებს (>90%), მაგრამ დაუყოვნებლივ არ ამცირებს მასის ეფექტს და ატარებს რადიაციით გამოწვეული ჰიპოპიტუიტარიზმის მნიშვნელოვან დაგვიანებულ რისკს (~30-60% 10 წლის განმავლობაში) [28].
- მედიკამენტური თერაპია: ამჟამად არ არსებობს ეფექტური სამედიცინო თერაპია, რომელიც დადასტურებულია, რომ თანმიმდევრულად ამცირებს NFPA-ებს ან ხელს უშლის ზრდას. დოფამინის აგონისტები ან სომატოსტატინის ანალოგები შესწავლილია, მაგრამ ზოგადად არაეფექტურია ტიპიური გონადოტროფული NFPA-ებისთვის.
- ჰიპოპიტუიტარიზმის მართვა: მკურნალობამდე ან მის შემდეგ გამოვლენილი ჰორმონალური დეფიციტი მოითხოვს შესაბამის და უწყვეტ ფიზიოლოგიურ ჩანაცვლებით თერაპიას (მაგ., ჰიდროკორტიზონი თირკმელზედა ჯირკვლის უკმარისობისთვის - საჭიროა სტრესული დოზის დაფარვა; ლევოთიროქსინი მეორადი ჰიპოთირეოზისთვის; ტესტოსტერონი/ესტროგენი +/- პროგესტერონი ჰიპოგონადიზმისთვის; პოტენციურად GH ჩანაცვლება მოზრდილებში დადასტურებული დეფიციტით და მნიშვნელოვანი გავლენით ცხოვრების ხარისხზე ან მეტაბოლურ პარამეტრებზე; DDAVP უშაქრო დიაბეტისთვის, თუ არსებობს).
- გრძელვადიანი შემდგომი დაკვირვება: აუცილებელია მკურნალობის შემდეგ (ქირურგია +/- რადიაცია) ყველა მაკროადენომისთვის. მოიცავს სიმსივნის რეციდივის ან ხელახალი ზრდის მონიტორინგს (სერიული მრტ, სიხშირე დამოკიდებულია ნარჩენ სიმსივნეზე/მკურნალობის ტიპზე), ენდოკრინული ფუნქციის რეგულარულ შეფასებას (ჰიპოპიტუიტარიზმის ყოველწლიური ტესტირება, მათ შორის RT-ს შემდეგ) და ვიზუალური სტატუსის მონიტორინგს (მხედველობის ველები, თუ არსებობს კომპრესიის ისტორია). რეციდივის მაჩვენებლები მხოლოდ ოპერაციის შემდეგ შეიძლება იყოს მნიშვნელოვანი დროთა განმავლობაში (10-50% დამოკიდებულია შემდგომი დაკვირვების ხანგრძლივობასა და ნარჩენ სიმსივნეზე), რაც მოითხოვს დამხმარე სხივური თერაპიის განხილვას საგანგაშო ნარჩენი სიმსივნისთვის.
![]() ყურადღებით! ჰიპოფიზის ადენომები საჭიროებს სპეციალიზებულ დიაგნოზს და მართვას მულტიდისციპლინური გუნდის მიერ. სიმპტომები, როგორიცაა მხედველობის ცვლილებები, მუდმივი თავის ტკივილი, ჰორმონალური დისბალანსი (მენსტრუალური ცვლილებები, ლაქტაცია, აუხსნელი ფიზიკური ცვლილებები, სქესობრივი დისფუნქცია) ან გადაჭარბებული დაღლილობა მოითხოვს ექიმის შეფასებას, რაც პოტენციურად გამოიწვევს ენდოკრინოლოგთან და ნეიროქირურგთან რეფერალს.
ყურადღებით! ჰიპოფიზის ადენომები საჭიროებს სპეციალიზებულ დიაგნოზს და მართვას მულტიდისციპლინური გუნდის მიერ. სიმპტომები, როგორიცაა მხედველობის ცვლილებები, მუდმივი თავის ტკივილი, ჰორმონალური დისბალანსი (მენსტრუალური ცვლილებები, ლაქტაცია, აუხსნელი ფიზიკური ცვლილებები, სქესობრივი დისფუნქცია) ან გადაჭარბებული დაღლილობა მოითხოვს ექიმის შეფასებას, რაც პოტენციურად გამოიწვევს ენდოკრინოლოგთან და ნეიროქირურგთან რეფერალს.
ლიტერატურა
- Melmed S. Pituitary-Tumor Endocrinopathies. N Engl J Med. 2020 Mar 5;382(10):937-950. doi: 10.1056/NEJMra1810772
- Melmed S, Casanueva FF, Hoffman AR, et al. Diagnosis and Treatment of Hyperprolactinemia: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2011 Feb;96(2):273-88. doi: 10.1210/jc.2010-1692
- Katznelson L, Laws ER Jr, Melmed S, et al; Endocrine Society. Acromegaly: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2014 Nov;99(11):3933-51. doi: 10.1210/jc.2014-2700
- Nieman LK, Biller BM, Findling JW, et al. The diagnosis of Cushing's syndrome: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2008 May;93(5):1526-40. doi: 10.1210/jc.2008-0125
- Beck-Peccoz P, Persani L. Thyrotropin-secreting pituitary adenomas. N Engl J Med. 1996;334(11):712-713. doi: 10.1056/NEJM199603143341107
- Ntali G, Wass JA. Epidemiology, clinical presentation and diagnosis of non-functioning pituitary adenomas. Pituitary. 2011 Jun;14(2):111-8. doi: 10.1007/s11102-011-0300-1
- Molitch ME. Pituitary incidentalomas. Endocrinol Metab Clin North Am. 1997 Mar;26(1):1-17. doi: 10.1016/s0889-8529(05)70239-7
- Fernández-Balsells MM, Murad MH, Barwise A, et al. Clinical management of nonfunctioning pituitary adenomas (NFPAs): a systematic review and meta-analysis. J Clin Endocrinol Metab. 2011 Apr;96(4):905-15. doi: 10.1210/jc.2010-1921
- Chapter on Pituitary Imaging. In: Osborn AG, Salzman KL, Jhaveri MD, et al. Osborn's Brain. 2nd ed. Elsevier; 2018.
- Asa SL, Ezzat S. The pathogenesis of pituitary tumours. Nat Rev Cancer. 2002 Feb;2(2):83-94. doi: 10.1038/nrc760
- Vierimaa O, et al. Pituitary adenoma predisposition caused by germline mutations in the AIP gene. Science. 2006 May 26;312(5777):1228-30. doi: 10.1126/science.1126100
- Reincke M, et al. Mutations in the deubiquitinase gene USP8 cause Cushing's disease. Nat Genet. 2015 Jan;47(1):31-8. doi: 10.1038/ng.3166
- Costello RT. Subclinical adenoma of the pituitary gland. Am J Pathol. 1936 Mar;12(2):205-16.1.
- Ezzat S, Asa SL, Couldwell WT, et al. The prevalence of pituitary adenomas: a systematic review. Cancer. 2004 Aug 1;101(3):613-9. doi: 10.1002/cncr.20412
- Hall WA, et al. Pituitary magnetic resonance imaging in normal human volunteers: occult adenomas in the general population. Ann Intern Med. 1994 May 15;120(10):817-20. doi: 10.7326/0003-4819-120-10-199405150-00001
- Ciccarelli A, et al. High prevalence of pituitary adenomas: a cross-sectional study in the province of Varese, Italy. J Clin Endocrinol Metab. 2001 Feb;86(2):720-5. doi: 10.1210/jcem.86.2.7204
- Fernandez A, et al. Prevalence of pituitary adenomas: a community-based study in Olmsted County, Minnesota, 1993-1997. Arch Intern Med. 2000 Jan 10;160(1):78-81. doi: 10.1001/archinte.160.1.78
- Daly AF, et al. High prevalence of pituitary adenomas: a cross-sectional study in the province of Liege, Belgium. J Clin Endocrinol Metab. 2006 Dec;91(12):4756-69. doi: 10.1210/jc.2006-1668
- Melmed S. Acromegaly pathogenesis and treatment. J Clin Invest. 2009 Mar;119(3):429-38. doi: 10.1172/JCI38090
- Nieman LK. Cushing's syndrome: update on signs, symptoms and biochemical screening. Eur J Endocrinol. 2015 Oct;173(4):M33-8. doi: 10.1530/EJE-15-0464
- Elster AD, et al. Pituitary gland: MR imaging of physiologic hypertrophy in adolescence. Radiology. 1990;174(3 Pt 1):681-5. doi: 10.1148/radiology.174.3.2305044
- Molitch ME. Nonfunctioning pituitary adenomas. Pituitary. 2005;8(3-4):213-20. doi: 10.1007/s11102-006-8512-6
- Freda PU, Beckers AM, Katznelson L, et al; Endocrine Society. Pituitary incidentaloma: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2011 Apr;96(4):894-904. doi: 10.1210/jc.2010-1048
- Frieze TW, et al. Hook effect in prolactinomas: case report and review of literature. Endocr Pract. 2006;12(3):296-303. doi: 10.4158/EP.12.3.296
- Bonneville F, et al. Radiology of pituitary adenomas: an update. Radiol Clin North Am. 2012 Nov;50(6):995-1013. doi: 10.1016/j.rcl.2012.08.005
- Melmed S, et al. Guidelines for acromegaly management: an update. J Clin Endocrinol Metab. 2009;94(5):1509-17. doi: 10.1210/jc.2008-2421
- Nieman LK, Biller BMK, Findling JW, et al. Treatment of Cushing's Syndrome: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2015 Aug;100(8):2807-31. doi: 10.1210/jc.2015-1818
- Sheehan JP, et al. Radiosurgery for nonfunctioning pituitary adenomas: a systematic review. J Neurosurg. 2013 Aug;119(2):446-56. doi: 10.3171/2013.4.JNS121833
იხილეთ აგრეთვე
- ანატომია - თავის ტვინი და პერიფერიული ნერვები
- თავის ტვინის ინფექციური დაავადებები:
- თავის ტვინის ნახევარსფეროები და ნათხემი აბსცესი
- ეოზინოფილური გრანულომა, ლანგერჰანსის უჯრედების ჰისტიოციტოზი, ენებერის ფისტულური სიმპტომი
- თავის ტვინის ეპიდურალური აბსცესი
- ცხვირის ღრუს და მისი დამატებითი წიაღების ანთებითი დაავადებების შიდა ქალას გართულებები
- ყურის დაავადებების (ოტიტის) შიდა ქალას გართულებები
- ცხვირის ღრუს და წიაღების დაავადებების თვალბუდის გართულებები
- თავის ტვინის ჩირქოვანი ოტოგენური მენინგიტი
- თავის ტვინის სუბდურული აბსცესი
- სიგმოიდური სინუსის ჩირქოვანი თრომბოფლებიტი
- თავის ტვინის 3 პარკუჭის კოლოიდური კისტა
- ცერებრალური და სპინალური არაქნოიდიტი
- კორტიკობაზალური განგლიური დეგენერაცია (თავის ტვინის შეზღუდული ატროფია)
- თავის ტვინის ენცეფალოპათია
- თავის ტკივილი, შაკიკი
- ქალა-ტვინის ტრავმა, თავის ტვინის შერყევა, ტრავმული შეშუპება, კეროვანი და დიფუზური ტრავმა
- შიდა ქალის წნევა და ჰიდროცეფალია
- პარკინსონის დაავადება, პარკინსონიზმი
- ჰიპოფიზის მიკროადენომა, მაკროადენომა და არაფუნქციონირებადი ადენომა (NFPAs), ჰიპერპროლაქტინემიის სინდრომი
- სპონტანური კრანიალური ლიკვორეა