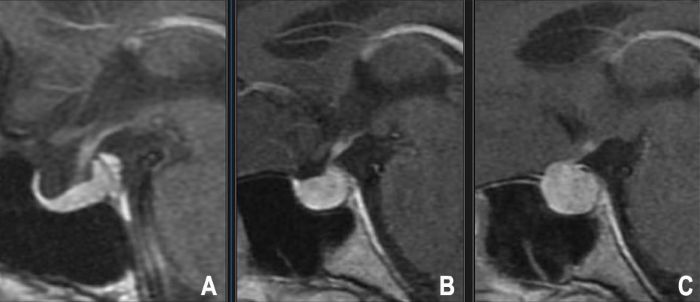
Микроаденома, макроаденома и нефункционирующая аденома гипофиза (NFPAs), синдром гиперпролактинемии
- Обзор аденомы гипофиза (микроаденома, макроаденома) и синдрома гиперпролактинемии
- Микроаденомы гипофиза:
- Макроаденомы гипофиза:
- Нефункционирующие аденомы гипофиза (NFPAs)
- Диагностика аденомы гипофиза и синдрома гиперпролактинемии
- Лечение аденомы гипофиза и синдрома гиперпролактинемии
- Лечение нефункционирующих аденом гипофиза (NFPAs)
- Литература
Обзор аденомы гипофиза (микроаденома, макроаденома) и синдрома гиперпролактинемии
Аденомы гипофиза — это, как правило, доброкачественные (нераковые) опухоли, происходящие из гормон-продуцирующих клеток передней доли гипофиза (аденогипофиза), расположенного у основания головного мозга внутри костной структуры, называемой турецким седлом [1]. Эти аденомы классифицируются в зависимости от размера (микроаденома или макроаденома) и гормональной активности (функционирующие или нефункционирующие).
Синдром гиперпролактинемии относится к клиническим последствиям постоянно повышенного уровня пролактина, гормона, который в норме участвует в лактации. Пролактиномы (пролактин-секретирующие аденомы гипофиза) являются наиболее распространенным типом функционирующей аденомы гипофиза и частой причиной гиперпролактинемии [2]. У женщин симптомы обычно включают галакторею (неадекватную выработку молока), нарушения менструального цикла (олигоменорею или аменорею) и бесплодие. У мужчин гиперпролактинемия часто приводит к снижению либидо, эректильной дисфункции, бесплодию из-за олигоспермии, гинекомастии (увеличению грудных желез) и, реже, галакторее. Повышенный уровень пролактина подавляет секрецию гонадотропин-рилизинг-гормона (ГнРГ) из гипоталамуса, что приводит к вторичному гипогонадизму.
Симптомы, связанные с аденомами гипофиза, возникают либо из-за избыточной секреции гормонов (при функционирующих аденомах), либо из-за физического размера опухоли и давления на окружающие структуры (масс-эффект), особенно при макроаденомах. Синдромы избытка гормонов включают:
Избыток гормона |
Возникающее состояние и основные проблемы со здоровьем |
|---|---|
| Пролактин (ПРЛ) |
Гиперпролактинемия: - Женщины: Менструальная дисфункция (олигоменорея, аменорея), галакторея, бесплодие, снижение плотности костей. - Мужчины: Снижение либидо, эректильная дисфункция, бесплодие, гинекомастия (реже), снижение плотности костной ткани. [2] |
| Гормон роста (ГР) |
Акромегалия (у взрослых) / Гигантизм (у детей): - Увеличение кистей, стоп, черт лица (челюсти, надбровных дуг). - Отек мягких тканей, повышенная потливость. - Остеоартрит, синдром запястного канала. - Апноэ во сне. - Гипертония, кардиомиопатия. - Сахарный диабет или нарушение толерантности к глюкозе. - Повышенный риск колоректальных полипов/рака. [3] |
| Адренокортикотропный гормон (АКТГ) |
Болезнь Кушинга (гипофизарно-зависимый синдром Кушинга): - Центральное ожирение (жир на туловище, лунообразное лицо, "вдовий горб"), истончение кожи, легкое образование синяков, багровые стрии. - Мышечная слабость (проксимальная миопатия), остеопороз. - Изменения настроения (тревога, депрессия, психоз). - Гипертония, сахарный диабет. - Повышенная восприимчивость к инфекциям. - Нарушения менструального цикла (у женщин). [4] |
| Тиреотропный гормон (ТТГ) |
ТТГ-секретирующая аденома (редко): - Вторичный гипертиреоз: Симптомы включают непереносимость жары, потливость, тахикардию/учащенное сердцебиение (аритмии, такие как фибрилляция предсердий), тремор, тревогу/раздражительность, непреднамеренную потерю веса несмотря на повышенный аппетит, зоб. Характеризуется неадекватно нормальным или повышенным ТТГ с повышенными уровнями свободного Т4/Т3. [5] |
| Гонадотропины (ЛГ, ФСГ) |
Гонадотрофная аденома (часто клинически нефункционирующая): - Обычно секретируют неактивные или интактные фрагменты гормонов (например, альфа-субъединицу, бета-ФСГ, реже интактный ФСГ/ЛГ). - В редких случаях может вызывать гиперстимуляцию яичников (у женщин) или увеличение яичек/преждевременное половое созревание (у мужчин). - Чаще всего проявляются из-за масс-эффекта или обнаруживаются случайно. [6] |
Нефункционирующие аденомы гипофиза (NFPAs) не секретируют клинически значимых количеств активных гормонов, хотя многие из них вырабатывают гормональные субъединицы, определяемые специальными тестами. Обычно они вызывают симптомы из-за масс-эффекта, когда становятся макроаденомами, сдавливая прилегающие структуры, такие как перекрест зрительных нервов (вызывая дефекты поля зрения, классически битемпоральную гемианопсию), черепные нервы в кавернозном синусе (вызывая двоение в глазах) или нормальную ткань гипофиза (вызывая гипопитуитаризм — дефицит одного или нескольких гормонов гипофиза). Головные боли также распространены из-за растяжения твердой мозговой оболочки или повышения внутриселлярного давления.
Микроаденомы гипофиза
Описание микроаденом гипофиза
Микроаденома гипофиза определяется как аденома гипофиза с максимальным диаметром менее 10 миллиметров (менее 1 см) [7]. Эти опухоли ограничены турецким седлом и обычно не вызывают симптомов масс-эффекта, таких как потеря зрения. Микроаденомы могут быть как функционирующими (секретирующими гормоны), так и нефункционирующими. Функционирующие микроаденомы вызывают симптомы, связанные со специфическим гормоном, который они перепроизводят (например, пролактинома, вызывающая гиперпролактинемию, АКТГ-секретирующая, вызывающая болезнь Кушинга, ГР-секретирующая, вызывающая акромегалию).
Многие микроаденомы, однако, клинически не функционируют и обнаруживаются случайно во время визуализации головного мозга (магнитно-резонансная томография - МРТ или КТ), выполняемой по другим причинам (например, головная боль, головокружение, травма). Их часто называют гипофизарными «инциденталомами». Хотя подавляющее большинство из них являются доброкачественными находками, требующими только наблюдения, даже небольшие случайные микроаденомы иногда могут вызывать едва заметный гормональный дисбаланс (субклинический Кушинг, легкая гиперпролактинемия) или, редко (< 10% в течение нескольких лет), расти со временем [8].
МРТ с гадолиниевым контрастом, особенно с использованием последовательностей динамического контрастирования и тонких срезов через ямку гипофиза, является методом выбора для выявления микроаденом. Они часто выглядят как небольшие очаговые поражения, которые накапливают контраст менее интенсивно или позже, чем окружающая нормальная ткань гипофиза (обычно гипоинтенсивные на ранних постконтрастных Т1-изображениях) [9].
Клинически значимые микроаденомы чаще всего являются пролактиномами, за которыми следуют АКТГ-секретирующие аденомы, вызывающие болезнь Кушинга, и ГР-секретирующие аденомы, вызывающие акромегалию. Нефункционирующие микроаденомы часто являются гонадотрофными аденомами по данным иммуногистохимии, но не имеют клинического избытка гормонов. Дифференциальный диагноз при визуализации включает кисты кармана Ратке, гиперплазию гипофиза, метастазы или воспалительные процессы (гипофизит), хотя они часто имеют отличительные характеристики или клинический контекст.
Патофизиология микроаденом гипофиза
Аденомы гипофиза, включая микроаденомы, обычно считаются моноклональными новообразованиями, то есть они возникают в результате клональной экспансии одной мутировавшей клетки передней доли гипофиза [10]. Специфические инициирующие мутации и последующие генетические/эпигенетические события, приводящие к образованию аденомы, сложны и разнообразны, но в них вовлечены несколько факторов и путей.
Специфические генетические синдромы зародышевой линии предрасполагают людей к аденомам гипофиза: Множественная эндокринная неоплазия 1 типа (МЭН1), вызванная мутациями в гене-супрессоре опухолей MEN1, часто включает пролактиномы или ГР-секретирующие аденомы. Синдром МакКьюна-Олбрайта, обусловленный мозаичными активирующими мутациями в гене GNAS, кодирующем альфа-субъединицу Gs-белка, часто приводит к ГР-секретирующим аденомам (соматотропиномам). Комплекс Карни (мутации PRKAR1A) может включать аденомы гипофиза (обычно ГР-секретирующие). Мутации в гене AIP (белок, взаимодействующий с рецептором арилуглеводородов) предрасполагают к семейным изолированным аденомам гипофиза (FIPA), в частности ГР-секретирующим или пролактин-секретирующим опухолям, которые часто проявляются в молодом возрасте и бывают более крупными/агрессивными [11].
Спорадические (несемейные) аденомы также включают соматические генетические и эпигенетические изменения. Активирующие соматические мутации в GNAS обнаруживаются примерно в 40 процентах спорадических ГР-секретирующих аденом. Мутации в USP8 часто встречаются в АКТГ-секретирующих аденомах [12]. Другие соматические мутации и эпигенетические изменения, затрагивающие регуляторы клеточного цикла (например, потеря функции CDKN1B/p27, изменения в путях p53, RB), пути факторов роста (например, гиперэкспрессия FGFR4) и специфичные для гипофиза факторы транскрипции, способствуют туморогенезу и выработке гормонов. Также наблюдается потеря гетерозиготности в определенных локусах хромосом (например, 11q13, где находится MEN1).
Пролактиномы, наиболее распространенный тип, возникают из лактотрофных клеток. Кортикотропиномы, вызывающие болезнь Кушинга, возникают из кортикотрофных клеток. Соматотропиномы, вызывающие акромегалию, возникают из соматотрофных клеток. Гонадотропиномы обычно возникают из гонадотрофных клеток и часто секретируют неактивные субъединицы гормонов (альфа-субъединицу, бета-ФСГ, бета-ЛГ). Тиреотропиномы, вызывающие гипертиреоз, возникают из тиреотрофных клеток и встречаются редко.
Большинство клинически нефункционирующих аденом иммунопозитивны к субъединицам гонадотропинов (ФСГ, ЛГ, альфа-субъединица), но не вызывают клинических синдромов избытка гормонов. Некоторые из них могут быть аденомами из «нулевых клеток» без специфического окрашивания гормонов или «молчащими» кортикотрофными/соматотрофными аденомами.
Эпидемиология микроаденом гипофиза
Частота микроаденом гипофиза
Микроаденомы гипофиза на удивление часто являются случайными находками. Исследования аутопсий выявили микроскопические или небольшие аденомы (часто < 3 мм) у 27 процентов людей без известных заболеваний гипофиза [13, 14]. Исследования с использованием визуализации высокого разрешения (МРТ) обнаруживают инциденталомы гипофиза (большинство из которых являются микроаденомами < 10 мм) примерно у 10-20 процентов населения в целом, проходящего сканирование мозга по не связанным с этим причинам [15].
Подавляющее большинство этих случайно обнаруженных микроаденом являются нефункционирующими и остаются стабильными или растут очень медленно, никогда не вызывая клинических симптомов. Функционирующие микроаденомы встречаются гораздо реже, но они являются обычной причиной синдромов избытка гормонов гипофиза, таких как гиперпролактинемия (пролактинома — наиболее частый клинически диагностируемый тип, предполагаемая распространенность ~10-50 на 100 000 населения [16]), болезнь Кушинга и акромегалия.
Микроаденомы гипофиза могут возникать в любом возрасте, но чаще всего диагностируются у молодых людей и людей среднего возраста (от 20 до 50 лет). Существует преобладание женщин для пролактином (соотношение Ж:М ~10:1) и болезни Кушинга (~3-5:1), в то время как ГР-секретирующие аденомы имеют примерно равное распределение по полу.
До широкого использования МРТ гиперпролактинемия, выявляемая с помощью анализов крови, была основным ключом к выявлению лежащих в основе, часто невидимых, пролактин-секретирующих микроаденом. МРТ теперь позволяет осуществлять прямую визуализацию.
Высокая распространенность случайно обнаруженных микроаденом по сравнению с более низкой распространенностью клинически значимых заболеваний гипофиза или макроаденом свидетельствует о том, что большинство микроаденом не прогрессируют в крупные или симптомные опухоли.
Макроаденомы гипофиза
Описание макроаденом гипофиза
Макроаденома гипофиза определяется как аденома гипофиза с максимальным диаметром 10 миллиметров (1 см) или более [3]. В отличие от микроаденом, макроаденомы часто выходят за пределы турецкого седла, потенциально сдавливая окружающие нервные и сосудистые структуры.
Они могут быть как функционирующими (секретирующими гормоны), так и нефункционирующими. Нефункционирующие аденомы гипофиза (NFPAs) являются наиболее распространенным типом макроаденом, диагностируемых клинически [6]. Функционирующие макроаденомы включают крупные пролактиномы, ГР-секретирующие аденомы, вызывающие акромегалию, и реже крупные АКТГ-секретирующие аденомы (часто связанные с синдромом Нельсона после адреналэктомии) или ТТГ-секретирующие аденомы.
Макроаденомы часто проявляются симптомами, связанными с масс-эффектом из-за их размера:
- Нарушения зрения: Сдавление перекреста зрительных нервов, расположенного над гипофизом, часто встречается при супраселлярном распространении, классически вызывая битемпоральную гемианопсию (потерю периферического зрения в обоих наружных височных полях). Сдавление зрительных нервов или трактов может вызывать другие виды потери зрения или снижение остроты зрения.
- Параличи черепных нервов: Латеральное распространение в кавернозный синус может сдавливать черепные нервы III (глазодвигательный), IV (блоковый), V (тройничный - V1 глазная и V2 верхнечелюстная ветви) и VI (отводящий), что приводит к двоению в глазах (диплопии), опущению век (птозу), изменениям зрачков или онемению/боли лица. ЧМН III и VI клинически поражаются чаще всего.
- Головные боли: Часто неспецифические, потенциально из-за растяжения твердой мозговой оболочки, покрывающей седло (диафрагма турецкого седла), или повышения внутриселлярного давления.
- Гипопитуитаризм: Сдавление и разрушение нормальной ткани гипофиза может привести к дефициту одного или нескольких гормонов передней доли гипофиза (дефицит ГР часто возникает раньше всего, за ним следуют гонадотропины ЛГ/ФСГ, вызывающие гипогонадизм, затем ТТГ, вызывающий вторичный гипотиреоз, и, наконец, АКТГ, вызывающий вторичную надпочечниковую недостаточность) или, реже, к дисфункции задней доли гипофиза (дефицит антидиуретического гормона - АДГ, вызывающий центральный несахарный диабет, чаще наблюдается при сдавлении ножки или поражениях, исходящих кзади).
- Апоплексия гипофиза: Острое неотложное состояние, вызванное внезапным кровоизлиянием или инфарктом в аденоме гипофиза (гораздо чаще встречается при макроаденомах, чем при микроаденомах). Проявляется внезапной сильной головной болью, быстрой потерей зрения, параличами черепных нервов, изменением сознания и часто острым гипопитуитаризмом (требующим срочной заместительной терапии стероидами).
Функционирующие макроаденомы также вызывают симптомы, связанные с перепроизводством гормонов, часто более тяжелые, чем при микроаденомах из-за большей опухолевой массы, как описано ранее.
Патофизиология макроаденом гипофиза
Основная патофизиология включает клональную экспансию мутировавших аденогипофизарных клеток, подобно микроаденомам. Факторы, стимулирующие прогрессирование от микроаденомы к макроаденоме или развитие макроаденом de novo, не полностью выяснены, но, вероятно, включают накопление дополнительных генетических (например, мутации в генах-супрессорах опухолей, таких как p53, хромосомная нестабильность) или эпигенетических изменений, способствующих усилению пролиферации, снижению апоптоза, ангиогенезу и иногда инвазивности [10].
Макроаденомы часто демонстрируют потерю нормальных механизмов обратной связи, контролирующих секрецию гормонов (особенно функционирующих). Их рост приводит к сдавлению и разрушению соседних нормальных клеток гипофиза, что приводит к гипопитуитаризму. Распространение кверху сдавливает перекрест зрительных нервов и, возможно, гипоталамус (приводя к несахарному диабету или нарушению регуляции аппетита/температуры). Латеральное распространение проникает в кавернозный синус, потенциально охватывая внутреннюю сонную артерию и черепные нервы III, IV, V1, V2 и VI. Распространение книзу может разрушать дно турецкого седла в клиновидную пазуху, иногда вызывая ринорею спинномозговой жидкости (ликворею).
Генетическая основа включает факторы, упомянутые для микроаденом, включая синдромы зародышевой линии (MEN1, GNAS, AIP, комплекс Карни) и соматические мутации (GNAS, USP8). Дополнительные изменения, связанные с более крупными или более агрессивными опухолями, могут включать мутации в регуляторах клеточного цикла (p53, RB), рецепторах факторов роста (FGFR4) или молекулах адгезии. Несмотря на гистологическую доброкачественность (низкий митотический индекс, обычно отсутствие цитологической атипии), некоторые макроаденомы демонстрируют инвазивный характер роста в окружающие структуры (твердую мозговую оболочку, кость, кавернозный синус), что затрудняет полную хирургическую резекцию. Истинные первичные карциномы гипофиза, определяемые наличием краниоспинальных или системных метастазов, встречаются крайне редко.
Сопутствующие клинические синдромы, такие как МЭН1, МакКьюна-Олбрайта и комплекс Карни, могут включать макроаденомы, часто ГР-секретирующих или пролактин-секретирующих типов.
Эпидемиология макроаденом гипофиза
Частота макроаденом гипофиза
В то время как случайные микроаденомы встречаются очень часто, клинически значимые опухоли гипофиза, требующие оценки и потенциального лечения, встречаются реже. Общая распространенность клинически явных аденом гипофиза оценивается примерно в 78-94 на 100 000 человек, или примерно 1 на 1000 [17, 18]. Макроаденомы составляют значительную долю этих клинически значимых опухолей, вероятно, составляя 30-50% диагностированных аденом, особенно среди нефункционирующих аденом, которые часто проявляются из-за размера.
Популяционные исследования предполагают, что общая ежегодная заболеваемость впервые диагностированными аденомами гипофиза составляет около 4 на 100 000 населения [18], причем показатели распространенности увеличиваются благодаря улучшению выявления с помощью визуализации. Заболеваемость, требующая нейрохирургического вмешательства, колеблется от примерно 1 до 7 на 100 000 в год, при этом макроаденомы, вызывающие масс-эффект или избыток гормонов, невосприимчивый к медикаментозной терапии, являются основными показаниями к хирургическому вмешательству.
Заболеваемость и смертность при макроаденоме гипофиза
Заболеваемость, связанная с макроаденомами гипофиза, в первую очередь проистекает из масс-эффектов (потеря зрения, параличи черепных нервов, изнурительные головные боли), гормональной дисфункции (гипопитуитаризм, требующий пожизненного замещения, или системные последствия синдромов избытка гормонов, таких как акромегалия или болезнь Кушинга), а также потенциальных осложнений лечения (например, хирургические риски, такие как утечка ликвора, менингит, повреждение сосудов, усугубление гипопитуитаризма; долгосрочные эффекты облучения, такие как гипопитуитаризм, вторичные опухоли, когнитивные изменения). Нарушение зрения, особенно необратимый дефицит из-за несвоевременного лечения компрессии хиазмы, значительно снижает качество жизни. Гипопитуитаризм требует тщательного ведения и несет в себе собственные риски в случае неадекватного лечения (например, адреналовый криз). Осложнения неконтролируемого избытка гормонов (например, сердечно-сосудистые заболевания, диабет, остеопороз, повышенный риск развития рака при акромегалии и болезни Кушинга) вносят значительный вклад в долгосрочную заболеваемость и смертность, если ими эффективно не управлять [19, 20].
Смертность, непосредственно связанная с доброкачественной природой самих макроаденом гипофиза, обычно низкая. Однако повышенный риск смертности хорошо документирован у пациентов с неконтролируемой акромегалией и болезнью Кушинга, в первую очередь из-за сердечно-сосудистых осложнений (гипертония, сердечная недостаточность, инсульт, аритмии), проблем с обменом веществ (диабет) и инфекций (Кушинг). Апоплексия гипофиза, хотя и редко встречается, может привести к летальному исходу, если не распознать и не лечить ее своевременно. Осложнения хирургического вмешательства (хотя смертность низкая, <1%, в опытных центрах) или долгосрочные эффекты лучевой терапии также могут вносить свой вклад. Общая выживаемость пациентов с макроаденомами в целом хорошая при современном многопрофильном лечении, которое контролирует уровень гормонов и масс-эффект, хотя качество жизни может страдать из-за остаточных симптомов или побочных эффектов лечения.
Макроаденомы гипофиза не демонстрируют значительной расовой предрасположенности.
Хотя исследования аутопсий показывают одинаковую распространенность случайных аденом у обоих полов, клинически диагностированные пролактиномы и АКТГ-секретирующие аденомы (болезнь Кушинга) значительно чаще встречаются у женщин репродуктивного возраста, возможно, из-за более раннего распознавания симптомов (нарушения менструального цикла, галакторея). ГР-секретирующие аденомы (акромегалия) и клинически проявляющиеся NFPAs имеют более равномерное распределение по полу. Макроаденомы гипофиза могут возникать в любом возрасте, но чаще всего диагностируются у взрослых, при этом пик заболеваемости приходится на период между третьим и шестым десятилетиями.
Нефункционирующие аденомы гипофиза (NFPAs)
Нефункционирующие аденомы гипофиза (NFPAs) — это опухоли гипофиза, которые не вызывают клинического синдрома избыточной секреции гормонов. Они составляют примерно 15-30 процентов всех клинически диагностируемых аденом гипофиза и являются наиболее распространенным типом, проявляющимся в виде макроаденом [22]. Несмотря на название «нефункционирующие», иммуногистохимическое окрашивание показывает, что большинство NFPAs происходят из гонадотрофных клеток и часто вырабатывают гонадотропные гормоны (фолликулостимулирующий гормон - ФСГ, лютеинизирующий гормон - ЛГ) или их субъединицы (особенно альфа-субъединицу или ФСГ-бета субъединицу), но эти гормоны обычно биологически неактивны, секретируются неэффективно или секретируются в аномальных соотношениях, таким образом, не вызывая клинических симптомов избытка гормонов[6]. Некоторые из них могут быть истинными аденомами из «нулевых клеток» или «молчащими» вариантами других гормон-продуцирующих клеток.
Поскольку у них отсутствуют синдромы гиперсекреции гормонов, NFPAs обычно проявляются позже, чем функционирующие аденомы, часто когда они вырастают достаточно большими (макроаденомы), чтобы вызывать симптомы из-за масс-эффекта:
- Дефекты полей зрения (как правило, битемпоральная гемианопсия из-за сдавления перекреста зрительных нервов).
- Головные боли (неспецифические, из-за растяжения твердой мозговой оболочки или давления в седле).
- Гипопитуитаризм (из-за сдавления нормальной ткани гипофиза, чаще всего в первую очередь страдает секреция ГР и гонадотропинов, затем ТТГ и АКТГ).
- Параличи черепных нервов (реже, из-за инвазии в кавернозный синус, вызывающей диплопию или онемение лица).
- Апоплексия гипофиза (острое кровоизлияние/инфаркт внутри опухоли).
Многие небольшие NFPAs обнаруживаются случайно (МРТ или КТ) как гипофизарные инциденталомы. Результаты вскрытий и визуализационных исследований предполагают высокую распространенность "молчащих" микроаденом (потенциально у 1 из 6 человек), но большинство из них остаются небольшими и бессимптомными на протяжении всей жизни.
Основным методом лечения симптомных NFPAs, вызывающих масс-эффект или прогрессирующий гипопитуитаризм, является хирургическая резекция, обычно транссфеноидальным доступом. Основными целями являются декомпрессия окружающих структур (особенно зрительного аппарата для улучшения/сохранения зрения) и максимально безопасное удаление опухоли для уменьшения масс-эффекта и потенциального улучшения функции гипофиза. Ведение бессимптомных случайных NFPAs включает наблюдение с помощью серийной визуализации и эндокринных/зрительных оценок [23].
Диагностика аденомы гипофиза и синдрома гиперпролактинемии
Дифференциальная диагностика селлярных/супраселлярных образований
| Состояние | Ключевые особенности / Отличительные признаки | Типичные данные визуализации (МРТ) |
|---|---|---|
| Аденома гипофиза (Микро/Макро) | Эндокринные симптомы (избыток/дефицит) или масс-эффект (потеря зрения, головная боль, паралич ЧМН). Исходит из седла, смещает железу, может распространяться супра/параселлярно. | Микро: Очаговое поражение <10 мм, обычно гипоинтенсивное на Т1, накапливает контраст меньше/позже, чем нормальная железа. Макро: Селлярное образование ≥10 мм, вариабельное контрастирование (часто меньше, чем железа), может иметь кровоизлияния/кисты, распространяется супра/параселлярно, может разрушать кость. |
| Краниофарингиома | Бимодальный возрастной пик (дети/пожилые люди). Частое супраселлярное расположение. Головные боли, потеря зрения, эндокринная дисфункция (дефицит ГР, несахарный диабет (НД) часто), гидроцефалия. | Часто смешанные кистозные (Т1 вариабельно/Т2 гипер-) и солидные компоненты. Очень часто кальцификация (лучше всего на КТ). Накапливает контраст (солидные части, толстая стенка кисты). Типично супраселлярный эпицентр, может спаиваться с окружающими структурами. |
| Менингиома (Селлярная/Супраселлярная/Кавернозного синуса) | Взрослые, обычно Ж>М. Медленно растущая, исходящая из твердой мозговой оболочки (planum sphenoidale, tuberculum sellae, диафрагма, стенка кавернозного синуса). Масс-эффект (потеря зрения, параличи ЧМН), головная боль, судороги. Редко значительная эндокринная дисфункция, если не очень большая. | Часто изоинтенсивна на Т1/Т2, интенсивное гомогенное контрастирование после контраста, характерен симптом "дурального хвоста". Может вызывать гиперостоз (утолщение кости) или обрастать сосуды. |
| Киста кармана Ратке | Доброкачественная эпителиальная киста (остаток кармана Ратке), часто случайная. Может вызывать головную боль, нарушения зрения или гипопитуитаризм, если она большая. Обычно внутриселлярное или интра/супраселлярное расположение по средней линии. | Четко очерченная киста, не накапливающая контраст (обычно). Сигнал сильно варьируется (Т1 гипер/изо/гипо, Т2 обычно гипер-) в зависимости от белкового содержимого. Тонкая, гладкая стенка, обычно без солидного компонента или контрастирования (может быть тонкий ободок). Возможен внутрикистозный узелок (белковый/геморрагический) (<30%). |
| Гиперплазия гипофиза | Увеличение нормальной ткани железы. Физиологическая (беременность, лактация, половое созревание) или патологическая (реакция на отказ органа-мишени, например первичный гипотиреоз, первичная недостаточность надпочечников). | Диффузно увеличенная железа (возможна высота >10-12 мм), обычно контрастируется гомогенно и интенсивно. Седло может симметрично увеличиваться. Форма железы сохраняется (утрачивается вогнутая верхняя граница). Разрешается, если лечить основную причину. |
| Гипофизит (Лимфоцитарный, Гранулематозный, IgG4) | Воспаление гипофиза/ножки. Головная боль, нарушения зрения, гипопитуитаризм (часто быстрое начало, множественные оси), часто НД (особенно при вовлечении ножки). Лимфоцитарный часто в послеродовом/аутоиммунном контексте. | Часто симметричное увеличение и утолщение железы/ножки, диффузное интенсивное контрастирование. Может имитировать аденому, но часто более инфильтративный вид ножки. Клинический контекст имеет решающее значение (быстрое начало гипопитуитаризма/НД). |
| Метастаз | Анамнез первичного рака (чаще всего молочной железы, легкого). Быстрое начало гипопитуитаризма, часто НД (предрасположенность к задней доле гипофиза/ножке). Возможны головная боль, потеря зрения, параличи ЧМН. | Образование, накапливающее контраст, часто инфильтративное, часто вовлекает заднюю долю гипофиза или ножку. Могут быть множественные внутричерепные поражения. Поиск первичного злокачественного новообразования является ключевым. |
| Аневризма (Кавернозная/Супраселлярная ВСА) | Может имитировать селлярное образование, особенно если частично тромбирована. Может вызывать параличи ЧМН (III, IV, V, VI из-за расположения в кавернозном синусе), головную боль. Риск разрыва (САК). | МРТ показывает характерное выпадение сигнала от тока крови (если проходима), слоистый сигнал тромба (если есть), контрастирование стенки. МРА/КТА/ЦДСА подтверждает диагноз и описывает анатомию сосудов. |
| Хордома / Хондросаркома | Редкие злокачественные/местно-агрессивные опухоли основания черепа, возникающие из остатков хорды (хордома) или хряща (хондросаркома). Могут распространяться в седло/супраселлярную область от ската/верхушки пирамиды. Часто вызывают обширную деструкцию кости, параличи ЧМН. | КТ показывает деструкцию кости. МРТ показывает местно-деструктивное образование, накапливающее контраст, часто гиперинтенсивное на Т2 (особенно хордома из-за физалиформных клеток). Расположение обычно центрировано на скате или петрокливальном соединении. |
| Герминома (Супраселлярная) | Редкая герминогенная опухоль, обычно у детей/молодых людей. Классическая триада: НД, потеря зрения, гипопитуитаризм. Может одновременно поражать пинеальную область ("двойные опухоли средней линии"). | Гомогенно контрастирующееся супраселлярное образование, часто вовлекает перекрест зрительных нервов, ножку/гипоталамус. Опухолевые маркеры в ликворе/сыворотке (АФП, β-ХГЧ) могут быть повышены (хотя часто в норме при чистой герминоме). Высоко радиочувствительна. |
Диагностика часто включает магнитно-резонансную томографию (МРТ) гипофиза — золотой стандарт для визуализации аденом (микроаденом, макроаденом, включая пролактиномы), оценки их размера, распространенности, связи с окружающими структурами, такими как перекрест зрительных нервов и кавернозные синусы, и помощи в дифференциации от других селлярных поражений.
Диагностический подход сочетает в себе клиническую оценку, гормональное тестирование и визуализацию:
- Клиническое подозрение: Основано на симптомах избытка гормонов (например, признаки акромегалии, кушингоидные признаки, галакторея/аменорея), масс-эффекта (изменения зрения, головная боль, паралич черепных нервов), гипопитуитаризма (усталость, гипогонадизм, непереносимость холода и т. д.) или случайной находке при визуализации.
- Гормональная оценка: Измерение базального уровня гормонов передней доли гипофиза и гормонов их органов-мишеней необходимо для выявления избытка или дефицита гормонов. Ключевые тесты включают:
- Пролактин (ПРЛ): Повышенные уровни указывают на гиперпролактинемию. Значительно повышенные уровни (>200-250 нг/мл или мкг/л) с высокой вероятностью указывают на пролактиному (особенно макроаденому). Умеренно повышенные уровни (25-150 нг/мл) требуют оценки других причин (лекарства, гипотиреоз, эффект ножки и т. д.). Проверьте наличие «хук-эффекта» с разбавленным образцом, если присутствует макроаденома, а ПРЛ неожиданно низкий/нормальный [24].
- Гормон роста (ГР) / Инсулиноподобный фактор роста 1 (ИФР-1): Повышенный ИФР-1 с поправкой на возраст и пол является лучшим скрининговым тестом на акромегалию. Диагноз подтверждается отсутствием подавления ГР (< 0,4 или < 1 нг/мл в зависимости от анализа) во время перорального глюкозотолерантного теста (ПГТТ). Базальные уровни ГР менее надежны из-за пульсирующего характера секреции.
- АКТГ / Кортизол: Скрининг на синдром Кушинга включает такие тесты, как уровень кортизола в слюне поздно вечером, уровень свободного кортизола в суточной моче (UFC) или ночной дексаметазоновый подавляющий тест с низкой дозой (1 мг). При положительном результате уровни АКТГ в плазме помогают дифференцировать АКТГ-зависимые (гипофизарные/эктопические) причины от независимых (надпочечниковых). Дексаметазоновые подавляющие тесты с высокими дозами и/или тесты стимуляции КРГ, иногда в сочетании с забором крови из нижних каменистых синусов (IPSS), помогают подтвердить гипофизарное происхождение (болезнь Кушинга) [4].
- ТТГ / Свободный Т4/Т3: Повышенный или неадекватно нормальный ТТГ при повышенных уровнях свободного Т4/Т3 указывает на редкую ТТГ-секретирующую аденому. Тестирование также позволяет провести скрининг на первичный гипотиреоз (высокий ТТГ, низкий св. Т4), потенциальную причину вторичной гиперпролактинемии.
- ЛГ / ФСГ / Тестостерон (у мужчин) / Эстрадиол (у женщин): Оценка функции гонад. Низкие уровни указывают на гипогонадизм (вторичный, если ЛГ/ФСГ также низкие/нормальные). Повышение альфа-субъединицы часто встречается при гонадотрофных аденомах.
- Оценка гипопитуитаризма: Если масс-эффект или симптомы указывают на дефицит, проверьте базовые утренние уровни кортизола и АКТГ, ТТГ и свободного Т4, ЛГ/ФСГ и тестостерона/эстрадиола (в зависимости от ситуации), ИФР-1 (для оси ГР). Динамические стимуляционные тесты (например, тест стимуляции АКТГ, тест на толерантность к инсулину — золотой стандарт, но рискованный, тест с ГРРГ-аргинином) могут понадобиться для подтверждения незначительных дефицитов. Оцените наличие несахарного диабета (НД), если вовлечена задняя доля гипофиза (полиурия, полидипсия, осмоляльность сыворотки/мочи).
- Визуализация:
- МРТ гипофиза: С контрастированием гадолинием и без него, с использованием специальных тонких срезов (≤3 мм) через седло в корональной и сагиттальной плоскостях. Последовательности динамического контрастирования особенно полезны для выявления микроаденом, которые часто выглядят как очаговые области с отсроченным накоплением контраста по сравнению с быстро накапливающей контраст нормальной передней долей гипофиза. МРТ точно определяет размер опухоли, ее отношение к перекресту зрительных нервов, инвазию в кавернозный синус (классификация Knosp) и отклонение ножки [25].
- КТ-сканирование: Менее чувствительно для самих аденом, но лучше показывает костную эрозию дна седла или клиновидных отростков, а также кальцификации (чаще встречаются при краниофарингиомах). Полезно, если МРТ противопоказана.
- Офтальмологическое обследование: Формальное исследование полей зрения (обычно автоматизированная периметрия, например, поле зрения Хамфри) обязательно, если аденома находится рядом или сдавливает перекрест зрительных нервов (макроаденомы), даже если пациент не сообщает о симптомах со стороны зрения. Оценка остроты зрения и внешнего вида зрительного нерва (офтальмоскопия на наличие бледности/атрофии или папилледемы) также является стандартной.
- Дифференциальная диагностика гиперпролактинемии: Если обнаружен повышенный уровень пролактина, систематически исключайте другие причины перед постановкой диагноза пролактиномы, особенно если уровни повышены лишь умеренно (<150 нг/мл) или визуализация в норме/сомнительна. Учитывайте:
- Физиологические причины: Беременность, лактация, стресс, сон (проверяйте утренние уровни), физические упражнения, стимуляция сосков, половой акт.
- Лекарства: Изучите принимаемые в настоящее время препараты (антипсихотики — особенно рисперидон, типичные; антидепрессанты — СИОЗС, ТЦА; противорвотные средства — метоклопрамид, домперидон; антигипертензивные средства — верапамил, метилдопа; опиоиды; эстрогены). По возможности отмените подозреваемый препарат и повторно проверьте ПРЛ примерно через 3 дня (или дольше, в зависимости от периода полувыведения).
- Системные состояния: Первичный гипотиреоз (проверьте ТТГ/св. Т4), хроническая болезнь почек (проверьте креатинин), тяжелый цирроз печени, синдром поликистозных яичников (СПКЯ), поражения грудной стенки (опоясывающий герпес, хирургические шрамы, пирсинг).
- Эффект ножки гипофиза: Сдавление ножки гипофиза непролактинсекретирующими опухолями (NFPAs, краниофарингиомы, менингиомы) или воспалительными поражениями прерывает доставку дофамина от гипоталамуса к лактотрофам, что приводит к легкой/умеренной гиперпролактинемии (обычно <150 нг/мл). Ключевое значение имеет визуализация.
- Макропролактинемия: Наличие крупных, биологически менее активных комплексов пролактина; требует специфического лабораторного тестирования (преципитация ПЭГ); клинически, как правило, не имеет значения.
Нормальные уровни пролактина в сыворотке немного различаются в зависимости от лаборатории и метода анализа, но в целом составляют (примерные диапазоны):
Группа пациентов |
Примерный нормальный диапазон пролактина (нг/мл или мкг/л) |
(Примерные единицы СИ: мМЕ/л) |
|---|---|---|
Дети (до полового созревания) |
Вариабельно, обычно < 15-20 | ~ < 300-400 |
Взрослые мужчины |
< 15-20 | ~ < 300-400 |
Небеременные взрослые женщины |
< 25-30 | ~ < 500-600 |
Беременные женщины |
Значительно повышен, увеличивается на протяжении беременности (например, до 200-400+ нг/мл) | ~ до 4000-8000+ мМЕ/л |
Послеродовой период (лактирующие) |
Повышен, уровни колеблются при грудном вскармливании, постепенно снижаются, если не кормит грудью | Вариабельно, может быть очень высоким первоначально |
Коэффициент пересчета приблизительный (1 нг/мл ≈ 21 мМЕ/л на основе стандартов ВОЗ, но варьируется в зависимости от анализа).
Лечение аденомы гипофиза и синдрома гиперпролактинемии
Цели лечения аденом гипофиза заключаются в нормализации уровней гормонов (в случае их избытка), облегчении симптомов масс-эффекта (потеря зрения, головная боль, параличи черепных нервов), сохранении или восстановлении нормальной функции гипофиза и предотвращении рецидива опухоли. Конкретный подход во многом зависит от типа аденомы (функционирующая или нефункционирующая), размера (микро- или макро-), секретируемого гормона, наличия и выраженности масс-эффекта, возраста пациента, репродуктивных планов и сопутствующих заболеваний [26, 2, 4, 23].
- Пролактиномы (Гиперпролактинемия):
- Медикаментозная терапия (Первая линия): Агонисты дофамина (АД) обладают высокой эффективностью и являются предпочтительным начальным лечением практически для всех пролактином, включая крупные макроаденомы, вызывающие дефекты полей зрения (за исключением случаев, когда потеря зрения тяжелая/быстро прогрессирует).
- Каберголин: Как правило, предпочтительнее из-за более высокой эффективности в нормализации пролактина и уменьшении размера опухолей, более длительного периода полувыведения, позволяющего дозировать один или два раза в неделю, и лучшей переносимости по сравнению с бромокриптином.
- Бромокриптин: Более старый препарат, требует ежедневного приема, чаще связан с тошнотой/постуральной гипотензией, но имеет более длительную историю безопасности, особенно при беременности.
- Хирургия (Нейрохирургическое вмешательство - Транссфеноидальная хирургия): Показана в первую очередь пациентам, не переносящим агонисты дофамина или резистентным к ним, пациентам с апоплексией гипофиза в пролактиноме, в редких случаях с крупными кистозными/геморрагическими компонентами, не реагирующими на АД, или иногда женщинам, желающим забеременеть, которые не могут переносить или хотят избежать приема АД. Показатели излечения выше для микроаденом (~70-90%), чем для инвазивных макроаденом (~30-50%).
- Лучевая терапия (Стереотаксическая радиохирургия или фракционированная ЛТ): Зарезервирована для редких случаев инвазивных/агрессивных пролактином, резистентных к максимальной медикаментозной и хирургической терапии или рецидивирующих после нее. Используется в первую очередь для контроля опухоли, так как влияние на уровень пролактина происходит медленно и часто не полностью; высокий риск гипопитуитаризма.
- Медикаментозная терапия (Первая линия): Агонисты дофамина (АД) обладают высокой эффективностью и являются предпочтительным начальным лечением практически для всех пролактином, включая крупные макроаденомы, вызывающие дефекты полей зрения (за исключением случаев, когда потеря зрения тяжелая/быстро прогрессирует).
- Акромегалия (ГР-секретирующие аденомы):
- Хирургия (Обычно первая линия): Транссфеноидальная хирургия является основным методом лечения, направленным на полную резекцию и биохимическое излечение (нормализация ИФР-1 с поправкой на возраст/пол и подавление ГР во время ПГТТ). Показатели излечения зависят от размера опухоли, инвазивности и опыта хирурга.
- Медикаментозная терапия: Используется при персистирующем заболевании после операции, у пациентов, которым операция не подходит, или иногда в предоперационном периоде для улучшения результатов операции. Варианты включают:
- Лиганды рецепторов соматостатина (SRLs): Первое поколение (октреотид LAR, ланреотид Autogel) нормализуют ИФР-1/ГР примерно у 50-60% и могут уменьшить опухоли. Второе поколение (пасиреотид LAR) может быть эффективным, если SRLs первого поколения не помогают, но несет более высокий риск гипергликемии.
- Антагонист рецептора ГР (Пегвисомант): Высокоэффективен в нормализации ИФР-1 (~80-90%) путем блокирования действия ГР на рецептор; не уменьшает опухоль и требует мониторинга функции печени и размера опухоли.
- Агонисты дофамина (Каберголин): Менее эффективен, нормализует ИФР-1 только примерно в 10-30% случаев, в основном используется в качестве дополнительной терапии, особенно если опухоль совместно секретирует пролактин.
- Лучевая терапия (Стереотаксическая или фракционированная): Эффективна для контроля роста опухоли и медленного снижения уровней ГР/ИФР-1 у пациентов с остаточным/рецидивирующим заболеванием, не реагирующим на медикаментозную терапию. Высокий риск отсроченного гипопитуитаризма.
- Болезнь Кушинга (АКТГ-секретирующие аденомы):
- Хирургия (Первая линия): Транссфеноидальная селективная аденомэктомия является методом выбора, направленным на биохимическую ремиссию с сохранением нормальной функции гипофиза. Частота ремиссии составляет ~70-90% для микроаденом в опытных центрах [27].
- Медикаментозная терапия: Используется перед операцией для контроля тяжелого гиперкортизолизма, после операции при персистирующем/рецидивирующем заболевании в ожидании эффектов ЛТ, или в качестве первичной терапии, если операция не удалась/противопоказана. Препараты нацелены на стероидогенез в надпочечниках (кетоконазол, метирапон, этомидат, осилодростат), секрецию АКТГ гипофизом (пасиреотид, каберголин) или блокаду глюкокортикоидных рецепторов (мифепристон).
- Лучевая терапия (Стереотаксическая или фракционированная): Эффективна при персистирующем/рецидивирующем заболевании после операции, но биохимическая ремиссия отсрочена (от месяцев до лет).
- Двусторонняя адреналэктомия: Обеспечивает окончательное излечение от гиперкортизолизма, если терапия, направленная на гипофиз, не дает результатов, но приводит к стойкой надпочечниковой недостаточности, требующей пожизненной заместительной терапии глюкокортикоидами/минералокортикоидами, и несет риск развития синдрома Нельсона (прогрессирующий рост/пигментация АКТГ-секретирующей опухоли гипофиза).
- ТТГ-омы (редко):
- Хирургия (Первая линия): Транссфеноидальная резекция является предпочтительным методом лечения.
- Медикаментозная терапия: Лиганды рецепторов соматостатина (октреотид, ланреотид) часто эффективны в подавлении секреции ТТГ и уменьшении размеров опухолей перед операцией или при остаточном заболевании. Антитиреоидные препараты (метимазол, ПТУ) устраняют симптомы гипертиреоза, но не лечат опухоль.
- Лучевая терапия: При остаточных/рецидивирующих опухолях, не реагирующих на другие методы лечения.
- Нефункционирующие аденомы гипофиза (NFPAs): См. раздел ниже.
Решения по ведению должны быть индивидуализированы и часто требуют междисциплинарного командного подхода с участием эндокринологов, нейрохирургов, нейрорадиологов, офтальмологов, а иногда и радиационных онкологов.
Лечение нефункционирующих аденом гипофиза (NFPAs)
Поскольку NFPAs обычно не вызывают синдромов избытка гормонов, лечение показано в первую очередь, когда они вызывают масс-эффект (нарушение зрения, параличи черепных нервов, клинически значимые головные боли, связанные с опухолью) или гипопитуитаризм, или если они демонстрируют значительный рост при серийной визуализации [22, 23].
- Бессимптомные случайные NFPAs:
- Микроаденомы (<10 мм): Обычно лечатся консервативно с помощью периодического МРТ-контроля (например, МРТ через 1 год, затем через 1-2 года, затем реже, если они стабильны) и базовой эндокринной оценки (скрининг на гипопитуитаризм и гиперпролактинемию из-за эффекта ножки). Большинство (~90-95%) существенно не растут [8].
- Макроаденомы (≥10 мм) без масс-эффекта (нет зрительных дефицитов, нормальная функция гипофиза, не прилегают к хиазме): Ведение индивидуально. Варианты включают тщательное наблюдение с помощью МРТ (например, через 6 месяцев, затем ежегодно, если стабильно) и регулярные эндокринные/зрительные оценки, или рассмотрение возможности хирургического вмешательства, особенно если опухоль большая или находится очень близко к перекресту зрительных нервов, учитывая потенциал будущего роста/осложнений. Вмешательство показано при наличии документально подтвержденного роста опухоли, развития симптомов (потеря зрения, гипопитуитаризм) или если опухоль начинает прилегать к/сдавливать перекрест зрительных нервов [23].
- Симптомные NFPAs (Вызывающие масс-эффект или гипопитуитаризм):
- Хирургическое вмешательство (Первая линия): Транссфеноидальная хирургия является основным методом лечения. Основными целями являются декомпрессия зрительного аппарата для улучшения/сохранения зрения и максимально безопасное удаление опухоли для облегчения масс-эффекта и потенциального восстановления функции гипофиза (менее вероятно, если дефицит существует давно). В настоящее время широко используются эндоскопические эндоназальные доступы. Полная резекция часто бывает затруднительной для крупных или инвазивных (например, в кавернозный синус) опухолей.
- Лучевая терапия (Стереотаксическая радиохирургия - СРХ или фракционированная ЛТ): Показана в первую очередь как адъювантное лечение при значительной остаточной опухоли после операции (особенно если она растет или имеет большой остаточный объем) или при рецидивирующих опухолях. Первичная ЛТ используется редко, если операция не противопоказана. ЛТ обеспечивает отличные показатели долгосрочного контроля опухоли (>90%), но не сразу уменьшает масс-эффект и несет значительный отсроченный риск (~30-60% в течение 10 лет) радиационно-индуцированного гипопитуитаризма [28].
- Медикаментозная терапия: В настоящее время не существует эффективной медикаментозной терапии, которая бы стабильно уменьшала NFPAs или предотвращала их рост. Агонисты дофамина или аналоги соматостатина изучались, но в целом неэффективны при типичных гонадотрофных NFPAs.
- Лечение гипопитуитаризма: Гормональный дефицит, выявленный до или после лечения, требует соответствующей и пожизненной физиологической заместительной терапии (например, гидрокортизон при надпочечниковой недостаточности - необходимо покрытие стрессовыми дозами; левотироксин при вторичном гипотиреозе; тестостерон/эстроген +/- прогестерон при гипогонадизме; потенциально заместительная терапия ГР у взрослых с подтвержденным дефицитом и значительным влиянием на качество жизни или метаболические параметры; десмопрессин (DDAVP) при несахарном диабете, если он присутствует).
- Долгосрочное наблюдение: Обязательно после лечения (операция +/- облучение) для всех макроаденом. Включает мониторинг рецидива или повторного роста опухоли (серийные МРТ, частота зависит от остаточной опухоли/типа лечения), регулярную оценку эндокринной функции (ежегодное тестирование на гипопитуитаризм, в том числе после ЛТ) и мониторинг зрительного статуса (поля зрения при наличии в анамнезе компрессии). Частота рецидивов после одной только хирургической операции может быть значительной с течением времени (10-50% в зависимости от продолжительности наблюдения и остаточной опухоли), что требует рассмотрения адъювантной лучевой терапии при наличии вызывающей опасения остаточной опухоли.
![]() Внимание! Аденомы гипофиза требуют специализированной диагностики и лечения многопрофильной командой. Такие симптомы, как изменения зрения, постоянные головные боли, гормональный дисбаланс (изменения менструального цикла, лактация, необъяснимые физические изменения, половая дисфункция) или чрезмерная усталость, требуют оценки врачом, что может привести к направлению к эндокринологу и нейрохирургу.
Внимание! Аденомы гипофиза требуют специализированной диагностики и лечения многопрофильной командой. Такие симптомы, как изменения зрения, постоянные головные боли, гормональный дисбаланс (изменения менструального цикла, лактация, необъяснимые физические изменения, половая дисфункция) или чрезмерная усталость, требуют оценки врачом, что может привести к направлению к эндокринологу и нейрохирургу.
Литература
- Melmed S. Pituitary-Tumor Endocrinopathies. N Engl J Med. 2020 Mar 5;382(10):937-950. doi: 10.1056/NEJMra1810772
- Melmed S, Casanueva FF, Hoffman AR, et al. Diagnosis and Treatment of Hyperprolactinemia: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2011 Feb;96(2):273-88. doi: 10.1210/jc.2010-1692
- Katznelson L, Laws ER Jr, Melmed S, et al; Endocrine Society. Acromegaly: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2014 Nov;99(11):3933-51. doi: 10.1210/jc.2014-2700
- Nieman LK, Biller BM, Findling JW, et al. The diagnosis of Cushing's syndrome: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2008 May;93(5):1526-40. doi: 10.1210/jc.2008-0125
- Beck-Peccoz P, Persani L. Thyrotropin-secreting pituitary adenomas. N Engl J Med. 1996;334(11):712-713. doi: 10.1056/NEJM199603143341107
- Ntali G, Wass JA. Epidemiology, clinical presentation and diagnosis of non-functioning pituitary adenomas. Pituitary. 2011 Jun;14(2):111-8. doi: 10.1007/s11102-011-0300-1
- Molitch ME. Pituitary incidentalomas. Endocrinol Metab Clin North Am. 1997 Mar;26(1):1-17. doi: 10.1016/s0889-8529(05)70239-7
- Fernández-Balsells MM, Murad MH, Barwise A, et al. Clinical management of nonfunctioning pituitary adenomas (NFPAs): a systematic review and meta-analysis. J Clin Endocrinol Metab. 2011 Apr;96(4):905-15. doi: 10.1210/jc.2010-1921
- Chapter on Pituitary Imaging. In: Osborn AG, Salzman KL, Jhaveri MD, et al. Osborn's Brain. 2nd ed. Elsevier; 2018.
- Asa SL, Ezzat S. The pathogenesis of pituitary tumours. Nat Rev Cancer. 2002 Feb;2(2):83-94. doi: 10.1038/nrc760
- Vierimaa O, et al. Pituitary adenoma predisposition caused by germline mutations in the AIP gene. Science. 2006 May 26;312(5777):1228-30. doi: 10.1126/science.1126100
- Reincke M, et al. Mutations in the deubiquitinase gene USP8 cause Cushing's disease. Nat Genet. 2015 Jan;47(1):31-8. doi: 10.1038/ng.3166
- Costello RT. Subclinical adenoma of the pituitary gland. Am J Pathol. 1936 Mar;12(2):205-16.1.
- Ezzat S, Asa SL, Couldwell WT, et al. The prevalence of pituitary adenomas: a systematic review. Cancer. 2004 Aug 1;101(3):613-9. doi: 10.1002/cncr.20412
- Hall WA, et al. Pituitary magnetic resonance imaging in normal human volunteers: occult adenomas in the general population. Ann Intern Med. 1994 May 15;120(10):817-20. doi: 10.7326/0003-4819-120-10-199405150-00001
- Ciccarelli A, et al. High prevalence of pituitary adenomas: a cross-sectional study in the province of Varese, Italy. J Clin Endocrinol Metab. 2001 Feb;86(2):720-5. doi: 10.1210/jcem.86.2.7204
- Fernandez A, et al. Prevalence of pituitary adenomas: a community-based study in Olmsted County, Minnesota, 1993-1997. Arch Intern Med. 2000 Jan 10;160(1):78-81. doi: 10.1001/archinte.160.1.78
- Daly AF, et al. High prevalence of pituitary adenomas: a cross-sectional study in the province of Liege, Belgium. J Clin Endocrinol Metab. 2006 Dec;91(12):4756-69. doi: 10.1210/jc.2006-1668
- Melmed S. Acromegaly pathogenesis and treatment. J Clin Invest. 2009 Mar;119(3):429-38. doi: 10.1172/JCI38090
- Nieman LK. Cushing's syndrome: update on signs, symptoms and biochemical screening. Eur J Endocrinol. 2015 Oct;173(4):M33-8. doi: 10.1530/EJE-15-0464
- Elster AD, et al. Pituitary gland: MR imaging of physiologic hypertrophy in adolescence. Radiology. 1990;174(3 Pt 1):681-5. doi: 10.1148/radiology.174.3.2305044
- Molitch ME. Nonfunctioning pituitary adenomas. Pituitary. 2005;8(3-4):213-20. doi: 10.1007/s11102-006-8512-6
- Freda PU, Beckers AM, Katznelson L, et al; Endocrine Society. Pituitary incidentaloma: an endocrine society clinical practice guideline. J Clin Endocrinol Metab. 2011 Apr;96(4):894-904. doi: 10.1210/jc.2010-1048
- Frieze TW, et al. Hook effect in prolactinomas: case report and review of literature. Endocr Pract. 2006;12(3):296-303. doi: 10.4158/EP.12.3.296
- Bonneville F, et al. Radiology of pituitary adenomas: an update. Radiol Clin North Am. 2012 Nov;50(6):995-1013. doi: 10.1016/j.rcl.2012.08.005
- Melmed S, et al. Guidelines for acromegaly management: an update. J Clin Endocrinol Metab. 2009;94(5):1509-17. doi: 10.1210/jc.2008-2421
- Nieman LK, Biller BMK, Findling JW, et al. Treatment of Cushing's Syndrome: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2015 Aug;100(8):2807-31. doi: 10.1210/jc.2015-1818
- Sheehan JP, et al. Radiosurgery for nonfunctioning pituitary adenomas: a systematic review. J Neurosurg. 2013 Aug;119(2):446-56. doi: 10.3171/2013.4.JNS121833
Смотрите также
- Анатомия нервной системы
- Инфекционные заболевания головного мозга:
- Абсцесс полушарий головного мозга и мозжечка
- Эозинофильная гранулёма, лангергансоклеточный гистиоцитоз, фистульный симптом Эннебера
- Абсцесс эпидуральный
- Внутричерепные осложнения заболеваний носа
- Внутричерепные осложнения заболеваний уха
- Глазничные осложнения заболеваний носа
- Менингит гнойный отогенный
- Тромбофлебит сигмовидного синуса и септикопиемия
- Коллоидная киста головного мозга 3 мозгового желудочка
- Арахноидит церебральный и оптико-хиазмальный
- Кортикобазальная ганглиозная дегенерация (ограниченная атрофия головного мозга)
- Энцефалопатия
- Головная боль, мигрень
- Черепно-мозговая травма (сотрясение, ушиб мозга, ДАП)
- Внутричерепное давление (гипертензия, гипотензия) и гидроцефалия
- Паркинсона болезнь
- Аденома гипофиза (микроаденома, макроаденома, нефункционирующая аденома), синдром гиперпролактинемии
- Спонтанная краниальная ликворея