Арахноидит церебральный, оптико-хиазмальный, спинальный
Обзор арахноидита
Арахноидит — это воспалительное заболевание, поражающее паутинную оболочку (арахноидальную), одну из трех мозговых оболочек, окружающих головной и спинной мозг. Это воспаление приводит к утолщению, рубцеванию и образованию спаек (патологических соединений) между паутинной и мягкой мозговыми оболочками (лептоменинксом), потенциально вовлекая нервные корешки, кровеносные сосуды и препятствуя току спинномозговой жидкости (ликвора) [1]. Хотя процесс и называется «арахноидит», воспалительный процесс обычно затрагивает соседние менингеальные слои и не изолирован исключительно в паутинной оболочке. Некоторые рассматривают его как форму хронического локализованного серозного менингита из-за вовлечения других слоев и путей ликвора. Тем не менее, его отчетливая клиническая картина, характеризующаяся хронической болью, неврологическими дефицитами и возможностью нарушений тока ликвора, оправдывает его выделение в отдельное заболевание.
Причины возникновения арахноидита
Арахноидит развивается как ответ на различные повреждения, которые провоцируют воспаление в субарахноидальном пространстве. Общие причины и способствующие факторы включают[2, 3]:
- Инфекции: Перенесенный бактериальный, грибковый, вирусный или паразитарный менингит или миелит (воспаление спинного мозга). Туберкулезный менингит является известной причиной.
- Осложнения спинальной хирургии: Особенно множественные или сложные операции (синдром неудачно оперированного позвоночника - FBSS), когда может возникнуть кровотечение в субарахноидальное пространство или прямое раздражение. Разрывы твердой мозговой оболочки во время операции являются фактором риска.
- Спинальная анестезия/Процедуры: Эпидуральная или спинальная анестезия (особенно многократные попытки или травматичные пункции, приводящие к кровотечению), миелография с использованием старых контрастных веществ на масляной основе (в настоящее время применяется редко) или интратекальные инъекции (например, химиотерапия, стероиды - особенно депо-препараты, хотя это весьма спорно).
- Травма: Значительная прямая травма позвоночника или головного мозга (ЧМТ, травма спинного мозга), приводящая к кровоизлиянию или воспалению в субарахноидальном пространстве.
- Субарахноидальное кровоизлияние: Продукты распада крови (например, железо) в ликворе обладают сильным раздражающим действием и могут вызывать воспалительную реакцию, приводящую к образованию спаек.
- Хроническая интоксикация/Химическое раздражение: Воздействие определенных токсинов или раздражителей, введенных в пространство ликвора. Хронический алкоголизм предлагался в качестве способствующего фактора в некоторой литературе.
- Воспалительные состояния: Системные воспалительные заболевания, поражающие ЦНС (например, саркоидоз). Реактивное воспаление вторично по отношению к смежным процессам, таким как хронические тяжелые грыжи межпозвонковых дисков или медленно растущие опухоли (например, шванномы, менингиомы).
- Идиопатические: В значительном числе случаев выявить конкретную причину не удается.
Морфологически паутинная оболочка становится утолщенной, непрозрачной и фиброзной. Между паутинной и мягкой мозговыми оболочками образуются спаечные тяжи, привязывающие нервные корешки (при спинальной форме) или охватывающие черепные нервы и кровеносные сосуды (при церебральной форме). Эти спайки могут перекрывать субарахноидальное пространство, препятствовать току ликвора и приводить к образованию кист, заполненных ликвором (арахноидальные кисты или локуляции) [4].
Арахноидит часто описывается как диффузный, поражающий широкую область, но часто проявляет более тяжелые, локализованные изменения в рамках этого диффузного процесса, что приводит к очаговым симптомам. Нарушение циркуляции ликвора является основным последствием. Блокада путей оттока ликвора (например, отверстий Лушки и Мажанди при арахноидите задней черепной ямки) может вызвать окклюзионную гидроцефалию. Нарушение всасывания ликвора через воспаленные или рубцово-измененные арахноидальные грануляции может привести к сообщающейся гидроцефалии.
Виды арахноидита
Церебральный арахноидит (оболочки головного мозга)
Церебральный арахноидит включает воспаление и рубцевание паутинной оболочки, окружающей головной мозг. Он может локализоваться в определенных областях, таких как выпуклая поверхность (конвекситальная) мозга, базальные цистерны (пространства ликвора в основании мозга) или задняя черепная ямка. Клиническая картина является результатом комбинации генерализованных воспалительных эффектов, местного сдавления или раздражения подлежащей ткани мозга и черепных нервов спайками или кистами, а также нарушений циркуляции ликвора, приводящих к гидроцефалии или локализованному скоплению ликвора [5]. Общим симптомом для разных локализаций является головная боль, часто описываемая как диффузная, постоянная и потенциально усиливающаяся при маневрах, повышающих внутричерепное давление (гипертензивная головная боль или «оболочечная» головная боль).
Конвекситальный церебральный арахноидит
Конвекситальный церебральный арахноидит поражает паутинную оболочку, покрывающую поверхность (конвекситет) полушарий головного мозга, чаще всего передние области и области вокруг центральной борозды (роландова область). Воспаление и спайки здесь могут непосредственно раздражать или сдавливать подлежащую кору головного мозга. Это может привести к очаговым неврологическим нарушениям, таким как двигательные расстройства (монопарез или гемипарез из-за вовлечения моторной коры) и сенсорные нарушения (парестезии, онемение). Корковое раздражение часто проявляется очаговыми судорогами, которые иногда могут генерализоваться. Образование кист внутри спаек может усугубить компрессию и увеличить вероятность судорог, потенциально прогрессируя до эпилептического статуса в тяжелых случаях [6]. Диагностические инструменты, такие как электроэнцефалография (ЭЭГ), могут помочь локализовать эпилептогенные очаги, в то время как нейровизуализация (МРТ) имеет важное значение для визуализации спаек, скоплений ликвора и любых подлежащих кортикальных изменений.
Оптико-хиазмальный арахноидит
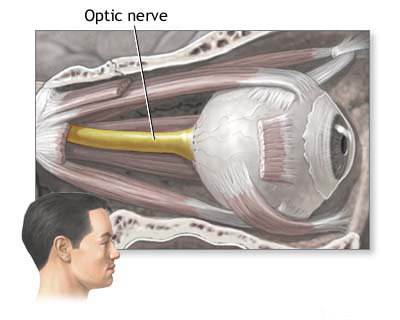
Арахноидит, локализованный в базальных цистернах, встречается часто, при этом опто-хиазмальная область (вокруг зрительных нервов, перекреста зрительных нервов и основания лобных долей) является частым местом. Оптико-хиазмальный арахноидит особенно важен из-за его способности вызывать тяжелую и часто необратимую потерю зрения. Общие предшествующие причины включают инфекции, распространяющиеся из близлежащих пазух (синусит), глотки, или системные инфекции, такие как сифилис или туберкулез, а также черепно-мозговую травму или субарахноидальное кровоизлияние [5].
Патологически воспаление приводит к образованию плотных спаек и иногда кист, которые охватывают зрительные нервы, хиазму и соседние структуры, такие как стебель гипофиза и гипоталамус. Процесс редко бывает строго локализованным, часто тонко распространяясь на окружающие базальные цистерны. Повреждение зрительных путей является результатом прямого сдавления спайками/кистами, воспалительного поражения нервов/хиазмы (компонент неврита зрительного нерва) и нарушения кровоснабжения (ишемия).
Клинически оптико-хиазмальный арахноидит обычно проявляется постепенной, прогрессирующей потерей зрения, которая часто начинается с одной стороны, но обычно становится двусторонней в течение недель или месяцев. Это медленное прогрессирование помогает отличить его от острого ретробульбарного неврита. Тяжесть варьируется от легкой нечеткости до полной слепоты. Боль за глазами (ретробульбарная боль) может возникать на ранних стадиях заболевания. Внутричерепная гипертензия обычно слабая или отсутствует при этой локализованной форме.
Офтальмологическое обследование является ключевым. Тестирование полей зрения (периметрия) выявляет дефекты, соответствующие месту максимального поражения вдоль зрительных путей. Типичные паттерны включают битемпоральную гемианопсию (указывающую на компрессию хиазмы), узловые скотомы, центральные скотомы (часто двусторонние) или концентрическое сужение полей зрения [8].
Решающее значение имеет исследование глазного дна. Атрофия зрительного нерва (бледность диска зрительного нерва) развивается со временем и наблюдается в большинстве случаев (60-65 процентов), отражая повреждение нерва. Оно может быть первичным (прямое повреждение нерва) или вторичным (после первоначального отека диска). Отек диска зрительного нерва (из-за повышенного ВЧД) встречается реже (10-13 процентов), чем атрофия в этой преимущественно базальной форме. Дисфункция гипоталамуса или гипофиза обычно отсутствует, если спайки не являются обширными. Визуализация турецкого седла обычно в норме, что помогает отличить заболевание от опухолей гипофиза.
Арахноидит задней черепной ямки
Арахноидит с поражением задней черепной ямки является наиболее частой формой локализованного церебрального арахноидита, часто связанного с предшествующими инфекциями уха (средний отит, мастоидит) или менингитом[5]. Его клиническая картина может точно имитировать опухоли задней черепной ямки (например, невриному слухового нерва, менингиому, опухоль мозжечка). Симптомы возникают в результате вовлечения мозжечка, ствола мозга и выходящих в этой области черепных нервов, а также в результате обструкции тока ликвора, приводящей к гидроцефалии.
Общие локализации включают мостомозжечковый угол (ММУ), большую цистерну и область вокруг выходов из четвертого желудочка (отверстия Лушки и Мажанди). Арахноидит ММУ обычно вовлекает черепные нервы VIII (потеря слуха, шум в ушах, головокружение), V (онемение/боль лица) и VII (слабость лицевых мышц). Часто встречаются мозжечковые признаки, такие как атаксия (неустойчивая походка, плохая координация), дисметрия, адиадохокинез и нистагм. Сдавление ствола мозга может вызвать пирамидные знаки или параличи других черепных нервов.
Нарушение оттока ликвора из четвертого желудочка спайками или кистами легко вызывает окклюзионную гидроцефалию, что приводит к симптомам повышенного внутричерепного давления (головная боль, тошнота, рвота, отек диска зрительного нерва). Проявления зависят от баланса между воспалением, образованием спаек/кист и развитием гидроцефалии. Течение может быть острым, подострым или хроническим.
Острая форма часто проявляется преимущественно симптомами повышенного ВЧД (сильная головная боль, часто в затылочной области, рвота, головокружение, отек дисков зрительных нервов, иногда брадикардия), тогда как очаговые неврологические симптомы вначале могут быть слабовыраженными или отсутствовать.
При подострой или хронической формах могут преобладать очаговые симптомы, особенно связанные с поражением ММУ. Вестибулярная дисфункция является частой, включая спонтанный нистагм (часто нестабильный, может менять направление или быть позиционным), нестабильность походки с падением в сторону поражения и аномальные вестибулярные функциональные тесты (калорические или вращательные тесты могут показать дисгармонию). Потеря слуха (нейросенсорная) часто встречается при вовлечении VIII нерва. Возможны параличи черепных нервов V, VI, VII, IX и X. Пирамидные знаки обычно выражены слабо, если нет значительного сдавления ствола мозга.
Специфическая локализация в пределах задней черепной ямки может давать различные синдромы, такие как изолированное вовлечение вестибулярного нерва, предпонтинный арахноидит, вызывающий проблемы с равновесием, или поражение яремного отверстия, затрагивающее нервы IX, X и XI.
Отогенная гидроцефалия, вторичная по отношению к арахноидиту задней черепной ямки, проявляется главным образом симптомами повышенного ВЧД, часто сопровождающимися вестибулярными расстройствами или легкими мозжечковыми признаками. Анализ ликвора может быть нормальным или показывать низкий уровень белка.
Быстро прогрессирующая окклюзионная гидроцефалия может привести к острым кризам с сильной головной болью, рвотой, изменением сознания, а также к возможному отеку дисков зрительных нервов и потере зрения. Опасным для жизни осложнением является вклинение миндалин мозжечка через большое затылочное отверстие из-за высокого давления, сдавливающее продолговатый мозг и вызывающее остановку дыхания.
Арахноидит задней черепной ямки также может быть сложной причиной трудноизлечимой невралгии тройничного нерва из-за вовлечения зоны входа корешка V нерва.
Спинальный арахноидит (оболочки спинного мозга)
Спинальный арахноидит включает воспаление и рубцевание паутинной оболочки, окружающей спинной мозг и нервные корешки в позвоночном канале. Причины отражают причины церебрального арахноидита, причем предшествующие операции на позвоночнике, спинальная анестезия/процедуры, травмы, инфекции (менингит, миелит) и субарахноидальное кровоизлияние являются частыми триггерами [1]. Это также может быть связано с системными воспалительными состояниями.
Спайки привязывают спинной мозг и нервные корешки, препятствуют току ликвора в субарахноидальном пространстве спинного мозга и могут нарушить кровоснабжение. Это обычно приводит к хроническим, прогрессирующим неврологическим симптомам. Клиническая картина часто напоминает симптомы экстрамедуллярной опухоли спинного мозга или стеноза позвоночного канала. Общие характеристики включают:
- Хроническая боль: Часто наиболее выраженный и изнуряющий симптом. Обычно нейропатического характера (жгучая, колющая, стреляющая боль), чаще всего затрагивающая спину, ноги или промежность.
- Радикулопатия: Симптомы, связанные с поражением определенных нервных корешков, включая иррадиирующую боль, онемение, покалывание и слабость в зоне иннервации пораженного(ых) корешка(ов).
- Миелопатия: Симптомы дисфункции спинного мозга из-за компрессии, ишемии или сопутствующего образования сиринго (полость с жидкостью внутри спинного мозга). Это включает слабость или спастичность в конечностях, дефицит сенсорного уровня, нарушение походки и дисфункцию кишечника/мочевого пузыря.
Спинальный арахноидит чаще всего поражает поясничный и грудной отделы, часто затрагивая конский хвост (нервные корешки в конце спинного мозга). Процесс обычно вовлекает несколько нервных корешков. Сенсорные нарушения могут быть неоднородными и изменчивыми. Анализ ликвора может показать повышенный уровень белка (белково-клеточная диссоциация) из-за застоя ликвора ниже уровня обструкции, но плеоцитоз встречается редко, если нет активного воспаления. Миелография (КТ или МРТ) необходима для диагностики, классически показывая слипание нервных корешков, прилипание корешков к периферии дурального мешка (симптом «пустого мешка»), ограниченные скопления ликвора или блокировку тока контраста. МРТ является предпочтительным методом визуализации [9].
Спинальный арахноидит, как правило, является хроническим, часто прогрессирующим заболеванием, которое очень трудно поддается эффективному лечению.
Диагностика арахноидита
Диагностика арахноидита требует интеграции клинических данных (анамнез, симптомы, неврологический осмотр) с подтверждающими данными диагностических тестов, в первую очередь нейровизуализации и иногда анализа ликвора. Установить окончательную причину часто бывает сложно.
Дифференциальная диагностика арахноидита
| Состояние | Ключевые особенности / Отличительные признаки | Типичные данные визуализации / лаборатории |
|---|---|---|
| Арахноидит (Слипчивый) | Хроническая боль (часто нейропатическая), прогрессирующий неврологический дефицит (радикулопатия, миелопатия, параличи черепных нервов). История потенциального триггера (инфекция, хирургия, САК, травма, контраст). | МРТ: Слипание нервных корешков/смещение на периферию ("пустой дуральный мешок"), скопления ликвора/кисты, стертое субарахноидальное пространство, +/- утолщение/контрастирование оболочек (часто слабое/отсутствует в хронической стадии). Ликвор: Часто высокое содержание белка (ниже блока), нормальный/умеренный плеоцитоз. |
| Менингит (Бактериальный, Грибковый, ТБ) | Острое/подострое начало. Лихорадка, головная боль, ригидность затылочных мышц, измененный психический статус. Могут быть параличи черепных нервов. | МРТ: Диффузное лептоменингеальное контрастирование. Ликвор (ЛП крайне важна): Плеоцитоз (нейтрофилы при бактериальном, лимфоциты при вирусном/ТБ/грибковом), низкая глюкоза (бактериальный, ТБ, грибковый), высокий белок. Положительная окраска по Граму/посев/ПЦР. |
| Лептоменингеальный карциноматоз / Метастазы | История известного первичного рака. Мультифокальные неврологические признаки (черепные нервы, спинномозговые корешки, гидроцефалия). Головная боль, когнитивные изменения. Подострое начало. | МРТ: Узелковое или линейное лептоменингеальное контрастирование, может вовлекать нервные корешки/конский хвост ("сахарная глазурь"). Ликвор: Злокачественные клетки на цитологии (может потребоваться повторная ЛП), высокий белок, низкая глюкоза. Системное стадирование определяет первичный очаг. |
| Спинальный стеноз (Дегенеративный) | Нейрогенная перемежающаяся хромота (боль/слабость в ногах при ходьбе, облегчающаяся при отдыхе/сгибании). Боль в спине часто. Обычно пожилая возрастная группа. Как правило, нет истории воспалительного триггера. | МРТ/КТ: Сужение спинномозгового канала/отверстий из-за выбухания диска, гипертрофии фасеточных суставов, утолщения желтой связки, сдавливающей дуральный мешок/корешки. Нет первичных менингеальных изменений или диффузного слипания корешков. |
| Опухоль спинного мозга (Интрадуральная-Экстрамедуллярная - Менингиома, Шваннома) | Прогрессирующая миелопатия/радикулопатия в зависимости от локализации. Боль часто. Обычно паттерн очагового дефицита. | МРТ: Хорошо очерченное, часто интенсивно контрастирующее *образование*, смещающее спинной мозг/нервные корешки. Менингиома часто исходит из твердой мозговой оболочки; шваннома возникает из корешка (возможна форма "гантели"). Обычно нет диффузных спаек/слипания корешков. |
| Опухоль спинного мозга (Интрамедуллярная - Эпендимома, Астроцитома) | Прогрессирующая миелопатия (сенсорный уровень, слабость, изменения кишечника/мочевого пузыря). Боль вначале менее типична, чем при экстрамедуллярной. Обычно симптомы поражения центрального шнура. | МРТ: Расширение спинного мозга, внутренняя Т2-гиперинтенсивность, вариабельный паттерн контрастного усиления (эпендимома часто контрастируется интенсивно). Может сопровождаться сиринго или опухолевыми кистами. |
| Сирингомиелия | Полость, заполненная жидкостью, внутри спинного мозга. Часто вызывает синдром центрального шнура (диссоциированная потеря чувствительности - в первую очередь страдает болевая/температурная чувствительность, распределение по типу «куртки»), слабость/атрофию. Может быть вторичной по отношению к арахноидиту. | МРТ: Четко определяет интрамедуллярную кистозную полость (сиринкс). Важно искать основную причину (мальформация Киари, опухоль, посттравматическая, поствоспалительная/арахноидит). |
| Поперечный миелит | Острое/подострое начало миелопатии (слабость, сенсорный уровень, дисфункция кишечника/мочевого пузыря). Часто постинфекционный или аутоиммунный. Возможна боль. | МРТ: Интрамедуллярная Т2-гиперинтенсивность +/- контрастирование, обычно охватывающая несколько сегментов центрально. Ликвор может показать плеоцитоз/высокий белок/олигоклональные полосы. Специфические антитела (AQP4, MOG). |
| Внутричерепная гипотензия (часто из-за спонтанной утечки ликвора) | Ортостатическая головная боль (хуже в вертикальном положении, лучше в положении лежа) является отличительной чертой. Вызывается утечкой ликвора. Может вызывать диффузное пахименингеальное (дуральное) контрастирование, *не* лептоменингеальное. | МРТ: Диффузное, гладкое пахименингеальное контрастирование, "провисание" ствола мозга, субдуральные скопления/гигромы. ЛП (если выполняется) показывает низкое начальное давление. Миелография/КТ/МРТ миелография может выявить место утечки. |
| Синдром Гийена-Барре (СГБ) / ХВДП | Острая (СГБ) или хроническая (ХВДП) полирадикулоневропатия. Восходящая слабость, арефлексия, сенсорные изменения. В первую очередь поражает корешки периферических нервов, а не непосредственно мозговые оболочки. Боль часто. | МРТ: Может показать контрастирование корешков спинномозговых нервов/конского хвоста (особенно передних корешков). Ликвор: Белково-клеточная диссоциация (высокий белок, нормальные/низкие клетки) - классическая находка. ЭНМГ является диагностической. |
Магнитно-резонансная томография (МРТ) является основным инструментом для визуализации изменений, связанных с арахноидитом, таких как утолщение мозговых оболочек, спайки, слипание нервных корешков или скопления ликвора. Это видео может демонстрировать типичные результаты МРТ.
Ключевые диагностические подходы включают:
- Клиническая оценка: Решающее значение имеет подробный анамнез, ориентированный на потенциальные причины (инфекция, операция, травма, кровоизлияние, анестезия) и характер/прогрессирование симптомов (хроническая боль, специфические неврологические дефициты). Неврологическое обследование направлено на локализацию дефицитов (черепные нервы, двигательные/сенсорные пути, мозжечковая функция, корешки спинномозговых нервов).
- Нейровизуализация:
- МРТ головного мозга или МРТ спинного мозга (с контрастным усилением гадолинием и без него): Метод выбора [10, 9]. Данные могут включать:
- Утолщение и контрастное усиление лептоменинкса (паутинной/мягкой оболочек) после введения гадолиния (усиление может присутствовать при активном воспалении, но часто отсутствует или слабо выражено на хронических, чисто спаечных стадиях).
- Облитерация нормальных пространств ликвора или аномальное скопление/локуляция ликвора.
- *Специфично для спинного мозга:* Слипание нервных корешков в центре дурального мешка, прилипание корешков по периферии к дуральному мешку (симптом «пустого мешка») или нервные корешки, заключенные в утолщенные мозговые оболочки.
- Образование арахноидальных кист или скоплений ликвора (выглядят как скопления с интенсивностью сигнала жидкости на Т2-взвешенных изображениях, могут иметь тонкие контрастирующие стенки).
- Сопутствующие данные, такие как гидроцефалия (церебральная), сирингомиелия (полость спинного мозга) или изменения в подлежащей паренхиме головного/спинного мозга (например, отек, изменение сигнала Т2, указывающее на глиоз или миеломаляцию).
- КТ-миелография: Может использоваться при спинальном арахноидите, если МРТ противопоказана или не дает результатов. Может показать блокировку тока контраста, неровные края столба контраста, слипание нервных корешков, ампутацию корешковых манжеток или скопление контраста внутри кист/локуляций. Менее чувствительна, чем МРТ, для визуализации утолщения мозговых оболочек или внутренних изменений спинного мозга.
- Рентгенография или КТ черепа/позвоночника: Как правило, не используется для диагностики самого арахноидита, но может показать признаки повышенного ВЧД (например, эрозию турецкого седла при хронической гидроцефалии) или костные изменения, связанные с предыдущей операцией или травмой.
- МРТ головного мозга или МРТ спинного мозга (с контрастным усилением гадолинием и без него): Метод выбора [10, 9]. Данные могут включать:
- Анализ спинномозговой жидкости (ликвора): Получается путем люмбальной пункции (ЛП), только если это считается безопасным (т.е. нет признаков высокого ВЧД или полного спинального блока, подтвержденных визуализацией). Результаты часто неспецифичны при хроническом слипчивом арахноидите. Может наблюдаться повышенный уровень белка (особенно ниже спинального блока из-за застоя ликвора), легкий плеоцитоз (повышенное количество клеток, обычно лимфоцитов) в некоторых активных воспалительных фазах, или может быть совершенно нормальным. В первую очередь полезно для исключения активной инфекции (менингита) или злокачественного новообразования (лептоменингеальный карциноматоз).
- Электроэнцефалография (ЭЭГ): Может помочь локализовать эпилептогенную активность у пациентов с конвекситальным церебральным арахноидитом, проявляющимся судорогами. Может показать диффузное замедление в случаях со значительной гидроцефалией или диффузным поражением головного мозга, но, как правило, неспецифично для самого арахноидита.
- Офтальмологическое обследование: Включая осмотр глазного дна (на предмет отека диска зрительного нерва или атрофии зрительного нерва) и исследование поля зрения (периметрия), необходимо при подозрении на оптико-хиазмальный арахноидит или арахноидит задней черепной ямки, вызывающие зрительные симптомы или признаки повышенного ВЧД.
Дифференцировать арахноидит от других состояний, особенно опухолей (менингиомы, шванномы, эпендимомы, метастатического заболевания), бывает сложно только на основании визуализации, особенно при локализованных кистозных формах. Требуются клинический анамнез, анализ ликвора (особенно цитология на злокачественность) и иногда хирургическая биопсия. По сравнению с опухолями, арахноидит часто имеет более диффузное или многоуровневое поражение, менее интенсивное контрастирование на хронических стадиях (хотя активное воспаление может контрастироваться) и историю, указывающую на воспалительный триггер.
Лечение арахноидита
Лечение арахноидита часто бывает сложным и в первую очередь направлено на устранение симптомов, особенно хронической боли и неврологических дефицитов, поскольку обратить вспять основные рубцы и спайки трудно или невозможно. Окончательного лечения не существует [11].
Стратегии лечения включают:
- Медикаментозное лечение:
- Контроль боли: Это часто является основой и требует мультимодального подхода. Варианты включают препараты для лечения нейропатической боли (например, габапентин, прегабалин, трициклические антидепрессанты, такие как амитриптилин, СИОЗСН, такие как дулоксетин), НПВС для воспалительных компонентов и иногда, с осторожностью, опиоиды для сильной, рефрактерной боли (долгосрочное использование проблематично из-за толерантности, зависимости и побочных эффектов).
- Противовоспалительные препараты: Кортикостероиды (пероральные или внутривенные) могут использоваться кратковременно во время задокументированных острых воспалительных обострений или потенциально в послеоперационном периоде, но их долгосрочная польза при хроническом слипчивом арахноидите не доказана и вызывает споры из-за значительных побочных эффектов. Другие иммуномодуляторы применяются редко, если нет основного системного воспалительного заболевания.
- Миорелаксанты: При сопутствующих мышечных спазмах (например, баклофен).
- Физиотерапия: Легкие упражнения (избегая обострения), растяжка, гидротерапия и ЧЭНС (чрескожная электронейростимуляция) могут помочь справиться с болью, сохранить функцию и подвижность и предотвратить детренированность.
- Интервенционное лечение боли:
- Эпидуральные инъекции стероидов (блокады) (применение весьма спорно и потенциально рискованно при установленном арахноидите, может ухудшить состояние некоторых пациентов).
- Стимуляция спинного мозга (SCS): Имплантация устройства для доставки электрических импульсов к задним столбам спинного мозга может обеспечить значительное облегчение боли у некоторых пациентов с хронической нейропатической болью преимущественно в конечностях [12].
- Интратекальные системы доставки лекарств (Болевые помпы): Имплантированные помпы, доставляющие обезболивающие препараты (например, морфин, зиконотид, баклофен) непосредственно в ликворное пространство, могут рассматриваться при сильной, рефрактерной боли, когда другие варианты не помогают, но требуют тщательного отбора пациентов и контроля [12].
- Адгезиолизис (процедура Раца): Чрескожный лизис эпидуральных спаек инъекцией гипертонического раствора/местного анестетика/стероида; эффективность конкретно при интрадуральном арахноидите сомнительна и несет в себе риски.
- Хирургическое вмешательство: Операция обычно резервируется для определенных осложнений или прогрессирующего неврологического дефицита и направлена на декомпрессию нервных структур или восстановление тока ликвора, а не на «излечение» самого арахноидита. Процедуры часто технически сложны, с вариабельными исходами и риском ухудшения симптомов или повторного образования спаек [2, 6]. Варианты включают:
- Лизис спаек: Микрохирургическая диссекция для освобождения привязанных нервных корешков или спинного мозга. Результаты часто бывают временными, так как спайки имеют тенденцию к повторному образованию. Несет в себе значительные риски, включая повреждение нерва и утечку ликвора. В настоящее время редко выполняется при диффузном заболевании.
- Фенестрация или иссечение кисты: Создание отверстий в симптомных арахноидальных кистах/локуляциях, вызывающих значительную компрессию, или их удаление.
- Дуральное шунтирование / Экспансивная дуропластика: Иногда используется после лизиса спаек или удаления кисты, чтобы попытаться расширить пространство и потенциально предотвратить рецидив, с ограниченным доказанным успехом.
- Шунтирование ликвора (например, вентрикулоперитонеальный [ВП] шунт): Необходимо для лечения сопутствующей симптомной гидроцефалии.
- Сирингосубарахноидальный или сирингоперитонеальный шунт: Для дренирования симптомного сопутствующего сиринкса, вызывающего прогрессирующую миелопатию.
- Хирургия при оптико-хиазмальном арахноидите: Микрохирургическая декомпрессия зрительных нервов и хиазмы путем рассечения спаек и фенестрации кист может быть предпринята в срочном порядке при быстром ухудшении зрения, но результаты в отношении восстановления зрения вариабельны и часто разочаровывают; риски включают дальнейшее повреждение [5].
- Лечение основной причины: Если выявлен текущий инфекционный или специфический воспалительный процесс (что редко бывает на хронической стадии), необходимо целенаправленное лечение (например, антибиотики, специфическая иммуномодуляция).
Пневмоэнцефалография, исторически упоминавшаяся в старой литературе для диагностики и иногда попыток терапии (вдувание воздуха), устарела и больше не используется, уступив место МРТ и КТ.
Прогноз при арахноидите весьма вариабелен, но часто осторожный, особенно при спинальной форме. Хотя заболевание, как правило, не представляет прямой угрозы для жизни (если оно не осложнено тяжелой нелеченой гидроцефалией или сдавлением ствола мозга), оно часто вызывает хроническую изнуряющую боль и прогрессирующие неврологические нарушения, которые существенно влияют на качество жизни. Функциональное восстановление после лечения часто ограничено, особенно в хронических, обширных случаях с устоявшимся неврологическим дефицитом. Ранняя диагностика и агрессивное лечение потенциальных причин (например, быстрое лечение менингита, тщательная хирургическая техника, отказ от старых миелографических агентов) могут помочь предотвратить его развитие.
![]() Внимание! Арахноидит — это сложное заболевание, часто приводящее к хронической боли и инвалидности. Диагностика требует тщательной клинической оценки и специализированной визуализации. Лечение представляет собой сложную задачу и требует междисциплинарного подхода с участием неврологов, нейрохирургов, специалистов по лечению боли и физиотерапевтов. Самодиагностика или опора на недоказанные методы лечения настоятельно не рекомендуются. Обратитесь к опытным медицинским специалистам для точной диагностики и выбора вариантов лечения.
Внимание! Арахноидит — это сложное заболевание, часто приводящее к хронической боли и инвалидности. Диагностика требует тщательной клинической оценки и специализированной визуализации. Лечение представляет собой сложную задачу и требует междисциплинарного подхода с участием неврологов, нейрохирургов, специалистов по лечению боли и физиотерапевтов. Самодиагностика или опора на недоказанные методы лечения настоятельно не рекомендуются. Обратитесь к опытным медицинским специалистам для точной диагностики и выбора вариантов лечения.
Литература
- Wright MH, Denney LC. A comprehensive review of spinal arachnoiditis. Orthop Nurs. 2003 May-Jun;22(3):215-9; quiz 220-1. doi: 10.1097/00006416-200305000-00008
- Aldrete JA. Chronic Adhesive Arachnoiditis. Springer; 2011.
- Doležal M, Vizváry Z, Srp A, Chaloupský R. Spinal adhesive arachnoiditis. Review. Neuro Endocrinol Lett. 2019;40(2):61-66.
- Pantanowitz L, Hatae M, Fitt G, Miller DC. Pathology of arachnoiditis. Surg Neurol Int. 2011;2:90. doi: 10.4103/2152-7806.82567
- Chapter 32: Inflammatory diseases. In: Ropper AH, Samuels MA, Klein JP, Prasad S. Adams and Victor's Principles of Neurology. 11th ed. McGraw Hill; 2019.
- Greenberg MS. Handbook of Neurosurgery. 9th ed. Thieme; 2020.
- Osborn AG, Salzman KL, Jhaveri MD, et al. Osborn's Brain. 2nd ed. Elsevier; 2018.
- Walsh FB, Hoyt WF. Clinical Neuro-Ophthalmology. 4th ed. Williams & Wilkins; 1982-1991.
- Anderson TL, et al. Imaging of Spinal Arachnoiditis. Neuroimaging Clin N Am. 2017 Feb;27(1):93-106. doi: 10.1016/j.nic.2016.09.005
- Jinkins JR. MR of adhesive arachnoiditis. AJNR Am J Neuroradiol. 1993 May-Jun;14(3):764-6.
- Guyer DW, et al. Arachnoiditis. Orthop Clin North Am. 2019 Apr;50(2):181-191. doi: 10.1016/j.ocl.2018.12.003
- Deer TR, et al. The Polyanalgesic Consensus Conference (PACC): Recommendations for Intrathecal Drug Delivery: Guidance for Improving Safety and Reducing Serious Adverse Events. Neuromodulation. 2017;20(2):155-176. doi: 10.1111/ner.12579
Смотрите также
- Анатомия нервной системы
- Инфекционные заболевания головного мозга:
- Абсцесс полушарий головного мозга и мозжечка
- Эозинофильная гранулёма, лангергансоклеточный гистиоцитоз, фистульный симптом Эннебера
- Абсцесс эпидуральный
- Внутричерепные осложнения заболеваний носа
- Внутричерепные осложнения заболеваний уха
- Глазничные осложнения заболеваний носа
- Менингит гнойный отогенный
- Абсцесс субдуральный
- Тромбофлебит сигмовидного синуса и септикопиемия
- Коллоидная киста головного мозга 3 мозгового желудочка
- Арахноидит церебральный и оптико-хиазмальный
- Кортикобазальная ганглиозная дегенерация (ограниченная атрофия головного мозга)
- Энцефалопатия
- Головная боль, мигрень
- Черепно-мозговая травма (сотрясение, ушиб мозга, ДАП)
- Внутричерепное давление (гипертензия, гипотензия) и гидроцефалия
- Паркинсона болезнь
- Аденома гипофиза (микроаденома, макроаденома, нефункционирующая аденома), синдром гиперпролактинемии
- Спонтанная краниальная ликворея