პარკინსონის დაავადება და პარკინსონიზმი
პარკინსონის დაავადებისა და პარკინსონიზმის მიმოხილვა
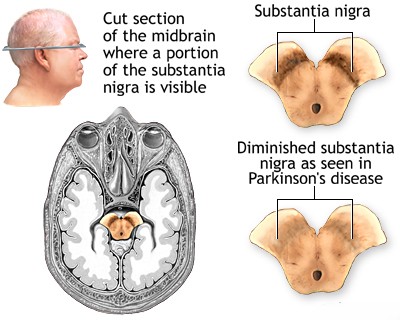
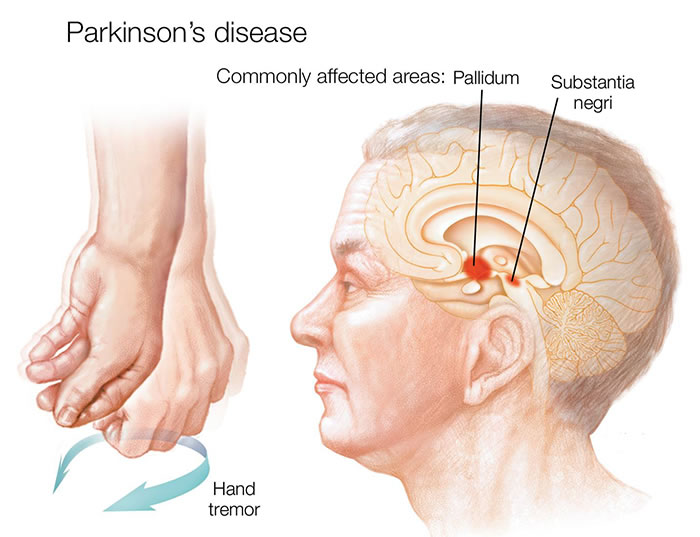
პარკინსონის დაავადება (PD) არის ქრონიკული, პროგრესირებადი ნეიროდეგენერაციული აშლილობა, რომელიც უპირველესად ხასიათდება მოტორული სიმპტომებით, რაც გამოწვეულია შუა ტვინის სპეციფიკურ რეგიონში, რომელსაც ეწოდება შავი ნივთიერების კომპაქტური ნაწილი (substantia nigra pars compacta - SNc), დოფამინის მწარმოებელი (დოფამინერგული) ნეირონების მნიშვნელოვანი დანაკარგით [1]. ეს SNc ნეირონები ნორმაში ნიგროსტრიატული გზის მეშვეობით პროეცირდებიან ბაზალურ განგლიებში (კონკრეტულად სტრიატუმში: კუდიან ბირთვსა და ფუთაში), ცერებრალური ნახევარსფეროების სიღრმეში მდებარე სტრუქტურებში, რომლებიც გადამწყვეტია ნებაყოფლობითი მოძრაობის დაწყებისა და კონტროლისთვის, მოტორული სწავლისთვის, ჩვევების ფორმირებისთვის და სხვა ფუნქციებისთვის.
დოფამინი მოქმედებს როგორც საკვანძო ნეიროტრანსმიტერი, რომელიც არეგულირებს აქტივობას ბაზალური განგლიების სქემებში (პირდაპირი და არაპირდაპირი გზები). პარკინსონის დაავადების დროს დოფამინერგული ნეირონების პროგრესირებადი დეგენერაცია იწვევს დოფამინის მნიშვნელოვან დეფიციტს სტრიატუმში, რაც არღვევს ამ სქემების ნაზ ბალანსს [2].
დოფამინის ეს დეფიციტი არღვევს ბაზალური განგლიების მოტორული მარყუჟების ნორმალურ ფუნქციონირებას, რაც იწვევს კარდინალურ მოტორულ სიმპტომებს, რომლებიც ერთობლივად ცნობილია როგორც პარკინსონიზმი. მიმდინარე კლინიკური სადიაგნოსტიკო კრიტერიუმების მიხედვით (მაგ., MDS კლინიკური სადიაგნოსტიკო კრიტერიუმები პარკინსონის დაავადებისთვის), პარკინსონიზმი განისაზღვრება ბრადიკინეზიის არსებობით სხვა ორი კარდინალური ნიშნიდან სულ მცირე ერთთან კომბინაციაში: რიგიდულობა ან მოსვენების ტრემორი [3].
- ბრადიკინეზია: მოძრაობის სინელე და სიღარიბე. ეს ითვლება პარკინსონიზმის ყველაზე დამახასიათებელ თვისებად და მოიცავს მოძრაობის დაწყების სირთულეს (აკინეზია), მოძრაობის სიჩქარის შემცირებას, და განმეორებითი მოქმედებების დროს ამპლიტუდისა და სიჩქარის პროგრესულ შემცირებას (მიმდევრობის ეფექტი).
- კუნთების რიგიდულობა: გაზრდილი წინააღმდეგობა პასიური მოძრაობის მიმართ მოძრაობის მთელ დიაპაზონში, რომელსაც შეიგრძნობს გამომკვლევი. შეიძლება იყოს გლუვი ("ტყვიის მილის") ან კბილანისებრი ("კბილანა ბორბლის" რიგიდულობა, ხშირად ზედდებული ტრემორით).
- მოსვენების ტრემორი: უნებლიე კანკალი, ტიპიურად იწყება ცალმხრივად კიდურში (ხშირად ხელი ან ფეხი, ზოგჯერ ყბა/ტუჩი), ყველაზე თვალსაჩინოა, როდესაც კიდური სრულად არის დაყრდნობილი და მოსვენებულ მდგომარეობაშია, ხშირად დროებით ითრგუნება ნებაყოფლობითი მოძრაობით. სიხშირე ჩვეულებრივ არის 4-6 ჰც. ხელში დამახასიათებელი "აბების გორების" იერსახე ხშირია.
- პოსტურალური არასტაბილურობა: დაქვეითებული წონასწორობის რეფლექსები, რაც იწვევს არასტაბილურობას და დაცემას. მიუხედავად იმისა, რომ პარკინსონიზმის ნაწილია, ის ტიპიურად გვხვდება იდიოპათიური პარკინსონის დაავადების მოგვიანებით ეტაპზე და მისი ადრეული გამოხატულება არის "წითელი დროშა", რომელიც მიუთითებს ატიპიურ პარკინსონიზმზე [3].
PD-ს დიაგნოზის მხარდამჭერი სხვა ასოცირებული მოტორული მახასიათებლები შეიძლება მოიცავდეს მიკროგრაფიას (მცირე, შეკუმშული ხელწერა), ჰიპოფონიას (რბილი, მონოტონური მეტყველება), ნიღბისებრ სახეს (შემცირებული მიმიკა, "პოკერის სახე"), თვალის დახამხამების სიხშირის შემცირებას, სიარულის გაყინვას და არეულ სიარულს მკლავების რხევის შემცირებით.
გადამწყვეტია პარკინსონის დაავადების (PD), სპეციფიკური ნეიროდეგენერაციული აშლილობის, რომელიც პათოლოგიურად ხასიათდება SNc ნეირონების დაკარგვით და ლუის სხეულების (შეიცავს ალფა-სინუკლეინს) წოდებული ინტრანეირონული ცილოვანი აგრეგატების არსებობით, დიფერენცირება პარკინსონიზმის უფრო ფართო კლინიკური სინდრომისგან. პარკინსონიზმი შეიძლება გამოწვეული იყოს PD-ს გარდა სხვა პირობებით, მათ შორის გარკვეული მედიკამენტებით (წამლით გამოწვეული პარკინსონიზმი), სხვა ნეიროდეგენერაციული დარღვევებით (ატიპიური პარკინსონიზმი, როგორიცაა მრავლობითი სისტემური ატროფია [MSA], პროგრესირებადი სუპრანუკლეარული დამბლა [PSP], კორტიკობაზალური დეგენერაცია [CBD]), სისხლძარღვოვანი პარკინსონიზმით (ინსულტების გამო), ნორმალური წნევის ჰიდროცეფალიით (NPH), ინფექციებით (პოსტ-ენცეფალიტური პარკინსონიზმი - ახლა იშვიათია), ტოქსინებითა და ტრავმით [4].
პარკინსონის დაავადებისა და პარკინსონიზმის დიაგნოსტიკა
პარკინსონის დაავადების (PD) დიაგნოზი რჩება უპირველესად კლინიკური, დაფუძნებული პაციენტის სამედიცინო ისტორიის, მოხსენებული სიმპტომების და დეტალური ნევროლოგიური გამოკვლევის აღმოჩენების ფრთხილ ინტერპრეტაციაზე, რომელსაც ატარებს გამოცდილი კლინიცისტი, იდეალურად მოძრაობის დარღვევებზე სპეციალიზებული ნევროლოგი. ამჟამად არ არსებობს ერთი საბოლოო ბიოლოგიური მარკერი ან სადიაგნოსტიკო ტესტი (როგორიცაა სისხლის ანალიზი ან ტვინის სტანდარტული სკანირება), რომელსაც შეუძლია ცალსახად დაადასტუროს იდიოპათიური პარკინსონის დაავადება სიცოცხლის განმავლობაში, თუმცა კვლევები გრძელდება [5]. საბოლოო დიაგნოზი კვლავ მოითხოვს SNc ნეირონების დაკარგვისა და ლუის სხეულების პათოლოგიის პოსტ-მორტემ ნეიროპათოლოგიურ დადასტურებას.
კლინიკური სადიაგნოსტიკო კრიტერიუმები, როგორიცაა გაერთიანებული სამეფოს პარკინსონის დაავადების საზოგადოების ტვინის ბანკის ან უფრო ახალი მოძრაობის დარღვევების საზოგადოების (MDS) კლინიკური დიაგნოსტიკური კრიტერიუმების მიერ დადგენილი, უზრუნველყოფს სტანდარტიზებულ ჩარჩოს [3]. ძირითადი სადიაგნოსტიკო ნაბიჯები მოიცავს:
- პარკინსონიზმის დადგენა: ეს არის აუცილებელი პირველი ნაბიჯი. პარკინსონიზმი კლინიკურად განისაზღვრება ბრადიკინეზიის (ნებაყოფლობითი მოძრაობის დაწყების სინელე განმეორებითი მოქმედებების დროს სიჩქარისა და ამპლიტუდის პროგრესირებადი შემცირებით) არსებობით შემდეგი ორიდან სულ მცირე ერთთან კომბინაციაში:
- კუნთების რიგიდულობა (ტყვიის მილის ან კბილანა ბორბლის ტიპის).
- მოსვენების ტრემორი (ტიპიურად 4-6 ჰც).
- პარკინსონის დაავადების კრიტერიუმების შეფასება: მას შემდეგ, რაც პარკინსონიზმი დადგინდება, დიაგნოზი იხრება PD-სკენ, თუ:
- არ არსებობს აბსოლუტური გამორიცხვის კრიტერიუმები (იხ. ქვემოთ).
- წარმოდგენილია მინიმუმ ორი მხარდამჭერი კრიტერიუმი (PD-ში ხშირად ნანახი დადებითი მახასიათებლები).
- არ არსებობს "წითელი დროშები" (მახასიათებლები, რომლებიც აჩენენ ეჭვს ალტერნატიულ დიაგნოზზე).
- მკაფიო და დრამატული სასარგებლო პასუხი (გაუმჯობესება >30%) დოფამინერგულ თერაპიაზე (ლევოდოპა).
- ლევოდოპით გამოწვეული დისკინეზიების არსებობა.
- კიდურის მოსვენების ტრემორი, რომელიც შეინიშნება კლინიკურად.
- ყნოსვის დისფუნქციის არსებობა (ყნოსვის დაკარგვა ან დაქვეითება).
- გულის სიმპათიკური დენერვაცია MIBG სცინტიგრაფიაზე (ნაკლებად ხშირად გამოიყენება კლინიკურად).
- გამორიცხვის კრიტერიუმებისა და წითელი დროშების შეფასება: მახასიათებლები, რომლებიც მტკიცედ ეწინააღმდეგება PD-ს ან მიუთითებს ალტერნატიულ დიაგნოზზე (ატიპიური პარკინსონიზმი ან მეორადი პარკინსონიზმი).
აბსოლუტური გამორიცხვის კრიტერიუმები (გამორიცხავს PD-ს, თუ არსებობს):
- ცალსახა ნათხემის ანომალიები (ატაქსია, ნისტაგმი).
- ქვემოთ მიმართული ვერტიკალური სუპრანუკლეარული მზერის დამბლა, ან ქვემოთ მიმართული საკადების შერჩევითი შენელება.
- სავარაუდო ქცევითი ვარიანტის ფრონტოტემპორალური დემენციის ან პირველადი პროგრესირებადი აფაზიის დიაგნოზი პირველი 5 წლის განმავლობაში.
- პარკინსონული მახასიათებლები შეზღუდულია ქვედა კიდურებით 3 წელზე მეტი ხნის განმავლობაში.
- მკურნალობა დოფამინის რეცეპტორების ბლოკერით ან დოფამინის შემამცირებელი აგენტით იმ დოზით და დროით, რომელიც შეესაბამება წამლით გამოწვეულ პარკინსონიზმს.
- მაღალი დოზით ლევოდოპაზე დაკვირვებადი პასუხის არარსებობა დაავადების სულ მცირე ზომიერი სიმძიმის მიუხედავად.
- ცალსახა კორტიკალური სენსორული დაკარგვა, მკაფიო კიდურის იდეომოტორული აპრაქსია, ან პროგრესირებადი აფაზია.
- პრესინაფსური დოფამინერგული სისტემის ნორმალური ფუნქციური ნეიროვიზუალიზაცია (მაგ., ნორმალური DAT სკანირება).
- სიარულის გაუარესების სწრაფი პროგრესირება, რომელიც მოითხოვს ინვალიდის ეტლის რეგულარულ გამოყენებას დაწყებიდან 5 წლის განმავლობაში.
- მოტორული სიმპტომების ან ნიშნების პროგრესირების სრული არარსებობა 5 ან მეტი წლის განმავლობაში, თუ სტაბილურობა არ არის დაკავშირებული მკურნალობასთან.
- ადრეული ბულბარული დისფუნქცია (მძიმე დიზართრია ან დისფაგია პირველი 5 წლის განმავლობაში).
- ადრეული ინსპირატორული რესპირატორული დისფუნქცია (დღის ან ღამის ინსპირატორული სტრიდორი).
- მძიმე ავტონომიური უკმარისობა პირველი 5 წლის განმავლობაში (მაგ., მძიმე ორთოსტატული ჰიპოტენზია, შარდის მძიმე შეკავება/შეუკავებლობა, რომელიც სხვაგვარად არ აიხსნება).
- განმეორებითი დაცემა (>1/წელიწადში) დაქვეითებული წონასწორობის გამო დაწყებიდან 3 წლის განმავლობაში.
- არაპროპორციული ანტეროკოლისი ან კონტრაქტურები პირველი 10 წლის განმავლობაში.
- რაიმე საერთო არამოტორული მახასიათებლის არარსებობა 5 წლიანი დაავადების ხანგრძლივობის მიუხედავად (ძილის დისფუნქცია, ავტონომიური დისფუნქცია, ჰიპოსმია, ფსიქიატრიული).
- სხვაგვარად აუხსნელი პირამიდული ტრაქტის ნიშნები.
- ორმხრივი სიმეტრიული პარკინსონიზმის დაწყება მკაფიო ასიმეტრიის შენარჩუნების გარეშე.
პარკინსონიზმის დიფერენციალური დიაგნოზი
| მდგომარეობა | ძირითადი განმასხვავებელი ნიშნები (ტიპიურ PD-სთან შედარებით) | ტიპიური პასუხი ლევოდოპაზე / დამხმარე ტესტები |
|---|---|---|
| პარკინსონის დაავადება (PD) | ხშირად ასიმეტრიული დაწყება, გამოხატული მოსვენების ტრემორი ხშირია, კარგი პასუხი ლევოდოპაზე თავდაპირველად, ყნოსვის დაკარგვა ხშირია, უფრო ნელი პროგრესირება ადრეულ ეტაპზე. მოტორული ფლუქტუაციების/დისკინეზიების განვითარება მოგვიანებით. არამოტორული სიმპტომები (ყაბზობა, RBD, დეპრესია) ხშირია. | შესანიშნავი/კარგი საწყისი პასუხი ლევოდოპაზე არის მხარდამჭერი. თავის ტვინის მრტ ჩვეულებრივ ნორმალურია. DAT სკანირება პათოლოგიურია (შემცირებული სტრიატალური შთანთქმა, თავდაპირველად ასიმეტრიული). |
| მრავლობითი სისტემური ატროფია (MSA) | პარკინსონიზმის (MSA-P) ან ნათხემის ნიშნების (MSA-C) კომბინაცია პლუს ადრეული, გამოხატული ავტონომიური უკმარისობა (ორთოსტატული ჰიპოტენზია, შარდის შეუკავებლობა/შეკავება, ერექციული დისფუნქცია). +/- პირამიდული ნიშნები, სტრიდორი, ანტეროკოლისი, ემოციური ლაბილობა ("პათოლოგიური სიცილი/ტირილი"). უფრო სწრაფი პროგრესირება. | ხშირად ცუდი ან არამდგრადი პასუხი ლევოდოპაზე. მრტ-მ შეიძლება აჩვენოს სპეციფიკური ნიშნები: ფუთის ატროფია/ჰიპოინტენსივობა/ჰიპერინტენსიური რგოლი ("ნაპრალის ნიშანი" - MSA-P) ან ნათხემის/ხიდის ატროფია ("ცხელი ჯვარედინი ფუნთუშის" ნიშანი - MSA-C). DAT სკანირება პათოლოგიურია. ავტონომიური ფუნქციის ტესტები პათოლოგიურია. |
| პროგრესირებადი სუპრანუკლეარული დამბლა (PSP) | ადრეული პოსტურალური არასტაბილურობა და დაცემა (ხშირად უკან, "რაკეტის ნიშანი"). ვერტიკალური სუპრანუკლეარული მზერის დამბლა (განსაკუთრებით ქვემოთ მზერის შეზღუდვა). სიმეტრიული აქსიალური რიგიდულობა > აპენდიკულარულზე, ბრადიკინეზია. შუბლის წილის ნიშნები (კოგნიტური/ქცევითი ცვლილებები, აპათია, ფსევდობულბარული აფექტი). დისფაგია, დიზართრია ("მღრღნელი მეტყველება"). "გაკვირვებული" სახის გამომეტყველება. | ლევოდოპაზე პასუხი ჩვეულებრივ ცუდია. მრტ-მ შეიძლება აჩვენოს დამახასიათებელი შუა ტვინის ატროფია ("კოლიბრის" ან "პინგვინის" ნიშანი საგიტალურზე), ზედა ნათხემის ფეხის ატროფია. DAT სკანირება პათოლოგიურია. |
| კორტიკობაზალური დეგენერაცია (CBD) / კორტიკობაზალური სინდრომი (CBS) | მკვეთრად ასიმეტრიული პარკინსონიზმი (რიგიდულობა, ბრადიკინეზია, ხშირად დისტონია). ასოცირებული კორტიკალური ნიშნები დაზიანებულ კიდურში: აპრაქსია (კიდურის იდეომოტორული), უცხო კიდურის ფენომენი (კიდური უცხოდ იგრძნობა/უნებლიედ მოძრაობს), კორტიკალური სენსორული დაკარგვა (ასტერეოგნოზია, აგრაფესთეზია), მიოკლონუსი (რეფლექსური ან სპონტანური). კოგნიტური/ქცევითი ცვლილებები ხშირია. | ლევოდოპაზე პასუხი ჩვეულებრივ ცუდია. მრტ-მ შეიძლება აჩვენოს ასიმეტრიული კორტიკალური ატროფია (პერიროლანდური/ფრონტოპარიეტალური, დაზიანებული კიდურის კონტრალატერალური). DAT სკანირება პათოლოგიურია, ხშირად ასიმეტრიული. FDG-PET შეიძლება აჩვენოს ასიმეტრიული ჰიპომეტაბოლიზმი. |
| დემენცია ლუის სხეულებით (DLB) | პარკინსონიზმი ვითარდება დემენციის დაწყებიდან ერთი წლის განმავლობაში (ან ერთდროულად). ძირითადი მახასიათებლები: მერყევი კოგნიცია/სიფხიზლე, განმეორებითი რთული ვიზუალური ჰალუცინაციები (ხშირად კარგად ფორმირებული ადამიანები/ცხოველები), სპონტანური პარკინსონიზმი, REM ძილის ქცევითი აშლილობა (RBD). მკვეთრი მგრძნობელობა ანტიფსიქოზური მედიკამენტების მიმართ. | ლევოდოპაზე პასუხი ცვალებადია (შეიძლება გააუმჯობესოს მოტორული, გააუარესოს ფსიქოზი). მრტ ჩვეულებრივ ნორმალურია ან აჩვენებს არასპეციფიკურ ატროფიას. DAT სკანირება პათოლოგიურია. პოლისომნოგრაფია ადასტურებს RBD-ს. |
| წამლით გამოწვეული პარკინსონიზმი (DIP) | დოფამინის რეცეპტორების ბლოკირებადი აგენტების (ტიპიური/ატიპიური ანტიფსიქოტიკები - რისპერიდონი, ჰალოპერიდოლი; ღებინების საწინააღმდეგო საშუალებები - მეტოკლოპრამიდი, პროქლორპერაზინი) ან დოფამინის შემამცირებლების (ტეტრაბენაზინი) ექსპოზიციის ისტორია. ხშირად სიმეტრიული პარკინსონიზმი. ტრემორი შეიძლება იყოს ნაკლებად გამოხატული ან პოსტურალური. შეიძლება ჰქონდეს ასოცირებული გვიანი დისკინეზია ან აკათიზია. | არ არის პასუხი ლევოდოპაზე. სიმპტომები უმჯობესდება/გადის გამომწვევი წამლის შეჩერების შემდეგ (შეიძლება კვირებიდან თვეებამდე დასჭირდეს). DAT სკანირება ტიპიურად ნორმალურია (განასხვავებს PD/ატიპიური სინდრომებისგან). |
| სისხლძარღვოვანი პარკინსონიზმი (VP) | ხშირად სხეულის ქვედა ნაწილის უპირატესი პარკინსონიზმი ("ქვედა ნახევარი" ან "სისხლძარღვოვანი ფსევდოპარკინსონიზმი") სიარულის დარღვევით (გაყინვა, მოკლე არეული ნაბიჯები, ფართო ბაზა, "სიარულის აპრაქსია"), რომელიც არაპროპორციულია ზედა კიდურების ნიშნებთან. ინსულტ(ებ)ის ან გამოხატული სისხლძარღვოვანი რისკ-ფაქტორების (ჰიპერტენზია, დიაბეტი) ისტორია. +/- პირამიდული ნიშნები, კოგნიტური დაქვეითება (სისხლძარღვოვანი დემენცია), ფსევდობულბარული აფექტი. ტრემორი ნაკლებად ხშირია/გამოხატული. | ტიპიურად ცუდი პასუხი ლევოდოპაზე. თავის ტვინის მრტ აჩვენებს მნიშვნელოვან ცერებროვასკულურ დაავადებას (მრავლობითი ლაკუნური ინფარქტები, თეთრი ნივთიერების ვრცელი ჰიპერინტენსივობები, სტრატეგიული ინფარქტები ბაზალურ განგლიებში/თალამუსში/სუბკორტიკალურ რეგიონებში). DAT სკანირების შედეგი ცვალებადია (შეიძლება იყოს ნორმალური ან პათოლოგიური სისხლძარღვოვანი დაზიანებების ადგილმდებარეობის მიხედვით). |
| ესენციური ტრემორი (ET) | უპირველესად პოსტურალური და სამოქმედო ტრემორი (კინეტიკური ტრემორი), რომელიც მოქმედებს ხელებზე/მკლავებზე (ხშირად ორმხრივი, მაგრამ შეიძლება იყოს ასიმეტრიული), თავზე ("კი-კი" ან "არა-არა"), ან ხმაზე. არ არის მნიშვნელოვანი ბრადიკინეზია, რიგიდულობა, ან მოსვენების ტრემორის კომპონენტი. ოჯახური ისტორია ხშირია (~50%). ალკოჰოლი ხშირად უზრუნველყოფს დროებით გაუმჯობესებას. | არ არის პასუხი ლევოდოპაზე. ნევროლოგიური გამოკვლევა სხვა მხრივ ტიპიურად ნორმალურია (არ არის ბრადიკინეზია/რიგიდულობა). DAT სკანირება ნორმალურია. |
| ნორმალური წნევის ჰიდროცეფალია (NPH) | კლასიკური ტრიადა: სიარულის დარღვევა (მაგნიტური, ფართო ბაზაზე, არეული, დაწყების სირთულე), კოგნიტური დაქვეითება (ფრონტო-სუბკორტიკალური ტიპი), შარდის შეუკავებლობა. პარკინსონიზმის მახასიათებლები (განსაკუთრებით სხეულის ქვედა ნაწილის ბრადიკინეზია/რიგიდულობა) შეიძლება მოხდეს, მაგრამ ტრემორი ნაკლებად ხშირია. | ცვალებადი ან არავითარი პასუხი ლევოდოპაზე. თავის ტვინის მრტ აჩვენებს ვენტრიკულომეგალიას სულკალური ატროფიის არაპროპორციულად (ევანსის ინდექსი >0.3), წყალსადენის ნაკადის შესაძლო სიცარიელეს, პერივენტრიკულური თეთრი ნივთიერების ცვლილებებს. დიდი მოცულობის ლუმბალურმა პუნქციამ (ლიკვორის გამოშვების ტესტი) შეიძლება გამოიწვიოს სიარულის დროებითი გაუმჯობესება. შეიძლება მოითხოვოს ლიკვორის შუნტის ოპერაცია. |
მიუხედავად იმისა, რომ გამოცდილი ნევროლოგის მიერ კლინიკური დიაგნოზი ძალზე ზუსტია (ხშირად >90% დადგენილი კრიტერიუმების გამოყენებისას), დამხმარე ტესტები შეიძლება დაგვეხმაროს კონკრეტულ სიტუაციებში ან დაგვეხმაროს მიმიკებისგან დიფერენცირებაში:
- თავის ტვინის მრტ: ძირითადად გამოიყენება სტრუქტურული მიმიკების (სიმსივნეები, ინსულტები, ჰიდროცეფალია) გამოსარიცხად. სტანდარტული მრტ მიმდევრობები ჩვეულებრივ ნორმალურია ან აჩვენებს არასპეციფიკურ ასაკთან დაკავშირებულ ცვლილებებს იდიოპათიური PD-ს დროს. სპეციფიკურმა მიმდევრობებმა ან აღმოჩენებმა შეიძლება მიუთითოს ატიპიურ პარკინსონიზმზე (მაგ., ატროფიის პატერნები MSA/PSP-ში, ვრცელი სისხლძარღვოვანი დაავადება VP-ში).
- დოფამინის ტრანსპორტიორის სკანირება (DAT Scan, მაგ., DaTscan™ 123I-ioflupane SPECT-ის გამოყენებით): ასახავს პრესინაფსური დოფამინის ტრანსპორტიორების მთლიანობას სტრიატუმში. შემცირებული შთანთქმა დამახასიათებელია ნეიროდეგენერაციული პარკინსონიზმისთვის (PD, MSA, PSP, CBD, DLB), სადაც ნიგროსტრიატული გზა დაზიანებულია. ნორმალური DAT სკანირება მკაცრად ეწინააღმდეგება ამ პირობებს და მხარს უჭერს დიაგნოზებს, როგორიცაა ესენციური ტრემორი, წამლით გამოწვეული პარკინსონიზმი, ან ფსიქოგენური პარკინსონიზმი [6]. შენიშვნა: ის ვერ განასხვავებს PD-ს ატიპიური სინდრომებისგან.
- პასუხი ლევოდოპას გამოცდაზე: ძლიერი, მდგრადი გაუმჯობესება მოტორულ სიმპტომებში ლევოდოპას ადეკვატური გამოცდის შემდეგ (მაგ., 1000მგ/დღემდე რამდენიმე კვირის/თვის განმავლობაში) ძლიერ უჭერს მხარს PD-ს, თუმცა ზოგიერთმა ატიპიურმა სინდრომმა შეიძლება აჩვენოს მსუბუქი ან გარდამავალი პასუხი. მკაფიო სარგებლის ნაკლებობა ხდის PD-ს ნაკლებად სავარაუდოს [7].
- ყნოსვის ტესტირება: ფორმალურმა ტესტირებამ შეიძლება გამოავლინოს ჰიპოსმია ან ანოსმია, რაც ძალიან ხშირია (>90%) PD-ში, ხშირად წინ უძღვის მოტორულ სიმპტომებს. მიუხედავად იმისა, რომ არ არის სპეციფიკური (ასევე გვხვდება სხვა პირობებში), ნორმალური ყნოსვის შეგრძნება ხდის PD-ს ნაკლებად სავარაუდოს [8].
- სხვა: ავტონომიური ფუნქციის ტესტირება (MSA-სთვის), პოლისომნოგრაფია (RBD-სთვის სინუკლეინოპათიებში, როგორიცაა PD/DLB/MSA), MIBG გულის სცინტიგრაფია (აჩვენებს გულის სიმპათიკურ დენერვაციას PD/DLB-ში, ჩვეულებრივ ნორმალურია MSA/PSP-ში), ნეიროფსიქოლოგიური ტესტირება (კოგნიტური პატერნებისთვის), გენეტიკური ტესტირება (თუ ეჭვია ოჯახურ/ახალგაზრდა ასაკში დაწყებულზე) შეიძლება გამოყენებულ იქნას კონკრეტულ კონტექსტში.
მიუხედავად იმისა, რომ სტანდარტული თავის ტვინის მაგნიტურ-რეზონანსული ტომოგრაფია (მრტ) ხშირად შეუმჩნეველია ადრეული პარკინსონის დაავადების დროს, ის ხშირად სრულდება სადიაგნოსტიკო გამოკვლევის დროს, უპირველესად პარკინსონიზმის სხვა სტრუქტურული მიზეზების გამოსარიცხად, როგორიცაა ინსულტი, სიმსივნეები, ჰიდროცეფალია, ან ატროფიის სპეციფიკური პატერნები, რომლებიც მიუთითებენ ატიპიურ პარკინსონულ სინდრომებზე. ფუნქციური ვიზუალიზაცია, როგორიცაა DAT სკანირება, უშუალოდ აფასებს დოფამინის სისტემას.
PD-ის დიფერენცირება პარკინსონიზმის სხვა მიზეზებისგან ("პარკინსონ-პლუს" სინდრომები ან მეორადი პარკინსონიზმი) გადამწყვეტია, რადგან პროგნოზი და მკურნალობაზე პასუხი მნიშვნელოვნად განსხვავდება. წამლით გამოწვეული პარკინსონიზმი ხშირად უმჯობესდება ან გადის გამომწვევი მედიკამენტის მოხსნის შემდეგ. ატიპიური პარკინსონული სინდრომები (MSA, PSP, CBD) ზოგადად აქვთ პროგრესირების უფრო სწრაფი ტემპი, უვითარდებათ დამატებითი დამაინვალიდებელი მახასიათებლები უფრო ადრე (ავტონომიური უკმარისობა, დაცემა, მზერის დამბლა, კორტიკალური ნიშნები, დემენცია) და ცუდად ან გარდამავალად რეაგირებენ ლევოდოპაზე ტიპიურ PD-სთან შედარებით.
კოგნიტური დაქვეითება და დემენცია არის PD-ის საერთო არამოტორული მახასიათებლები, მაგრამ ტიპიურად ვითარდება დაავადების მიმდინარეობის მოგვიანებით ეტაპზე (ხშირად მოტორული დაწყებიდან მრავალი წლის შემდეგ) – ამას ეწოდება პარკინსონის დაავადების დემენცია (PDD). თუ მნიშვნელოვანი დემენცია ვლინდება ძალიან ადრე, კონკრეტულად მოტორული სიმპტომების დაწყებიდან პირველი წლის განმავლობაში, დიაგნოზი ჩვეულებრივ ითვლება დემენციად ლუის სხეულებით (DLB) მიმდინარე კონსენსუსის კრიტერიუმების მიხედვით [9]. დემენციის გავრცელება მნიშვნელოვნად იზრდება ასაკთან და დაავადების ხანგრძლივობასთან ერთად PD-ში, პოტენციურად მოქმედებს პაციენტების 80%-მდე ძალიან განვითარებულ ეტაპებზე (>15-20 წლის ხანგრძლივობა)[10].
პარკინსონის დაავადებისა და პარკინსონიზმის მკურნალობა
მიუხედავად იმისა, რომ ამჟამად არ არსებობს განკურნება, რომელიც აჩერებს ან აბრუნებს ძირითად ნეიროდეგენერაციას პარკინსონის დაავადების დროს, ხელმისაწვდომია რიგი ეფექტური მკურნალობა სიმპტომების სამართავად, ცხოვრების ხარისხის მნიშვნელოვნად გასაუმჯობესებლად და ფუნქციისა და დამოუკიდებლობის შესანარჩუნებლად მრავალი წლის განმავლობაში[11]. მკურნალობა არის უაღრესად ინდივიდუალიზებული, მორგებული კონკრეტულ სიმპტომებზე, დაავადების სტადიაზე, ფუნქციური დაქვეითების ხარისხზე, ასაკზე, ცხოვრების წესზე, თანმხლებ დაავადებებზე და პაციენტის პრეფერენციებზე. მართვა ტიპიურად მოიცავს ფარმაკოლოგიური თერაპიების, არსებითი არაფარმაკოლოგიური მიდგომების და ზოგჯერ მოწინავე თერაპიების, როგორიცაა ღრმა ტვინის სტიმულაცია, კომბინაციას.
| სტადია / სიმპტომი | პირველი რიგის მკურნალობა | მოწინავე ვარიანტები |
|---|---|---|
| ადრეული (მსუბუქი, ტრემორ-დომინანტური) | MAO-B ინჰიბიტორი ან დოფამინის აგონისტი | — |
| საშუალო (ბრადიკინეზია/რიგიდობა გამოხატული) | ლევოდოპა/კარბიდოპა | COMT/MAO-B დამატებითი თერაპია |
| მოწინავე (ფლუქტუაციები, დისკინეზია) | ლევოდოპა + დამხმარე საშუალებები | DBS, აპომორფინის ინფუზია, LCIG |
ფარმაკოლოგიური მკურნალობა: მთავარი მიზანია მოტორული სიმპტომების შემსუბუქება დოფამინერგული ფუნქციის გაძლიერებით.
- ლევოდოპა (L-DOPA, ტიპიურად კომბინირებული პერიფერიულ დეკარბოქსილაზას ინჰიბიტორთან, როგორიცაა კარბიდოპა ან ბენსერაზიდი): რჩება ყველაზე ეფექტურ სიმპტომატურ მკურნალობად PD-ის მოტორული მახასიათებლებისთვის, განსაკუთრებით ბრადიკინეზიისა და რიგიდულობისთვის [12]. დოზირებას სჭირდება ფრთხილი ტიტრირება ("დაიწყეთ დაბალი, წადით ნელა"), რათა მოიძებნოს ყველაზე დაბალი ეფექტური დოზა, რომელიც უზრუნველყოფს სარგებელს მწვავე გვერდითი მოვლენების (გულისრევა, ორთოსტატული ჰიპოტენზია) მინიმიზაციისას. გრძელვადიანი გამოყენება ხშირად ასოცირდება მოტორული გართულებების განვითარებასთან:
- გამოფიტვა (Wearing-off): სიმპტომების პროგნოზირებადი დაბრუნება შემდეგი დოზის მიღებამდე.
- დისკინეზიები: უნებლიე, ხშირად ქორეიფორმული ან დისტონიური მოძრაობები, რომლებიც ტიპიურად ხდება ლევოდოპას პიკურ დონეზე ("პიკური დოზის დისკინეზია").
- "ჩართვა-გამორთვის" (On-Off) ფლუქტუაციები: არაპროგნოზირებადი ცვლილებები კარგი მობილურობის პერიოდებს ("ჩართული" დრო) და ცუდ მობილურობას/პარკინსონული სიმპტომების დაბრუნებას ("გამორთული" დრო) შორის.
- დოფამინის აგონისტები (DAs) (მაგ., პრამიპექსოლი, როპინიროლი - ორალური; როტიგოტინი - ტრანსდერმული პლასტირი; აპომორფინი - კანქვეშა ინექცია/ინფუზია სამაშველო/მოწინავე თერაპიისთვის): უშუალოდ ასტიმულირებენ დოფამინის რეცეპტორებს. შეიძლება გამოყენებულ იქნას როგორც საწყისი მონოთერაპია, განსაკუთრებით ახალგაზრდა პაციენტებში (< 60-70), რათა პოტენციურად გადავადდეს ლევოდოპას საჭიროება და შემცირდეს ადრეული მოტორული გართულებების რისკი, ან გამოყენებულ იქნას როგორც დამხმარე თერაპია ლევოდოპასთან მოგვიანებით ეტაპებზე "გამორთული" დროის შესამცირებლად და ლევოდოპას დაბალი დოზების დასაშვებად [13]. DA-ებს ზოგადად აქვთ ნაკლებად ძლიერი მოტორული სარგებელი ვიდრე ლევოდოპას, მაგრამ მოქმედების უფრო ხანგრძლივი ხანგრძლივობა. ისინი ატარებენ გარკვეული გვერდითი მოვლენების უფრო მაღალ რისკს, მათ შორის ჭარბი დღის ძილიანობა, ძილის უეცარი შეტევები, ჰალუცინაციები (განსაკუთრებით ხანდაზმულებში/კოგნიტური დარღვევების მქონე პირებში), პერიფერიული შეშუპება და იმპულსების კონტროლის დარღვევები (ICDs - მაგ., პათოლოგიური აზარტული თამაშები, კომპულსიური შოპინგი, ჰიპერსექსუალობა, გადაჭარბებული კვება), რაც მოითხოვს ფრთხილ მონიტორინგს.
- MAO-B ინჰიბიტორები (მონოამინოქსიდაზა B ინჰიბიტორები) (მაგ., სელეგილინი, რასაგილინი, საფინამიდი): აფერხებენ ფერმენტ MAO-B-ს, რომელიც შლის დოფამინს ტვინში, რითაც იზრდება დოფამინის ხელმისაწვდომობა. უზრუნველყოფენ მსუბუქ სიმპტომატურ სარგებელს როგორც მონოთერაპია ადრეულ დაავადებაში ან შეიძლება გამოყენებულ იქნას დამხმარე საშუალებად ლევოდოპასთან "გამორთული" დროის შესამცირებლად [14]. საფინამიდს ასევე აქვს ანტი-გლუტამატერგული თვისებები, რამაც შეიძლება დაეხმაროს დისკინეზიას.
- COMT ინჰიბიტორები (კატექოლ-O-მეთილტრანსფერაზას ინჰიბიტორები) (მაგ., ენტაკაპონი, ოპიკაპონი): ბლოკავენ ლევოდოპას პერიფერიულ დაშლას COMT-ის მიერ, რითაც ზრდიან ტვინში მიღწეული ლევოდოპას რაოდენობას და ახანგრძლივებენ მის მოქმედებას. გამოიყენება მხოლოდ როგორც დანამატები ლევოდოპასთან "გამოფიტვის" ფენომენის სამართავად [15]. ტოლკაპონი არის კიდევ ერთი COMT ინჰიბიტორი, მაგრამ მოითხოვს ღვიძლის ფუნქციის მონიტორინგს ჰეპატოტოქსიურობის რისკის გამო.
- ამანტადინი: მექანიზმი რთულია (სუსტი NMDA ანტაგონისტი, აძლიერებს დოფამინის გამოყოფას, ანტიქოლინერგული ეფექტები). უზრუნველყოფს მსუბუქ სარგებელს ბრადიკინეზიის, რიგიდულობის და ტრემორის დროს ადრეულ ეტაპზე. განსაკუთრებით სასარგებლოა დაავადების მოგვიანებით ლევოდოპით გამოწვეული დისკინეზიების სამკურნალოდ [16]. გვერდითი მოვლენები შეიძლება მოიცავდეს დაბნეულობას, ჰალუცინაციებს, livedo reticularis, ტერფის შეშუპებას.
- ანტიქოლინერგული საშუალებები (მაგ., ტრიჰექსიფენიდილი, ბენზტროპინი): პირველ რიგში ბლოკავენ აცეტილქოლინის ეფექტებს, ძირითადად სასარგებლოა ტრემორის შესამცირებლად, განსაკუთრებით ახალგაზრდა პაციენტებში (< 60-70), სადაც ტრემორი ჭარბობს. ზოგადად თავს არიდებენ ხანდაზმულებში ან კოგნიტური დარღვევების მქონე პირებში გვერდითი მოვლენების მნიშვნელოვანი რისკის გამო, როგორიცაა დაბნეულობა, მეხსიერების პრობლემები, ჰალუცინაციები, პირის სიმშრალე, ყაბზობა, შარდის შეკავება, ბუნდოვანი მხედველობა.
არაფარმაკოლოგიური თერაპიები: ეს არის მედიკამენტების აუცილებელი დამატებები ოპტიმალური მართვისა და ცხოვრების ხარისხისთვის.
- ფიზიოთერაპია / ვარჯიში: გადამწყვეტია ყველა ეტაპზე. აუმჯობესებს სიარულს, წონასწორობას, მოქნილობას, პოზას, კოორდინაციას და გულ-სისხლძარღვთა ფიტნესს. ამცირებს დაცემის რისკს. სპეციფიკურმა პროგრამებმა, რომლებიც მიმართულია მოძრაობის ამპლიტუდაზე (მაგ., LSVT BIG®), წონასწორობის ვარჯიშმა, ძალისმიერმა ვარჯიშმა, აერობულმა ვარჯიშმა (სიარული, ველოსიპედით სიარული, ცურვა, ცეკვა, როგორიცაა ტანგო) და ტაი ჩიმ აჩვენეს სარგებელი [17]. რეგულარული, მდგრადი ვარჯიში არის მთავარი.
- ოკუპაციური თერაპია: ეხმარება პაციენტებს ადაპტირდნენ ყოველდღიური ცხოვრების აქტივობებთან (ჩაცმა, ჭამა, წერა) და შეცვალონ თავიანთი საშინაო გარემო უსაფრთხოებისა და დამოუკიდებლობის შესანარჩუნებლად მოტორული და არამოტორული სიმპტომების მიუხედავად.
- მეტყველების თერაპია: მიმართავს მეტყველების პრობლემებს (ჰიპოფონია - რბილი ხმა, მონოტონური, დიზართრია) და ყლაპვის სირთულეებს (დისფაგია). სპეციფიკური ინტენსიური პროგრამები, როგორიცაა LSVT LOUD®, ეფექტურია ხმის მოცულობის გასაუმჯობესებლად [18].
- კვებითი მხარდაჭერა: მითითებები ადეკვატური კვებისა და ჰიდრატაციის შენარჩუნებაზე, ყაბზობის მართვაზე (მაღალი ბოჭკოვანი, სითხეები, ვარჯიში) და ზოგჯერ ცილის მიღების დროის კორექტირებაზე ლევოდოპას დოზებთან მიმართებაში (მაღალცილოვანმა საკვებმა ზოგჯერ შეიძლება ხელი შეუშალოს ლევოდოპას შეწოვას).
- ფსიქოლოგიური მხარდაჭერა / ფსიქიკური ჯანმრთელობის დაცვა: გავრცელებული არამოტორული სიმპტომების, როგორიცაა დეპრესიის, შფოთვის, აპათიის, ფსიქოზის (ხშირად მედიკამენტებთან დაკავშირებული) და ძილის დარღვევების მოგვარება კრიტიკულია. შეიძლება საჭირო გახდეს კონსულტაცია, მხარდამჭერი ჯგუფები და შესაბამისი ფსიქოტროპული მედიკამენტები.
- კომპლემენტური თერაპიები: ზოგიერთი პაციენტი იკვლევს თერაპიებს, როგორიცაა მასაჟი, ოსტეოპათია/მანუალური თერაპია, აკუპუნქტურა, იოგა ან მუსიკალური თერაპია სიმპტომების შესამსუბუქებლად (მაგ., ტკივილი, სიხისტე, სტრესი), თუმცა მაღალი ხარისხის მტკიცებულებები ეფექტურობის შესახებ სპეციალურად PD-ის მოტორული სიმპტომებისთვის ხშირად შეზღუდულია. მათ უნდა შეავსონ და არა ჩაანაცვლონ ჩვეულებრივი მტკიცებულებებზე დაფუძნებული მკურნალობა.
მოწინავე თერაპიები / ქირურგიული მკურნალობა: განიხილება PD-ს მქონე შერჩეული პაციენტებისთვის, რომლებსაც აღენიშნებათ დამაინვალიდებელი მოტორული გართულებები (ფლუქტუაციები, დისკინეზიები) ან მედიკამენტებისადმი რეფრაქტერული ტრემორი ოპტიმიზებული ორალური/ტრანსდერმული სამედიცინო მართვის მიუხედავად.
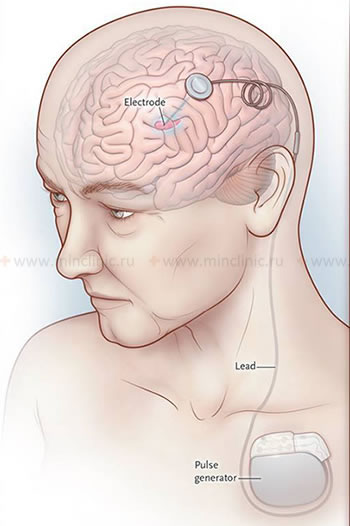
- ღრმა ტვინის სტიმულაცია (DBS): ამჟამად ყველაზე გავრცელებული და ეფექტური ქირურგიული მიდგომაა განვითარებული PD-სთვის [19]. გულისხმობს სტერეოტაქსიურ ტვინის ოპერაციას თხელი ელექტროდების ზუსტად იმპლანტაციისთვის ტვინის სპეციფიკურ ღრმა სამიზნეებში (ყველაზე ხშირად სუბთალამური ბირთვი - STN ან შიდა მკრთალი ბირთვი - GPi). ეს ელექტროდები კანქვეშა მავთულებით უკავშირდება იმპლანტირებულ ნეიროსტიმულატორს (იმპულსების გენერატორი, პეისმეიკერის მსგავსი, ჩვეულებრივ მოთავსებულია გულმკერდის კედელში). მოწყობილობა აწვდის უწყვეტ მაღალი სიხშირის ელექტრულ იმპულსებს ბაზალური განგლიების მიზნობრივ წრედში არანორმალური ნეირონული აქტივობის მოდულირებისთვის. DBS-ს შეუძლია მნიშვნელოვნად გააუმჯობესოს ტრემორი, რიგიდულობა, ბრადიკინეზია, მოტორული ფლუქტუაციები ("ჩართვა-გამორთვის" დრო) და ლევოდოპით გამოწვეული დისკინეზიები, რაც ხშირად იძლევა მედიკამენტების დოზების შემცირების საშუალებას. ის არ კურნავს დაავადებას ან აჩერებს მის პროგრესირებას და ზოგადად ნაკლებად ეფექტურია არამოტორული სიმპტომებისთვის ან აქსიალური სიმპტომებისთვის, როგორიცაა წონასწორობის პრობლემები და სიარულის გაყინვა (თუმცა GPi DBS შეიძლება ოდნავ უკეთესი იყოს სიარულის/დისკინეზიისთვის, STN წამლის შესამცირებლად). პაციენტების ფრთხილი შერჩევა და გამოცდილი მულტიდისციპლინური გუნდი გადამწყვეტია წარმატებისთვის.
- დაზიანების ქირურგია (აბლაციური პროცედურები): ისტორიულად გულისხმობდა ზუსტი, შეუქცევადი დაზიანებების შექმნას ისეთ სამიზნეებში, როგორიცაა თალამუსი (თალამოტომია, უპირველესად ტრემორისთვის) ან მკრთალი ბირთვი (პალიდოტომია, უპირველესად დისკინეზიის/რიგიდულობისთვის). ძირითადად ჩანაცვლებულია DBS-ის რეგულირებადობითა და შექცევადობით, მაგრამ მაინც სრულდება ზოგჯერ კონკრეტულ სიტუაციებში ან ცენტრებში.
- მაგნიტურ-რეზონანსულად მართვადი ფოკუსირებული ულტრაბგერა (MRgFUS): უახლესი, უგანაკვეთო აბლაციური ტექნიკა, რომელიც იყენებს უაღრესად ფოკუსირებულ ულტრაბგერით ტალღებს, რომლებიც იმართება რეალურ დროში მრტ თერმომეტრიით, რათა შეიქმნას ზუსტი თერმული დაზიანებები ტვინის ღრმა სამიზნეებში (მაგ., თალამუსის ვენტრალური შუალედური ბირთვი [Vim] ტრემორისთვის) კრანიოტომიის ან ელექტროდის იმპლანტაციის საჭიროების გარეშე. ამჟამად FDA-ს მიერ დამტკიცებულია პირველ რიგში მედიკამენტებისადმი რეფრაქტერული ესენციური ტრემორისთვის და ტრემორით დომინირებული პარკინსონის დაავადებისთვის (ცალმხრივი თალამოტომია) [20]. კვლევები გრძელდება სხვა სამიზნეებისთვის (მაგ., პალიდოტომია).
- ლევოდოპა-კარბიდოპას ნაწლავური გელის (LCIG) ინფუზია: მოწყობილობით დახმარებული თერაპია, რომელიც მოიცავს ლევოდოპა-კარბიდოპას გელის ფორმულირების უწყვეტ ინფუზიას უშუალოდ თორმეტგოჯა ნაწლავში/მლივ ნაწლავში პერკუტანული ენდოსკოპიური გასტროსტომიის (PEG) მილის მეშვეობით, რომელიც დაკავშირებულია პორტატულ ტუმბოსთან. უზრუნველყოფს უფრო უწყვეტ დოფამინერგულ სტიმულაციას, ეფექტურად ამცირებს "გამორთულ" დროს და დისკინეზიებს განვითარებულ PD-ში მძიმე მოტორული ფლუქტუაციებით [21]. მოითხოვს ტუმბოს და PEG მილის მართვას.
- კანქვეშა აპომორფინის ინფუზია: დოფამინის აგონისტის აპომორფინის უწყვეტი კანქვეშა ინფუზია პორტატული ტუმბოს მეშვეობით. კიდევ ერთი ვარიანტი განვითარებული PD-სთვის რეფრაქტერული მოტორული ფლუქტუაციებით, რაც ამცირებს "გამორთულ" დროს [22]. მოითხოვს ინფუზიის ადგილების მართვას პოტენციური კვანძებისთვის.
პარკინსონის დაავადების მკურნალობა მოითხოვს მიმდინარე მონიტორინგს და პერიოდულ კორექტირებას ნევროლოგის ან მოძრაობის დარღვევების სპეციალისტის მიერ დაავადების პროგრესირებასთან და პაციენტის საჭიროებების განვითარებასთან ერთად. არამოტორული სიმპტომების (მაგ., დეპრესია, შფოთვა, ფსიქოზი, ყაბზობა, დაღლილობა, ძილის დარღვევები, როგორიცაა REM ძილის ქცევითი აშლილობა ან უძილობა, კოგნიტური დაქვეითება/დემენცია) მოგვარება ასევე არის ყოვლისმომცველი, პაციენტზე ორიენტირებული მოვლის კრიტიკული ნაწილი, რაც ხშირად მოითხოვს დამატებით სპეციფიკურ თერაპიებს.
![]() ყურადღებით! პარკინსონის დაავადებისა და პარკინსონული სხვა სინდრომების დიაგნოსტიკა და მართვა რთულია. პარკინსონიზმის მიმანიშნებელი სიმპტომები მოითხოვს შეფასებას ნევროლოგის მიერ, სასურველია ისეთი, რომელიც სპეციალიზირებულია მოძრაობის დარღვევებში, ზუსტი დიაგნოზისა და ინდივიდუალიზებული მკურნალობის დაგეგმვისთვის. თვითდიაგნოსტიკა ან მედიკამენტების შეცვლა სამედიცინო ზედამხედველობის გარეშე შეიძლება საშიში იყოს.
ყურადღებით! პარკინსონის დაავადებისა და პარკინსონული სხვა სინდრომების დიაგნოსტიკა და მართვა რთულია. პარკინსონიზმის მიმანიშნებელი სიმპტომები მოითხოვს შეფასებას ნევროლოგის მიერ, სასურველია ისეთი, რომელიც სპეციალიზირებულია მოძრაობის დარღვევებში, ზუსტი დიაგნოზისა და ინდივიდუალიზებული მკურნალობის დაგეგმვისთვის. თვითდიაგნოსტიკა ან მედიკამენტების შეცვლა სამედიცინო ზედამხედველობის გარეშე შეიძლება საშიში იყოს.
ლიტერატურა
- Dickson DW. Parkinson's disease and parkinsonism: neuropathology. Cold Spring Harb Perspect Med. 2012 Aug;2(8):a009258. doi: 10.1101/cshperspect.a009258
- Obeso JA, et al. The basal ganglia and disorders of movement: pathophysiological mechanisms. J Neurol Neurosurg Psychiatry. 2000;68(2):131-136. doi: 10.1136/jnnp.68.2.131
- Postuma RB, et al. MDS clinical diagnostic criteria for Parkinson's disease. Mov Disord. 2015 Oct;30(12):1591-601. doi: 10.1002/mds.26424
- Jankovic J. Parkinson's disease: clinical features and diagnosis. J Neurol Neurosurg Psychiatry. 2008 Apr;79(4):368-76. doi: 10.1136/jnnp.2007.131045
- Armstrong MJ, Okun MS. Diagnosis and Treatment of Parkinson Disease: A Review. JAMA. 2020 Feb 11;323(6):548-560. doi: 10.1001/jama.2019.22360
- Kägi G, et al. The role of DAT-SPECT in movement disorders. J Neurol Neurosurg Psychiatry. 2010;81(1):5-12. doi: 10.1136/jnnp.2008.157370
- Merims D, Giladi N. Levodopa challenge test for the diagnosis of Parkinson's disease. Mov Disord. 2008;23(10):1469-74. doi: 10.1002/mds.22092
- Doty RL. Olfactory dysfunction in Parkinson disease. Nat Rev Neurol. 2012;8(6):329-39. doi: 10.1038/nrneurol.2012.80
- McKeith IG, et al. Diagnosis and management of dementia with Lewy bodies: Fourth consensus report of the DLB Consortium. Neurology. 2017 Jul 4;89(1):88-100. doi: 10.1212/WNL.0000000000004058
- Aarsland D, et al. Prevalence and characteristics of dementia in Parkinson disease: an 8-year prospective study. Arch Neurol. 2003 Mar;60(3):387-92. doi: 10.1001/archneur.60.3.387
- Bloem BR, Okun MS, Lang AE. Parkinson's disease. Lancet. 2021 Jun 12;397(10291):2284-2303. doi: 10.1016/S0140-6736(21)00218-X
- Fahn S, et al; Parkinson Study Group. Levodopa and the progression of Parkinson's disease. N Engl J Med. 2004 Dec 9;351(24):2498-508. doi: 10.1056/NEJMoa033447
- Rascol O, et al. Ropinirole in the treatment of early Parkinson's disease: a 3-year study. Neurology. 1998;51(5):1460-7. doi: 10.1212/wnl.51.5.1460
- Parkinson Study Group. A controlled trial of rasagiline in early Parkinson disease: the TEMPO study. Arch Neurol. 2002;59(12):1937-43. doi: 10.1001/archneur.59.12.1937
- Brooks DJ, et al; Laroscor Study Group. Opicapone for the management of levodopa-associated motor fluctuations in patients with Parkinson's disease. JAMA Neurol. 2017;74(2):187-195. doi: 10.1001/jamaneurol.2016.4721
- Wolf E, et al. Amantadine for dyskinesia in Parkinson disease: A randomized controlled trial. Neurology. 2010;74(21):1698-705. doi: 10.1212/WNL.0b013e3181e0f4e9
- Tomlinson CL, et al. Physiotherapy versus placebo or no intervention for Parkinson's disease. Cochrane Database Syst Rev. 2013;(9):CD002817. doi: 10.1002/14651858.CD002817.pub4
- Ramig LO, et al. Intensive voice treatment (LSVT) for patients with Parkinson's disease: a 2 year follow up. J Neurol Neurosurg Psychiatry. 2001;71(4):493-8. doi: 10.1136/jnnp.71.4.493
- Deuschl G, et al; DBS study group. A randomized trial of deep-brain stimulation for Parkinson's disease. N Engl J Med. 2006 Aug 31;355(9):896-908. doi: 10.1056/NEJMoa060281
- Bond AE, et al. Magnetic resonance-guided focused ultrasound thalamotomy for essential tremor: 5-year follow-up. J Neurosurg. 2021 Nov 19:1-7. doi: 10.3171/2021.8.JNS211503
- Olanow CW, et al. Continuous intrajejunal infusion of levodopa-carbidopa intestinal gel for patients with advanced Parkinson's disease: a randomised, controlled, double-blind, double-dummy study. Lancet Neurol. 2014 Feb;13(2):141-9. doi: 10.1016/S1474-4422(13)70293-X
- Katzenschlager R, et al; Apomorphine-PUMP study investigators group. Apomorphine subcutaneous infusion in patients with Parkinson's disease with persistent motor fluctuations (TOLEDO): a multicentre, double-blind, randomised, placebo-controlled trial. Lancet Neurol. 2018 Sep;17(9):749-759. doi: 10.1016/S1474-4422(18)30239-4
იხილეთ აგრეთვე
- ანატომია - თავის ტვინი და პერიფერიული ნერვები
- ეოზინოფილური გრანულომა, ლანგერჰანსის უჯრედების ჰისტიოციტოზი, ენებერის ფისტულური სიმპტომი
- თავის ტვინის 3 პარკუჭის კოლოიდური კისტა
- თავის ტვინის ენცეფალოპათია
- თავის ტკივილი, შაკიკი
- თავის ტვინის ინფექციური დაავადებები:
- თავის ტვინის ნახევარსფეროები და ნათხემი აბსცესი
- თავის ტვინის სუბდურული აბსცესი
- თავის ტვინის ეპიდურალური აბსცესი
- თავის ტვინის ჩირქოვანი ოტოგენური მენინგიტი
- ცხვირის ღრუს და მისი დამატებითი წიაღების ანთებითი დაავადებების შიდა ქალას გართულებები
- ცხვირის ღრუს და წიაღების დაავადებების თვალბუდის გართულებები
- ყურის დაავადებების (ოტიტის) შიდა ქალას გართულებები
- კორტიკობაზალური განგლიური დეგენერაცია (თავის ტვინის შეზღუდული ატროფია)
- პარკინსონის დაავადება, პარკინსონიზმი
- სპონტანური კრანიალური ლიკვორეა
- ქალა-ტვინის ტრავმა, თავის ტვინის შერყევა, ტრავმული შეშუპება, კეროვანი და დიფუზური ტრავმა
- შიდა ქალის წნევა და ჰიდროცეფალია
- ცერებრალური და სპინალური არაქნოიდიტი
- ჰიპოფიზის მიკროადენომა, მაკროადენომა და არაფუნქციონირებადი ადენომა (NFPAs), ჰიპერპროლაქტინემიის სინდრომი