Субдуральный абсцесс головного мозга (субдуральная эмпиема)
Обзор субдурального абсцесса головного мозга (субдуральной эмпиемы)
Субдуральный абсцесс головного мозга (чаще называемый субдуральной эмпиемой или внутренним пахименингитом) — это скопление гноя в субдуральном пространстве — потенциальном пространстве между твёрдой мозговой оболочкой и паутинной оболочкой [1]. Это состояние является нейрохирургической экстренной ситуацией из-за быстрого распространения по поверхности мозга и высокой заболеваемости и смертности при отсутствии своевременного лечения [2].
Хотя в целом считается редким осложнением, особенно отогенного генеза, субдуральные эмпиемы чаще всего возникают в результате прямого распространения инфекции из соседних структур: параназальных синусов (синусит, особенно фронтальный — наиболее частый источник), среднего уха/мастоида (отит/мастоидит, преимущественно хронические гнойные формы), реже из менингита, черепно-мозговой травмы или нейрохирургических вмешательств [3]. Гематогенное распространение из отдалённых очагов встречается реже, чем при паренхиматозных абсцессах мозга.
Инфекция часто достигает субдурального пространства через тромбофлебит (воспаление и тромбоз) мостиковых вен, пересекающих субдуральное пространство от синусов или черепа, или путём прямого проникновения через твёрдую оболочку, часто после начального эпидурального абсцесса [4]. Попав в субдуральное пространство, которое не имеет перегородок над полушариями мозга, инфекция может быстро распространяться по поверхности мозга, чаще всего локализуясь на конвекситетах, в межполушарной щели или вдоль намета мозжечка. Хотя чаще всего возникает рядом с источником (например, лобная конвекситет при синусите), возможны контралатеральные или множественные скопления, особенно при гематогенном заносе.
Первоначально воспалительный процесс может проявляться стерильным субдуральным выпотом, но обычно быстро прогрессирует до гнойного скопления (эмпиемы). Подлежащая паутинная и мягкая оболочки часто воспаляются (лептоменингит), а прилежащая кора мозга может быть раздражена, отёчна или подвергнуться тромбофлебиту корковых вен с развитием ишемии или инфаркта.
Значительное скопление гноя может вызывать масс-эффект, сдавливая подлежащий мозг и потенциально приводя к смещению срединных структур или грыжеобразованию. Прямое разрушение через твёрдую оболочку и кость обратно в соседние полости или даже на кожу встречается крайне редко.
Симптомы и течение субдуральной эмпиемы
Субдуральная эмпиема обычно проявляется острым, быстро прогрессирующим заболеванием, развивающимся за несколько дней. Клиническая картина чаще всего более драматична и фульминантна, чем при эпидуральном или паренхиматозном абсцессе мозга [5]. Ключевые признаки:
- Сильная головная боль: Обычно генерализованная и интенсивная, часто самый ранний симптом.
- Высокая лихорадка и озноб: Системные признаки инфекции обычны, часто предшествуют неврологическим симптомам.
- Менингеальные симптомы: Ригидность затылочных мышц, фотофобия, симптомы Кернига/Брудзинского часто присутствуют из-за сопутствующего лептоменингита.
- Изменение сознания: Быстрое прогрессирование от вялости и спутанности до сопора и комы характерно, отражает повышение внутричерепного давления (ВЧД), раздражение/воспаление коры и возможную ишемию.
- Очаговые неврологические дефициты: Очень часты (присутствуют в >80% случаев [2]) из-за прямого сдавления коры, воспаления или тромбофлебита корковых вен с ишемией/инфарктом. Симптомы: контралатеральный гемипарез или гемиплегия, очаговые судороги (часто переходящие в статус эпилептикус), афазия (при доминантном полушарии), дефекты полей зрения.
- Признаки повышения ВЧД: Может развиваться папилледема, тошнота и рвота.
- Симптомы первичного источника: Одновременные проявления синусита (боль/давление в лице, гнойные выделения из носа) или отита (боль в ухе, выделения) могут присутствовать или предшествовать неврологическому ухудшению.
Клиническое течение обычно характеризуется быстрым ухудшением в течение часов-дней при отсутствии срочного лечения. Широкая природа субдурального пространства позволяет гною быстро распространяться, приводя к диффузной дисфункции коры и потенциально жизнеугрожающим осложнениям: отёк мозга, грыжеобразование, тромбоз корковых вен, тромбоз венозных синусов, сепсис.
Диагностика субдуральной эмпиемы
Своевременная диагностика субдуральной эмпиемы критически важна из-за потенциала быстрого неврологического ухудшения. Высокий индекс подозрения необходим у любого пациента с лихорадкой, головной болью, изменением сознания, менингеальными симптомами и очаговыми неврологическими дефицитами, особенно при недавнем синусите, отите, травме головы или нейрохирургическом вмешательстве.
Дифференциальная диагностика субдуральной эмпиемы
| Состояние | Ключевые особенности / отличия | Типичные данные визуализации / лабораторные |
|---|---|---|
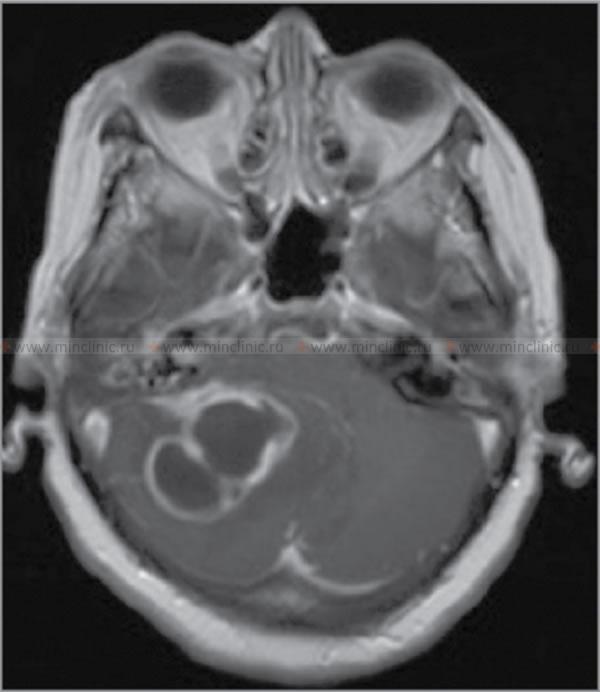
| Субдуральная эмпиема | Острое, быстрое ухудшение. Высокая лихорадка, сильная головная боль, менингизм, очаговые дефициты, судороги часты. История синусита/отита обычна. | MRI: Полулунная/слоистая субдуральная к коллекция, резко ограниченная диффузия (DWI яркая, ADC тёмная), усиливающиеся мембраны (дура/лептоменинкс). CT: может показать коллекцию, усиливающиеся мембраны. LP обычно противопоказана. |
| Эпидуральный абсцесс | Более постепенное начало. Локальная головная боль, лихорадка (~50%). Очаговые дефициты/менингизм редки без осложнений. | MRI/CT: Линзообразная коллекция между черепом и дурой. Усиление прилежащей дуры. Гной может ограничивать диффузию. |
| Бактериальный менингит | Лихорадка, головная боль, ригидность шеи, изменение сознания. Нет фокальной коллекции изначально. Очаговые дефициты/судороги реже, чем при эмпиеме на ранних стадиях. | MRI: Может быть лептоменингеальное усиление. LP (если безопасно) показывает плеоцитоз (нейтрофилы), низкую глюкозу, высокий белок, положительный посев/Грам-окраска. Визуализация часто нормальна на ранних стадиях. |
| Абсцесс мозга (паренхиматозный) | Обычно подострое начало. Головная боль, лихорадка (~50%), очаговые дефициты в зависимости от локализации в мозговой ткани. Менингизм менее выражен, чем при эмпиеме. | MRI/CT: Кольцевидное усиление внутри паренхимы мозга, центральная ограниченная диффузия (DWI яркая), окружающий отёк. |
| Субдуральная гематома (острая/хроническая) | История травмы (в хронической может быть минимальной). Головная боль, колебания сознания, очаговые дефициты. Лихорадка/менингизм отсутствуют без инфицирования (редко). | CT/MRI: Полулунная субдуральная коллекция. Плотность/сигнал зависит от возраста крови. Усиливающиеся мембраны в хронической СГ. Обычно нет ограничения диффузии (кроме гиперострой). Нет лихорадки/высоких маркеров воспаления. |
| Герпетический энцефалит (HSE) | Острое начало лихорадки, головная боль, спутанность, судороги, очаговые дефициты (часто височная доля — афазия, изменения памяти, личности). | MRI: T2/FLAIR гиперинтенсивность +/- кровоизлияния в медиальных височных долях и островке (часто асимметрично двусторонне). LP: лимфоцитарный плеоцитоз, повышенный белок, +/- эритроциты; ПЦР на ДНК HSV положительна. |
| Тромбоз корковых вен / дуральных синусов | Головная боль, судороги, очаговые дефициты (могут имитировать эмпиему), изменение сознания. Могут быть протромботические факторы риска или соседняя инфекция (как причина или следствие). | MRV/CTV подтверждает отсутствие кровотока/тромб в венах/синусах. MRI/CT может показать венозные инфаркты (часто геморрагические). Может сосуществовать с эмпиемой. |
Нейровизуализация, особенно контрастная магнитно-резонансная томография (МРТ) с диффузионно-взвешенным изображением (DWI), имеет решающее значение для диагностики подозреваемой субдуральной эмпиемы.
Диагностические шаги включают:
- Нейровизуализация:
- МРТ с гадолинием: Метод выбора благодаря высокой чувствительности и специфичности [6]. Обычно выявляет коллекцию в субдуральном пространстве, следующую контуру поверхности мозга (полулунная или слоистая), потенциально пересекающую швы, но ограниченную дупликатурами дуры (серп, намет).
- Коллекция часто гипоинтенсивна на T1 и гиперинтенсивна на T2/FLAIR относительно мозговой ткани.
- Выраженное усиление прилежащей дуры и часто подлежащих лептоменинксов после контраста — характерно для воспаления этих оболочек.
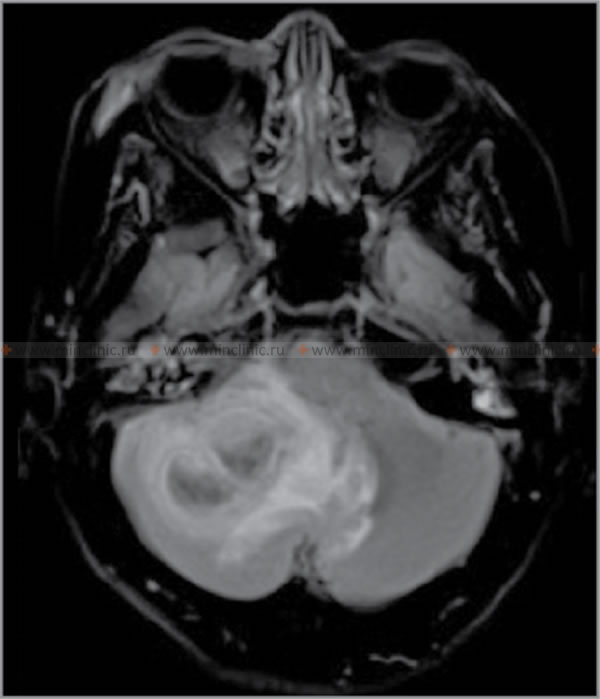
- Диффузионно-взвешенное изображение (DWI) высоко чувствительно, показывает ограниченную диффузию (резко яркий сигнал на DWI, тёмный на ADC-картах) внутри эмпиемы из-за высокой вязкости и клеточности гноя. Это ключевое отличие от стерильных выпотов или хронических гематом.
- МРТ также эффективно показывает сопутствующие осложнения: отёк мозга, масс-эффект, тромбоз корковых вен, церебрит/инфаркт подлежащей паренхимы, гидроцефалию.
- КТ с контрастом: Часто начальная визуализация в экстренных условиях. Может показать гиподенсную или иногда изоденсную полулунную коллекцию в субдуральном пространстве с усилением прилежащих менинксов после контраста. КТ менее чувствительна, чем МРТ, особенно для малых или ранних коллекций и визуализации ограниченной диффузии гноя, но может демонстрировать значительный масс-эффект, смещение срединных структур и сопутствующее заболевание синусов/мастоида или переломы.
- МРТ с гадолинием: Метод выбора благодаря высокой чувствительности и специфичности [6]. Обычно выявляет коллекцию в субдуральном пространстве, следующую контуру поверхности мозга (полулунная или слоистая), потенциально пересекающую швы, но ограниченную дупликатурами дуры (серп, намет).
- Лабораторные тесты: Анализы крови часто показывают выраженный лейкоцитоз с нейтрофилией и значительно повышенные маркеры воспаления (СОЭ, СРБ). Культуры крови следует взять срочно, они могут быть положительными, особенно при сепсисе.
- Люмбальная пункция (ЛП): Обычно **противопоказана** из-за очень высокого риска грыжеобразования мозга при значительном масс-эффекте, часто ассоциированном с субдуральной эмпиемой [4, 2]. Если выполнена случайно или в крайне атипичных случаях, когда подозревается только менингит и визуализация однозначно исключает значительный масс-эффект (редко рекомендуется), ликвор обычно показывает признаки параменингеальной инфекции: высокий белок, высокий лейкоцитоз (преимущественно нейтрофилы) и нормальную или низкую глюкозу. Грам-окраска и посев ликвора часто отрицательны, если нет сопутствующего менингита или прорыва в субарахноидальное пространство.
- Оценка источника: Визуализация параназальных синусов (КТ) или височных костей (КТ) важна для выявления и планирования лечения вероятного первичного источника инфекции.
Диагностика субдуральной эмпиемы только на клинических данных исключительно трудна, поскольку симптомы значительно перекрываются с тяжёлым менингитом, абсцессом мозга и другими внутричерепными инфекциями, и эти состояния могут сосуществовать. Комбинация быстро прогрессирующих неврологических дефицитов, судорог, высокой лихорадки и менингеальных симптомов у пациента с недавним синуситом или отитом должна сильно предполагать субдуральную эмпиему, пока не доказано обратное. Срочное подтверждение нейровизуализацией обязательно.
Лечение субдуральной эмпиемы
Субдуральная эмпиема — **нейрохирургическая экстренная ситуация**, требующая немедленного и агрессивного вмешательства [11].
- Срочное хирургическое дренирование: Быстрое и адекватное дренирование субдурального гнойного скопления имеет решающее значение для выживания и функционального исхода. Обычно достигается путём:
- Краниотомии: Создание большого костного лоскута для широкого доступа к субдуральному пространству, тщательной эвакуации гноя (который может быть распространённым и вязким), рассечения спаек или локализаций, обильного промывания и исследования источника (например, дефект дуры). Часто предпочтительный метод для обширных эмпием для обеспечения полного дренирования [2, 4].
- Бур-холы: Множественные бур-холы стратегически размещаются над коллекцией для дренирования и промывания, иногда с установкой субдуральных катетеров для продолженного дренирования или ирригации после операции. Может применяться при более локализованных, жидких коллекциях или у пациентов, слишком нестабильных для краниотомии, но несёт более высокий риск неполного дренирования и необходимости повторной операции [12].
- Антибиотикотерапия: Высокие дозы антибиотиков широкого спектра внутривенно с хорошим проникновением в ЦНС должны быть начаты немедленно (идеально после взятия культур крови, но без задержки операции). Начальная эмпирическая терапия должна покрывать вероятные возбудители из синусов/уха (стрептококки — включая пенициллинорезистентные штаммы, Haemophilus influenzae, анаэробы) и Staphylococcus aureus (включая MRSA). Типичные схемы: ванкомицин + цефалоспорин III–IV поколения (цефтриаксон, цефепим) + метронидазол. Терапия корректируется по результатам культур и чувствительности из хирургически полученного гноя и продолжается длительно (обычно минимум 3–6 недель внутривенно, иногда дольше), под контролем клинической и визуализационной динамики [8].
- Поддерживающая терапия: Крайне важна и включает мониторинг в отделении интенсивной терапии у тяжёлых пациентов. Лечение направлено на контроль судорог (антиэпилептические препараты часто назначаются профилактически и продолжаются длительно при возникновении судорог), агрессивный контроль лихорадки, управление отёком мозга и возможным повышением ВЧД (хотя обычно менее выражен, чем при внутрипаренхиматозных объёмных образованиях, грыжеобразование всё же возможно), поддержание адекватной церебральной перфузии, баланса жидкости и электролитов, нутритивную поддержку. Применение кортикостероидов (дексаметазон) спорно и обычно не рекомендуется рутинно, резервируется для случаев с тяжёлым отёком и масс-эффектом, вызывающим неврологический дефицит, и используется максимально коротким курсом [1].
Агрессивное лечение, сочетающее своевременное адекватное хирургическое дренирование и длительную таргетную антибиотикотерапию, необходимо для выживания. Несмотря на оптимальное лечение, субдуральная эмпиема сохраняет значительную летальность (исторически высокую, в современных сериях 6–20% [2, 5]) и высокий процент отдалённых неврологических последствий (эпилепсия в 30–50%, гемипарез, когнитивные нарушения) у выживших, что подчёркивает необходимость быстрой диагностики и вмешательства [12].
![]() Внимание! Субдуральная эмпиема — критическая неврологическая экстренная ситуация. Симптомы вроде быстро нарастающей сильной головной боли, высокой лихорадки, ригидности шеи, спутанности сознания, судорог или очаговой слабости требуют немедленного обращения в экстренную службу. Ранняя диагностика и лечение жизненно важны для предотвращения смерти или тяжёлой долгосрочной инвалидности. Никогда не откладывайте обращение за специализированной медицинской помощью при подозрении на субдуральную эмпиему.
Внимание! Субдуральная эмпиема — критическая неврологическая экстренная ситуация. Симптомы вроде быстро нарастающей сильной головной боли, высокой лихорадки, ригидности шеи, спутанности сознания, судорог или очаговой слабости требуют немедленного обращения в экстренную службу. Ранняя диагностика и лечение жизненно важны для предотвращения смерти или тяжёлой долгосрочной инвалидности. Никогда не откладывайте обращение за специализированной медицинской помощью при подозрении на субдуральную эмпиему.
Список литературы
- Osborn AG, Salzman KL, Jhaveri MD, et al. Osborn's Brain. 2nd ed. Elsevier; 2018.
- Nathoo N, Nadvi SS, van Dellen JR, Gouws E. Intracranial subdural empyemas in the era of computed tomography: a review of 699 cases. Neurosurgery. 1999;44(3):529-35.
- Brouwer MC, van de Beek D. Epidemiology, diagnosis, and treatment of brain abscesses. Curr Opin Infect Dis. 2017;30(1):129-134.
- Greenberg MS. Handbook of Neurosurgery. 9th ed. Thieme; 2020.
- Osman Farah M, et al. Subdural Empyema: A Single Institution Experience. World Neurosurg. 2018;111:e429-e435.
- Wong AM, et al. The role of diffusion-weighted imaging in the diagnosis and management of intracranial infections. Neuroimaging Clin N Am. 2004;14(2):177-95.
- Lai PH, Hsu SS, Ding SW, et al. Brain abscess and necrotic brain tumor: discrimination with proton MR spectroscopy and diffusion-weighted imaging. AJNR Am J Neuroradiol. 2002;23(8):1369-77.
- Chapter 91: Brain Abscess and Other Parameningeal Infections. In: Bennett JE, Dolin R, Blaser MJ, eds. Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases. 9th ed. Elsevier; 2020.
- Sexton DJ, et al. Spinal epidural abscess. UpToDate. Accessed [Insert Access Date - e.g., April 20, 2024]. (Subscription required - principles often similar to cranial)
- Germiller JA, Monin DL, Sparano AM, et al. Intracranial complications of sinusitis in children and adolescents and their outcomes. Arch Otolaryngol Head Neck Surg. 2006;132(9):969-76.
- Tunkel AR, Hasbun R, Bhimraj A, et al. 2017 Infectious Diseases Society of America’s Clinical Practice Guidelines for Healthcare-Associated Ventriculitis and Meningitis. Clin Infect Dis. 2017;64(6):e34-e65.
- French H, Schaefer N, Keijzers G, Barison D, Olson S. Subdural empyema: a review of the literature. J Clin Neurosci. 2014;21(12):2037-41.
Дополнительно
- Анатомия нервной системы
- Инфекционные заболевания головного мозга:
- Абсцесс полушарий головного мозга и мозжечка
- Абсцесс субдуральный
- Абсцесс эпидуральный
- Внутричерепные осложнения заболеваний носа
- Внутричерепные осложнения заболеваний уха
- Глазничные осложнения заболеваний носа
- Менингит гнойный отогенный
- Тромбофлебит сигмовидного синуса и септикопиемия
- Эозинофильная гранулёма, лангергансоклеточный гистиоцитоз, фистульный симптом Эннебера
- Коллоидная киста головного мозга 3 мозгового желудочка
- Паркинсона болезнь
- Сотрясение и ушиб мозга (ЧМТ)
- Спонтанная краниальная ликворея
- Функциональные заболевания головного мозга:
- Энцефалопатия